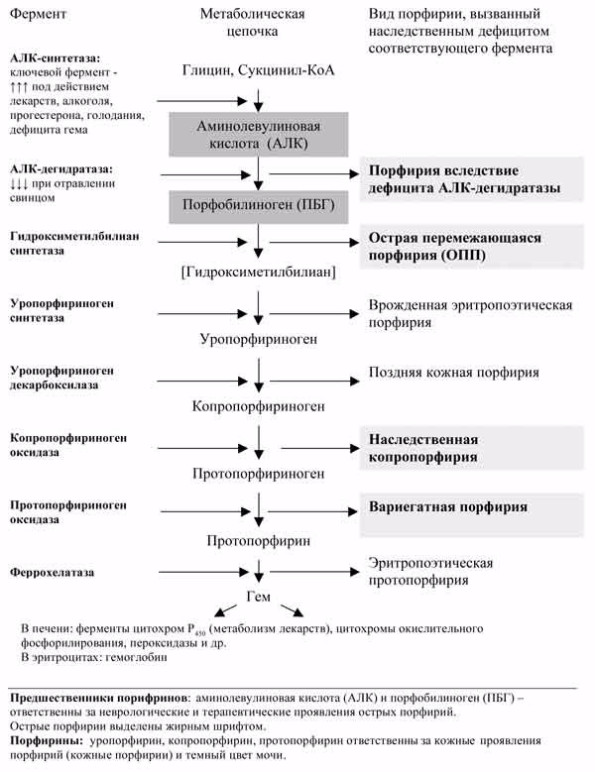
Основная часть синтезируемых порфиринов эритробластов идет на образование Нв, а неиспользованные порфирины и их предшественники выделяются с мочой и калом.
Различные типы порфиринов (уро-копро-прото) образуются в зависимости от того, какими радикалами замещены атомы водорода в порфине. Названы по источнику первоначального выделения.
Порфирины в моче — преимущественно копропорфирины > уропорфирины > порфобилиноген и ДАЛК. Основной источник – печень, меньше эритронормобласты.
Порфирины в кале — копропорфирины и протопорфирины. Часть порфиринов в организме экзогенного происхождения (поступают с пищей в составе мясных продуктов, овощей, фруктов). В печени они превращаются в копропорфирины и выделяются с желчью.
Лабораторная диагностика нарушений порфиринового обмена
Исследование порфиринов в биологическом материале представляет определенные трудности в связи с небольшим содержанием, наличием различных типов и изомеров (различное расположение радикалов), определение которых требует специфических методов. Принцип — соединения, имеющие кольцо порфирина, флуоресцируют и характеризуются интенсивным поглощением на границе видимой и ультрафиолетовой областей спектра. Восстановленные формы порфиринов (порфириногены) бесцветны.
v Определение уровня порфиринов в моче
v Определение содержания порфобилиногена в моче
v Определение ДАЛК в моче
v Определение протопорфирина в эритроцитах
Определение уровня порфиринов в моче
1. Качественные – основаны на способности порфиринов в УФ давать красную флуоресценцию. В норме с мочой выделяется 0-2 мг/л (вне чувствительности метода).
2. Количественные — унифицированный метод Соулсби — основан на спектрофотометрии. Производят экстракцию порфиринов из мочи, а затем измерение оптической плотности на 3 длинах волн – 380, 402, 430нм → пересчет по креатинину.
Норма – 30,5-122 н/моль/г креатинина.
Показания: заболевания печени, Порфирии.
Определение содержания порфобилиногена в моче
Материал: свежевыделенная моча (хранение не более 2 часов при комнатной температуре) или в холодильнике при 4 0 С или -20 0 С.
Используется качественная реакция с реактивом Эрлиха (парадиметилбензальдегид в концетрированной соляной кислоте) +бутанол. Смешивают, встряхивают, отстаивают. Происходит разделения на 2 слоя. Верхний – бутанол. Внизу – водная фаза. У здоровых – окрашен бутанольный слой, у больных – водный.
Не нашли то, что искали? Воспользуйтесь поиском:
Лучшие изречения: Только сон приблежает студента к концу лекции. А чужой храп его отдаляет. 8740 — 

195.133.146.119 © studopedia.ru Не является автором материалов, которые размещены. Но предоставляет возможность бесплатного использования. Есть нарушение авторского права? Напишите нам | Обратная связь.
Отключите adBlock!
и обновите страницу (F5)
очень нужно
источник
Вид анализа, подлежащий приборному оснащению. Определение содержания копропорфиринов в моче. Критерии для выбора анализатора. Метод измерения и первичный преобразователь. Автоматизация процесса измерения флуоресценции раствора копропорфиринов.
Студенты, аспиранты, молодые ученые, использующие базу знаний в своей учебе и работе, будут вам очень благодарны.
Размещено на http://www.allbest.ru/
Санкт-Петербургский государственный электротехнический университет
«ЛЭТИ» им. В.И. Ульянова (Ленина)
по дисциплине «Медицинские приборы, аппараты, системы и комплексы»
Тема: Определение содержания копропорфиринов в моче
Студент гр. 2081 Глушенко И.В.
Преподаватель Садыкова Е.В.
1. ВИД АНАЛИЗА, ПОДЛЕЖАЩИЙ ПРИБОРНОМУ ОСНАЩЕНИЮ
3. СТРУКТУРНАЯ СХЕМА РАЗРАБОТАННОЙ СИСТЕМЫ С ПОЗИЦИИ БТСЛА
4. КРИТЕРИИ ДЛЯ ВЫБОРА АНАЛИЗАТОРА
5. МЕТОД ИЗМЕРЕНИЯ И ПЕРВИЧНЫЙ ПРЕОБРАЗОВАТЕЛЬ
6. ЦЕПЬ ВТОРИЧНЫХ ПРЕОБРАЗОВАТЕЛЕЙ
7. РЕГИСТРАЦИЯ, ОТОБРАЖЕНИЕ И ИСПОЛЬЗОВАНИЕ ИНФОРМАЦИИ
8. ПУТИ АВТОМАТИЗАЦИИ ПРОЦЕССА АНАЛИЗА
10. СПОСОБ ПОВЕРКИ АНАЛИЗАТОРА
СПИСОК ИСПОЛЬЗОВАННЫХ ИСТОЧНИКОВ
Порфирины представляют собой циклические соединения, образованные четырьмя пиррольными кольцами, связанными между собой метенильными мостиками [3].
Встречающиеся в природе порфирины являются соединениями, у которых восемь атомов водорода порфиринового ядра замещены боковыми группами, строение и относительное расположение которых, определяют отличие порфиринов друг от друга рис. 1.1 [5].
Рис. 1.1 Молекулярная структура некоторых порфиринов
Изомеров копропорфиринов типа III больше чем типа I так, как биологически важные порфирины, гемоглобин, миоглобин и т.д., являются изомерами типа III.
Самый большой клинический интерес из всех порфиринов представляют копропорфирины и уропорфирины, так как при порфириях наблюдается значительное увеличение экскреции этих соединений. Экскреция копропорфирина также увеличивается при лейкозах, анемиях, заболеваниях печени, ожогах, инфекционных заболеваниях, выраженном дефиците железа, при отравлениях мышьяком, этанолом, свинцом.
Копропорфирины растворимы в смеси эфира и ледяной уксусной кислоты. Уропорфирины в этой смеси нерастворимы, но частично растворимы в этилацетате. Полученные растворы при облучении УФ дают характерное красное флуоресцентное свечение. Эти свойства копропорфиринов можно использовать для количественного определения содержания их в моче.
Максимум поглощения всех порфиринов находится около 400нм. Спектр флуоресценции сильно зависит от величины pH раствора. При pH?6 один из максимумов интенсивности флуоресценции копропорфирина III приходится на 690нм.
1. ВИД АНАЛИЗА, ПОДЛЕЖАЩИЙ ПРИБОРНОМУ ОСНАЩЕНИЮ
моча анализатор флуоресценция копропорфирин
Определение содержания копропорфиринов в моче.
Для измерения флуоресценции раствора копропорфиринов.
Область применения анализатора.
Применяется для определения концентрации компонентов биологических жидкостей и клеток, основанный на измерении интенсивности флуоресцентного излучения при оптическом воздействии на жидкую биологическую пробу с последующей обработкой результатов [1].
Биологическая. Моча человека.
Материалы и реактивы необходимые для определения содержания копропорфиринов в моче представлены в таблице 2.1.
Таблица 2.1 Перечень используемых материалов и реактивов при проведении анализа
источник
Комплексный количественный анализ, позволяющий определить в моче уровень уро- и копропорфиринов: уропорфирин, гептакарбоксипорфирин, гексакарбоксипорфирин, пентакарбоксипорфирин, копропорфирин I, копропорфирин III, общий порфирин. Исследование предназначено для диагностики как врождённых, так и приобретенных порфирий. В основе генетически обусловленной порфирии лежит нарушение биосинтеза гема, приводящее к избыточному накоплению в организме порфиринов и их предшественников. Вторичные порфирии возникают вследствие нарушения функций печени или кроветворных органов как результат воздействия тяжелых металлов, интоксикаций свинцом, фосфором, алкоголем, бензолом, четыреххлористым углеродом, при некоторых злокачественных опухолях и аллергических состояниях, циррозах печени и проч.
Высокоэффективная жидкостная хроматография-масс-спектрометрия (ВЭЖХ-МС).
Нмоль/сут. (наномоль в сутки), мкмоль/сут. (микромоль в сутки).
Какой биоматериал можно использовать для исследования?
Как правильно подготовиться к исследованию?
- Исключить из рациона алкоголь в течение 24 часов до исследования.
- Исключить (по согласованию с врачом) прием мочегонных препаратов в течение 48 часов до сбора мочи.
Общая информация об исследовании
Порфирины — циклические соединения, образованные четырьмя пиррольными кольцами, связанными между собой метенильными мостиками, синтезируются из глицина и сукцинил-CoA через образование δ-аминолевулиновой кислоты и порфобилиногена. Это промежуточные соединения в синтезе гема, являющегося частью молекулы гемоглобина, осуществляющей перенос кислорода. При нарушении синтеза гема концентрация порфиринов в моче увеличивается.
Порфирины представляют собой оранжево-красные флюоресцирующие соединения, состоящие из 4 колец пиррола, которые образуются в процессе биосинтеза гема. Они обнаруживаются во всех клетках, принимают участие в энергетическом обмене, и экскретируются с мочой в небольших количествах. Повышение в моче уровня порфиринов или порфириногенов свидетельствует о нарушении биосинтеза гема, которое бывает врождённым, например при наследственных ферментопатиях, и приобретенным, например при заболеваниях печени и гемолитической анемии.
Принято различать первичные и вторичные порфинурии. К первым, обычно называемым порфириями, относят группу наследственных заболеваний, для каждого из которых характерен набор экскретируемых с мочой порфиринов и их предшественников. Вторичные порфинурии возникают вследствие нарушения функций печени или кроветворных органов в результате каких-либо первичных заболеваний, например тяжелых гепатитов, интоксикаций свинцом, фосфором, алкоголем, бензолом, четыреххлористым углеродом, при некоторых злокачественных опухолях и аллергических состояниях, циррозах печени и т. п. При вторичных порфинуриях в моче обнаруживаются значительные количества копропорфиринов.
Измеряются семь показателей порфиринов, включая общий порфирин, что позволяет идентифицировать токсический эффект металлов и увидеть, какое лечение необходимо. Также показатели конкретных порфиринов служат функциональными маркерами токсичности ядовитых металлов и органических химических веществ. С помощью порфириновых тестов можно определить уровень биохимического повреждения, вызванного воздействием токсических веществ, ртутное воздействие у пациентов, уровень токсинов у пациентов до и во время хелатирования, токсичность лекарственных препаратов, провести дифференциальную диагностику при отравлениях тяжелыми металлами.
Действие токсинов может вызвать повышенную чувствительность к химическим веществам, поведенческие расстройства и снижение обучаемости, иммунную дисфункцию, синдром хронической усталости, неврологические и психические, эмоциональные расстройства, анемии.
Также целесообразно при определении токсичности исследовать спектр заболеваний, связанных с аутизмом (ASD), и проводить разработку лечебных мероприятий по устранению недостаточной детоксикации и сульфатации, накопления тяжелых металлов. Источниками токсинов могут быть рыба, амальгамы, загрязненный воздух и почва, флуоресцентные лампы, краски, керамика, лечение с помощью методов народной медицины, грунтовые воды, табак. Симптомы интоксикации: усталость, слабость, повышенная химическая чувствительность, раздражительность, беспокойство, потеря памяти, бессонница, онемение и покалывание в руках и ногах, судороги, желудочно-кишечные расстройства, потеря аппетита.
Когда назначается исследование?
- Диагностика первичных (наследственных) порфирий;
- при подозрении на интоксикацию свинцом или ртутью, органическими растворителями, лекарственными препаратами (противосудорожные, анальгетики, анестетики, антипсихотики, противовоспалительные и гормональные), а также алкоголем и его суррогатами;
- болезни гепатобилиарной системы, сопровождающиеся порфиринуриями;
- гормональные изменения у женщин на фоне менструального цикла с обильными выделениями;
- анорексия на фоне низкокалорийной, низкоуглеводной диеты;
- острые атаки в анамнезе, одновременно сочетающие в себе острую боль в животе без симптомов раздражения брюшины с выделением красной или розовой мочи, появлением нарушений сердечного ритма, тошноты и рвоты, повышением артериального давления, повышением температуры тела на фоне различных проявлений полиневропатии.
источник
Комплексное определение порфиринов (7 параметров)
Перечень тестов в составе исследования:
- гексакарбоксипорфирин;
- гептакарбоксипорфирин;
- копропорфирин I;
- копропорфирин III;
- пентакарбоксипорфирин;
- уропорфирин;
- общий порфирин.
Порфирины мочи
Порфирины мочи — промежуточные соединения в синтезе гема, являющегося частью молекулы гемоглобина, которая осуществляет транспортировку кислорода. При нарушении синтеза гема концентрация порфиринов в моче увеличивается.
Порфирины представляют собой оранжево-красные флюоресцирующие соединения, состоящие из 4 колец пиррола, которые образуются в процессе биосинтеза гема. Они обнаруживаются во всех клетках, принимают участие в энергетическом обмене и экскретируются с мочой в небольших количествах. Повышение в моче уровня порфиринов или порфириногенов свидетельствует о нарушении биосинтеза гема, которое бывает врожденным, например, при наследственных ферментопатиях, и приобретенным, например, при заболеваниях печени и гемолитической анемии.
Определение в моче уровня отдельных порфиринов или порфириногенов позволяет выявить недостаточность отдельных ферментов, участвующих в биосинтезе гема. В некоторых случаях количественному анализу предшествует проведение качественных скрининговых тестов (для этого используют произвольно взятую пробу мочи). В случае положительных результатов исследуют суточную мочу.
Сопоставление уровней порфиринов в моче, плазме крови и кале повышает достоверность диагностики порфирий.
Порфириновые болезни
Порфирии (болезни порфириновые) — наследственные или приобретённые (как результат воздействия химических агентов) дефекты ферментов, участвующих в биосинтезе гема.
Порфирии классифицируют в зависимости от первичной локализации нарушения синтеза порфиринов:
- эритропоэтическая порфирия обусловлена нарушением синтеза порфиринов эритробластами костного мозга и проявляется главным образом кожной фотосенсибилизацией (вследствие активации УФО повышенного отложения порфиринов в коже);
- печёночная порфирия обусловлена нарушением синтеза порфиринов в печени и проявляется главным образом острыми неврологическими нарушениями (приступы артериальной гипертензии, колики в животе, психозы и невропатии) без кожной фотосенсибилизации. Во время приступа в плазме и моче повышается концентрация предшественников порфирина — дельта-аминолевулиновой кислоты и порфобилиногена.
Показания:
- анемия;
- гепатиты;
- отравления свинцом.
Подготовка
Накануне сдачи анализа не рекомендуется употреблять в пищу овощи и фрукты, которые могут изменить цвет мочи (свёкла, морковь, клюква и т.п.), принимать диуретики.
Утром опорожнить мочевой пузырь (эта порция мочи выливается в унитаз). Зафиксировать время мочеиспускания, например: «8:00».
Следующие 24 часа собрать всю выделенную мочу в сухую чистую ёмкость вместимостью 2–3 литра.
После завершения сбора мочи, содержимое ёмкости нужно точно измерить. На контейнере нужно указать суточный объём мочи (диурез) в миллилитрах. Например: «Диурез: 1250 мл».
Мочу обязательно тщательно перемешать и сразу же отлить 50–60 мл в стерильный контейнер с крышкой. Всю мочу, собранную за сутки, приносить не надо.
В течение всего времени сбора и до отправки, биоматериал должен храниться в холодильнике при 2–8°С. Материал должен быть доставлен в медицинский офис в день окончания сбора.
Женщинам не рекомендуется сдавать анализ мочи во время менструации.
Интерпретация результатов
В норме экскреция уропорфиринов с мочой составляет от 27 до 52 мкг/ сут (СИ: 32–63 нмоль/сут), а копропорфиринов — от 34 до 230 мкг/сут (СИ: 52–351 нмоль/сут).
Повышение в моче содержания порфиринов и их предшественников — характерный признак порфирий. Кроме того, экскреция порфиринов может возрастать при вирусном гепатите, лимфогранулематозе, поражении ЦНС, циррозе печени, а также отравлениях солями тяжёлых металлов, бензолом и четыреххлористым углеродом.
Факторы, повышающие результат:
- применение барбитуратов, хлоралгидрата, хлорпропамида, сульфаниламидов, мепробамата, хлордиазепоксида — индуцирует порфирию или порфиринурию; от приема этих препаратов следует по возможности отказаться за 12 дней до проведения исследования;
- прием пероральных контрацептивов, гризеофульвина (экскреция порфиринов с мочой увеличивается);
- беременность или менструация (возможно повышение или снижение содержания порфиринов в моче);
- применение рифампицина повышает содержание уробилиногена в моче;
- нарушение биосинтеза гема на разных этапах способствует повышению в моче содержания порфиринов и их предшественников и развитию порфирий.
источник
Порфирины — циклические соединения, образованные четырьмя пиррольными кольцами, связанными между собой метенильными мостиками, синтезируются из глицина и сукцинил-CoA через образование δ-аминолевулиновой кислоты и порфобилиногена.
Порфирины способны образовывать комплексы с ионами металлов, связывающихся с атомами азота пиррольных колец. Примерами служат железопорфирины, в частности гем, входящий в состав гемоглобина, и магнийсодержащий порфирин — хлорофилл — пигмент растений, участвующий в фотосинтезе.
Превращение порфобилиногена в порфирин может происходить просто при нагревании в кислой среде (например, в кислой моче), в тканях это превращение катализируется специфическими ферментами. Все порфириногены бесцветны, тогда как все порфирины окрашены.
Копропорфирины I и III растворимы в смесях эфира и ледяной уксусной кислоты, из которых их можно экстрагировать соляной кислотой. Уропорфирины, напротив, в этих смесях нерастворимы, но частично растворимы в этилацетате, и их также можно экстрагировать соляной кислотой. Полученные солянокислые растворы при облучении ультрафиолетовым светом дают красное флюоресцентное окрашивание. Характерные полосы поглощения могут быть зарегистрированы с помощью спектрофотометра.
Последовательно образующиеся в процессе синтеза гема из δ-аминолевулиновой кислоты интермедиаты становятся все более гидрофобными. Это повышение гидрофобности отражается на распределении интермедиатов синтеза гема в составе мочи и кала. Более полярный уропорфири-ноген экскретируется преимущественно с мочой, а более гидрофобные копропорфириноген и протопорфириноген оказываются преимущественно в желчи и удаляются с калом.
Принцип метода . При реакции порфобилиногена с пара-диметиламинобензальдегидом образуется соединение красного цвета. Повышение специфичности реакции достигается добавлением ацетата натрия. Уробилиноген, производные индола, скатола и другие соединения, дающие аналогичную реакцию с пара-диметиламинобензальдегидом, удаляют экстракцией бутанолом и хлороформом, в которых порфобилиноген нерастворим.
Реактивы . 1) пара-диметиламинобензальдегид; 2) концентрированная соляная кислота; 3) реактив Эрлиха: 0,7 г пара-диметиламинобензальдегида растворяют в 150 мл концентрированной соляной кислоты, приливают 100 мл дистиллированной воды и смешивают. Раствор должен быть бесцветным или слегка желтым. Хранят в посуде из темного стекла, стабилен; 4) насыщенный раствор ацетата натрия: 375 г CH3COONa × ЗН2O или 226 г CH3COONa растворяют в 250 мл теплой дистиллированной воды. Раствор должен быть бесцветным и прозрачным, хранят его при температуре 20 °С; 5) хлороформ; 6) бутиловый спирт; 7) индикаторная бумага для измерения pH в интервале 4,0–5,0.
Постановка пробы . Исследуют мочу в первые 2–3 ч после мочеиспускания. В пробирке смешивают по 2,5 мл мочи и реактива Эрлиха, добавляют 5 мл насыщенного раствора CH3COONa, перемешивают. Измеряют pH, который должен быть в пределах 4,0–5,0. При pH меньше 4,0 пробу подщелачивают раствором ацетата натрия.
Оценка результатов . При отсутствии развития окраски результат считается отрицательным. Если проба окрашивается в розовый или красный цвет, в пробирку добавляют 5 мл хлороформа и встряхивают. Окрашивание хлороформа при бесцветном или слегка желтоватом верхнем слое также позволяет считать пробу отрицательной. Если окрашенным остается слой над хлороформом, то 6–8 мл из него переносят в другую пробирку, добавляют бутанол в соотношении 1 : 2 и встряхивают. При плохом разделении слоев жидкостей пробу центрифугируют. Окрашивание бутанола свидетельствует о низком содержании порфобилиногена — проба также отрицательна. Если окрашенным остается исследуемый слой, то в моче концентрация порфобилиногена выше нормальной. В норме концентрация порфобилиногена в моче — до 2 мг/л. Данным методом порфобилиноген определяется при концентрации более 6 мг/л.
Примечание : при хранении мочи более 3 ч при комнатной температуре положительная реакция может стать отрицательной, что связано с превращением порфобилиногена в порфирин в кислой среде и образованием ингибиторов реакций. При невозможности исследования мочи в первые 2 ч хранить ее необходимо в холодильнике при 4‘°С, доведя pH до 6,0–7,0. В этих условиях порфобилиноген стабилен в течение длительного времени.
Принято различать первичные и вторичные порфинурии. К первым, обычно называемым порфириями, относят группу наследственных заболеваний, для каждого из которых характерен набор экскретируемых с мочой порфиринов и их предшественников. Вторичные порфинурии возникают вследствие нарушения функций печени или кроветворных органов в результате каких-либо первичных заболеваний, например тяжелых гепатитов, интоксикаций свинцом, фосфором, алкоголем, бензолом, четыреххлористым углеродом, некоторых злокачественных опухолях и аллергических состояниях, циррозах печени и т. п. При вторичных порфинуриях в моче обнаруживаются значительные количества копропорфиринов.
У здоровых людей с мочой за сутки в норме выводится в среднем около 67 мкг копропорфиринов; на изомер I типа приходится в среднем 14 мкг/сут, на изомер III типа — 53 мкг/сут. Отклонения в этом соотношении могут служить диагностическим признаком при некоторых заболеваниях печени.
источник
Порфирины — это природные химические вещества, которые содержатся в вашем организме. Они являются важной частью многих функций вашего организма.
Обычно ваше тело образует небольшое количество порфиринов, когда он производит гем. Хеме — важный компонент гемоглобина, белка в эритроцитах, который переносит кислород. Производство Heme включает в себя многоступенчатый процесс, и каждый шаг контролирует другой фермент. Если один из этих ферментов неисправен, это может привести к образованию порфиринов в вашем теле и потенциально достигать токсичных уровней. Это вызывает клиническую болезнь порфирии.
Порфирия редка. Большинство типов порфирии передаются человеку через их гены. Если ваш врач подозревает, что у вас есть тип порфирии, они захотят сделать некоторые тесты, чтобы установить уровень порфиринов в вашем теле. Один из способов проверить это — проверить мочу.
Один тип исследования мочи порфирина — это случайный образец с одной мочой, или они могут попросить вас пройти тест на мочу в течение 24-часового периода. Производство и устранение порфиринов может варьироваться в течение дня и между атаками, поэтому случайный образец может пропустить повышенные уровни порфирина. 24-часовой анализ мочи является безболезненным и требует простой сбор мочи, выполненной в три этапа.
Порфирии могут быть сгруппированы в два основных типа: неврологические порфирии и кожные порфирии.
Неврологические порфирии влияют на вашу нервную систему. Они также известны как острые порфирии, потому что они внезапно появляются и вызывают серьезные симптомы на короткое время.
Кожные порфирии приводят к чувствительности к солнцу, что приводит к проблемам кожи, таким как волдыри или зуд.
Врачи могут использовать контроль мочи порфиринов как часть их диагноза следующих типов неврологических порфирий:
- острая прерывистая порфирия
- variegate porphyria
- наследственная копопорфирия
- Порфирия дефицита дегидратазы ALA
Они могут также используйте его, если они подозревают, что у вас есть порфирия cutanea tarda, тип кожной порфирии.
Родители младенцев, принимающих мочу, могут захотеть приобрести дополнительные сумки для сбора, если активный ребенок вытеснит мешок.
Если вы взрослый, принимающий тест, ваш врач может дать вам указание прекратить принимать наркотики, которые могут помешать точности анализа мочи порфиринов. Обязательно следуйте указаниям и инструкциям вашего врача при остановке лекарств.
Следующие препараты могут мешать точному измерению порфиринов в моче:
- алкоголь
- аминосалициловая кислота, аспирин (Bayer Advanced Aspirin, Bufferin)
- барбитураты
- таблетки для борьбы с рождаемостью
- chloral гидрат
- хлорпропамид
- griseofulvin (Gris-PEG)
- морфин
- phenazopyridine (Pyridium, Uristat)
- procaine
- сульфонамиды
РекламаРеклама
Вот как работает процедура сбора для 24-часового исследования мочи:
- В первый день вы мочитесь в туалет при повышении утром.Промойте этот первый образец.
- В течение оставшейся части дня вы собираете всю свою мочу в специальном контейнере и храните ее в прохладном месте.
- Во второй день вы мочитесь в специальный контейнер, поднимаясь утром.
- После этого вы вернете контейнер в лабораторию как можно скорее.
Реклама
Если вы являетесь родителем ребенка, принимающего тест на мочу, вам необходимо выполнить следующую процедуру:
- В день один, вымойте область вокруг уретры вашего ребенка, затем приложите сумку для сбора в эту область. Для мальчика вы кладете сумку поверх пениса. Для девушки поместите сумку поверх ее половых губ. Затем вы можете положить подгузник вашего ребенка поверх сумки.
- В течение оставшейся части 24-часового периода собирайте образцы в соответствии с тем же графиком, что и взрослые.
- В течение дня проверяйте сумку. Измените сумку каждый раз, когда ваш ребенок мочится.
- Каждый раз, когда ваш ребенок мочится, вылейте образец в контейнер для сбора. Храните этот контейнер в прохладном месте.
- На второй день собирайте окончательный образец, когда ваш ребенок сначала просыпается.
- Верните контейнер в лабораторию как можно скорее.
РекламаРеклама
Нормальный диапазон для 24-часового теста мочи порфиринов составляет около 50-300 миллиграммов, хотя результаты варьируются в разных лабораториях.
Аномальные результаты теста могут указывать на рак печени, гепатит, отравление свинцом или одну из различных форм порфирии. Ваш врач сможет интерпретировать результаты для диагностики и рекомендовать лучший курс лечения.
источник
Порфирины (от греч означ пурпурный, багряный) – циклические органич соед-я, в основе ктр лежит кольцо порфирина, сост-ее из 4 пирролов, соед-ых метиновыми мостиками (=СН-). Каждый из порфинов представляет собой порфин, у ктр водородные атомы, связанные с С1-С8-углеродами колец пиррола замещены боковыми цепями: метиловыми(СН3), этиловыми, виниловыми (СН=СН2),остатками уксусной(-СН2-СООН),пропионовой(-СН2_СН2-СООН) кислот в зависимости от природы боковых цепей и их расположения в кольце порфина образуются разные изомеры порфирина (уро-,копро- и др). амфотерные соед-ия, облад-ие как кислотными так и основными св-вами. Не раствор-ся в воде, но хорошо раствор-ся в хлороформе, эфире и других органич соед-ях.связаны с клеточным дыханием. В свободных формах не встреч-ся. Гемопротеины:П.+белок+железо – гемоглобин, ткан дыхат ферменты: каталаза, пероксидаза, цитохромы. Выделяются с мочой и калом. Источником П. мочи у Здор людей явл-ся П. печени и (частично) эритронормобластовП. мочи этокопропорфирин, в небольшом количествесод-ся уропорфирины, а также предшественники порфиринов: порфобилиноген и ДАЛК. В кале – копропорфирины и протопорфирины. Часть экзогенного происхождения – они поступают с пищей.
Нарушения в обмене П. возникают при их повышенном синтезе, нарушении выведения из организма, а также при недостаточной активности ферментов синтеза гемма.
В начальной и на поздней стадиях этот процесс совершенствуется только в митохондриях, с участием многих ферментов и ряд процессов активен только в ядросодержащих эритроцитах. В норме основн кол-во синт-ся в костн мозге (образ гемоглобина) и печени (для образов железосодержащих ферментов митохондриальной цепи – цитохромов, каталазы, пероксидазы и др).
Порфирины — это амфотерные соединения, обладающие как кислотными, так и основными свойствами. Они не растворяются в воде, но хорошо растворяются в хлороформе, эфире и других органических соединениях, эти вещества отличаются устойчивостью к воздействию высоких температур, разлагаются при 360С. Порфирины способны избирательно поглощать свет при 400 нм, обладают способностью флюоресцировать ярко-зеленым свечением, спектр флюоресценции зависит от рН среды, это свойство порфиринов используется при их дифференцировке. В организме человека порфирины связаны с основным жизненным процессом — клеточным дыханием. Свободные порфирины почти не встречаются, соединения порфиринов представлены комплексами с белками и металлами (кобальт, магний, железо). Комплексы порфиринов с железом и белками называются гемопорфиринами (гемоглобин крови, тканевые дыхательные ферменты: каталаза, пероксидаза, цитохромы), функция которых связана с обменом кислорода.
Порфирины содержатся во всех клетках организма человека, где осуществляется клеточное дыхание, в том числе в клетках ЦНС. В наибольшем объеме их образование происходит в эритронормобластах костного мозга и гепатоцитах, где они используются для биосинтеза гемма. Для образования 6 г гемоглобина организм синтезирует 500 мг протопорфиринов. Основная часть синтезируемых порфиринов эритробластов идет на образование гемоглобина, а неиспользованные порфирины и их предшественники выделяются с мочой и калодм. Порфирины мочи и кала образуются из разных источников. Источником порфиринов мочи у здоровых людей являются порфирины печени и (частично) эритронормобластов. Основная часть порфиринов мочи представлена копропорфиринами, в небольшом количестве содержатся уропорфирины, а также предшественники порфиринов: порфобилиноген и дельта-аминолевулиновая кислота. В кале содержатся копропорфирины и выделяются с желчью. Небольшое количество порфиринов, неиспользованных при синтезе гемма, обнаруживается в эр здоровых людей, в их числе: протопорфирины, копропорфириногены, уропорфириногены. Их количество служит показателем синтеза порфиринов и степени их использования для построения гемма. Эти процессы тесно связаны с количеством железа в организме и активностью соответсвующих ферментов.
Нарушения в обмене порфиринов возникают при их повышенном синтезе, нарушении выведения из организма, а также при недостаточной активности ферментов синтеза гемма. Заболевания, связанные с нарушением обмена порфиринов, подразделяются на две группы: порфирии и порфиринурии.
Первичные порфирии делятся на эритропоэтические (эритропоэтическая уропорфирия, или болезнь Гюнтера, эритропоэтическая копропорфирия) и печеночные (острая перемежающаяся порфирия, наследственная печеночная копропорфирия, урокопропорфирия, или поздняя кожная порфирия)
Болезнь Гюнтера обусловлена наследственным нарушением синтеза порфиринов в эр. Чаще выявляется у детей первых лет жизни и наследуется по рецессивному типу. Течение зб хроническое, с обострениями в весеннее-летний период, клинич картина характеризуется резко повышенной чувствительностью кожных покровов к солнечному свету, при этом появляется зуд, пузыри с нагноением, язвочки, а затем рубцы. В дальнейшем развивается остеопороз, искривляются фаланги пальцев, зубы приобретают коричневую окраску и при облучении УФ дают ярко-красное свечение.Выявляется анемия гемолитического типа, в крови увеличено количество ретикулоцитов, отмечается гипербилирубинемия. В моче, которая приобретает ярко-красную окраску, увеличивается количество уробилина и в большом количестве уропорфирина-1. Содержание копропорфирина-1 и уропорфирина-1 в эр возрастает в 100-200 раз по сравнению со здоровыми.
Отсутствие фермента гемсинтетазы. В результате содержание протопорфирина-9 увелич в 10-100 раз. Отмечается выраженная чувствительность кожи к свету, даже через оконное стекло. При инсоляции – отеки, гиперемия, образ пузыря, изм функция печени, вследствии развития порфиринового цирроза печени.
Острая перемежающаяся порфирия наследуется по доминантному типу. Отсутствие фермента ….-синтетазы, в результате повышается содержание в органах и тканях крови порфобилиногена и ДАЛК. Течение хронич, с периодами обострения и ремиссии. Зб чаще проявляется в возрасте 20-30 лет, провоцирующими факторами является прием сульфаниламидов, анальгина, барбитуратов, валокордина, беременность и др. Характерным клиническим симптомом явл острые боли в животе, протекающие под маской острого живота. Могут отмечаться псих расстройства, судорожный синдром и даже слепота. Лабораторно в моче увеличено содержание предшественников порфиринов: гамма-аминолвулиновой кислоты, порфобилиногена. Эти соединения бесцветны, поэтому моча больных нормально окрашена. Накопление гамма-аминолевуленовой кислоты в нервных клетках вызывает токсических эффект. Лечение – глюкоза.
Печеночная урокопропорфирия – у женщин старше 40 лет. Характерна большая чувствительность кожи к механическим травмам, воздействию света. Наблюдается истощение кожных покровов, гипертрихоз, могут быть кисты в складках кожи пальцев рук.
Острая перемежающаяся порфирия – насл заб-ие перед по аут-дом типу. Понижение активности УП-1-синтетазы и повышен акт-ти синтетезы ДАЛК, вследствии чего увелич-ся образование и выделение с мочой порфобилиногена и ДАЛК. Эритр не изменены. Моча – ПБГ и ДАЛК значит увелич, не окрашена, розовато-красное окрашивание появляется при значительном увеличении УПГ 3. Кал – КПГ 3, ПП 9 незначительно увеличены. Лечение – глюкоза
Урокопропорфирия (поздняя кожная порфирия)– появл после 40 лет,повышен чувс-ть к легкой механич травме и солн облучению, пигментация кожи, нарушен функции печени, проявляется при опухолях печени. Эритроциты – без изменений. Моча – ДАЛК и ПБГ в пределах нормы, резко увел кол-во УПГ3, незначительно КПГ3, красного цвета. Лечение – делагил.
Порфиринурии – повышен выведен порфиринов из организма. Набл при заб-иях крови (анемия гемолитическая (эритроциты – ПП 9, КПГ3 значит увел, моча – ДАЛК и КПГ3 значит увел, кал – ПП9 увеличен,КПГ3 значит увеличен), лейкоз), острый гепатит, энтерит, аллерг анафил лихор состояниях, авитаминозах (эрит – ПП 9 увеличен, моча – ДАЛК увел, КПГ 3 знач увел), отравлении свинцом, оловом, ртутью, хлором, бензолом(эритр – ПП9 и КПГ3 значит увелич, моча – ДАЛК и КПГ 3 значит увеличены, кал – ПП9 увел, КПГ3 значит увеличен).
Вторичные нарушения обмена порфиринов.
Порфиринурии встрчаются как симптом при многих зб: гипохромные анемии, обусловленные длительными инф (туберкулез, остеомиелит, пиодермии), гемолитические анемии, зб печени (хр гепатиты, циррозы, опухоли), лечении цитостатиками. Наиболее значительные изменения в обмене порфиринов выявляются при сидероахристических анемиях, при которых количество железа в эритробластах достаточное, однако оно не используется для синтеза гемма гемоглобина ввиду отсутствия или снижения активности фермента гемсинтетезы. Сидероахристические анемии могут быть как наследственными, так и приобретенными, связанными с отравлением свинцом или дефицитом витамина В6, который катализирует первые этапы синтеза гемма и освобождение железа из митохондрий. При таких формах порфиринурий содержание протопорфиринов в эритроцитах понижено, а копро- и уропорфиринов – повышено.
Нарушения порфиринового обмена при токсических порфириях наблюдается при воздействии таких ядов, как свинец, ртуть, марганец, хром, фтор, висмут, селен, бензол, хлороформ, амидо- и нитросоединения, окись углерода, бензин, фосфор и др. Наиболее изучены нарушения обмена порфиринов при интоксикации свинцом. Отравление свинцом встречаются на производстве при изготовлении красок, аккумуляторов, в типографиях, в рентгенкабинетах, при использовании глиняной посуды, покрытой свинцовой глазурью. Свинец – тяжелый метал, способный блокировать сульфгидрильный группы многих ферментов синтеза гемма и тем самым нарушать его образование. При этом в эр накапливаются свободные порфирины: копро- и протопорфирины. В моче больных отмечается большое количество копропорфирина 111, значительно увеличивается содержание аминолевуленовой кислоты.
Полуколичественный метод определения копропорфиринов по Резнику и Федорову.
В пробирки вносят 5 мл мочи + неск капель ледяной уксусной кисоты (до кислой реакции по лакмусовой бумажке) и 5 мл диэтилового (медицинского) эфира, смесь встряхивают в течении 3-5 мин. Оставляют для отстаивания и разделения слоев. Отбирают верхрний слой в др пробирку и помещают ее в поток УФ света, реакцию оценивают по характеру свечения (флюоресценции): норм содержание копропорфиринов – голубое свечение, слабое повышение –слабое розовое свечение, повышенное содержание – слабое красное свечение, значительное повышение – отчетливое красное.
Папиллярные узоры пальцев рук — маркер спортивных способностей: дерматоглифические признаки формируются на 3-5 месяце беременности, не изменяются в течение жизни.
источник
Копропорфирины легко экстрагируются этил-ацетатом или эфиром из водного раствора при рН 4 ( изоэлектрическая точка порфиринов); уропорфирины остаются при этом в водной фазе. Количество порфирина в каждой фазе может быть определено колориметрически. [1]
При выделении, например, копропорфирина из мочи больных порфиринурией поступают следующим образом. [2]
Определение основано на специфическом красном флуоресцентном свечении гематопорфирина ( копропорфирина ) при его облучении ультрафиолетовым светом. [3]
В этой; же работе удалось решить и значительно более трудную задачу — разделить копропорфирины III и IV. Метиловые эфирьс этих соединений хромато-графировали на сорбенте ц-порасил в системе эфир — н-гептан ( 2: 3), содержащей воду в количестве 90 % от насыщения, причем для полного разделения изомеров потребовалось 10 циклов. [5]
Значительное структурное сходство многих природных порфиринов, таких, как уропорфирины I (11.6) и III (11.1) ил № копропорфирины I (11.7) и III (11.8), и близость значений рКа присутствующих в их молекулах карбоксильных групп обусловливают появление некоторых весьма специфических проблем, связанных с хроматографическим разделением этих соединений. Наилучшего отделения карбоксилсодержащих порфиринов от других водорастворимых метаболитов легче всего добиться путем этерификации этих соединений, в результате которой они приобретают липофильные свойства и могут быть выделены. Такой способ предварительного фракционирования порфиринов имеет немаловажное достоинство, заключающееся в том, что для сложных эфиров порфиринов уже разработано множество методов разделения и анализа ( разд. [6]
Ввиду неоснащенности лабораторий аппаратурой и отсутствия химреактивов практически все лечебно-профилактические учреждения как городов, так и районов, не проводят исследование функции печени, холинэстеразы, сыворотки крови, аминоле-вулиновой кислоты ( АЛК), копропорфирина в моче. [7]
Следовательно, мы определяли растворимый в эфире копропорфирин . [8]
Силикагель получил столь же широкое применение в хроматографии эфиров порфиринкарбоновых кислот, как и оксид алюминия, однако он обладает меньшей емкостью. Лукас и Ортен [120] хроматографировали метиловые эфиры уропорфирина I, копропорфирина I , мезопорфирина и протопорфирина на сили-кагеле в системах петролейный эфир — хлороформ. Для того чтобы добиться полного разделения смеси указанных соединений, нужно постепенно увеличивать концентрацию хлороформа в элюенте. С) — хлороформ ( 1: 5) ], исключив из нее аммиак. В действительности любые системы растворителей, пригодные для ТСХ на силикагеле, можно также использовать и для проведения колоночной хроматографии на этом сорбенте. [9]
ТСХ на целлюлозе [16-19] подчиняется тем же закономерностям, что и описанная выше бумажная хроматография. Эта методика была в дальнейшем усовершенствована Юаном и Расселом [18], предложившими использовать систему 2 6-лутидин — аммиак — вода — 0 1 М ЭДТА ( 500: 210: 140: 1), которая позволяет разделить копропорфирины I и III и отделить дейтеропорфирин от мезопорфирина. [10]
Классификация порфиринов исходит из типа заместителей его боковых цепей. Наиболее важными считаются следующие классы: этиопорфирины, которые имеют в качестве заместителей четыре метальные и четыре этильные группы; мезопорфирины с четырьмя метальными, двумя этильными и двумя карбоксивинильными группами; протопорфирины, содержащие четыре метальные, две винильные и две карбоксиэтильные группы, и копропорфирины с четырьмя метальными и четырьмя карбоксиэтильными группами. [11]
Изменения прочности и способности волос к растяжению; по данным Сузуки и др., у рабочих, подвергавшихся воздействию РЬ, содержание последнего в волосах колебалось от 3 9 до 618 8 мкг / г; причем была установлена зависимость между содержанием РЬ в волосах, моче, крови и копропорфирина в моче. [12]
Однако выделение порфиринов может резко возрасти ( в 10 — 12 раз) при заболеваниях печени и пернициозной анемии. В этих случаях в суточном количестве мочи обнаруживается до 10 мг смеси этих порфиринов. При острой порфирии отмечается экскреция с мочой повышенных количеств уропорфирина III, копропорфирина III , а также порфобилиногена. [13]
Классификация порфиринов исходит из типа этих боковых цепей. Наиболее важными считаются следующие классы: этиопорфирины, которые имеют в качестве заместителей четыре метальные и четыре этильные группы; мезо-порфирины с четырьмя метильными, двумя этильными и двумя карбокси-этильными группами; протопорфирины, содержащие четыре метальные, две винильные и две карбоксиэтильные группы, и копропорфирини с четырьмя метильными и четырьмя карбоксиэтильными группами. Порфирины, которые содержат одинаковое число заместителей двух разных типов, например этиопорфирины или копропорфирины , могут существовать в четырех изомерных формах в зависимости от расположения боковых цепей относительно порфиринового ядра. Соединения типа протопорфиринов, которые содержат три различных типа боковых цепей, могут существовать в пятнадцати изомерных формах. [14]
Как и в случае пирролов, растворимость каждого отдельного порфирина в водных или органических растворителях зависит от природы его заместителей. Карбоксильные группы способствуют растворимости в щелочных водных растворах. Например, уропорфирины, у которых в каждом из четырех пиррольных остатков имеется один остаток уксусной и один — пропионовой кислоты, растворимы в щелочах, но не растворимы в эфире; копропорфирины , у которых в каждом кольце имеется метильная группа и остаток пропионовой кислоты, растворимы в щелочах, а также в эфире; протопор-фирины, у которых в двух пиррольных кольцах присутствует по одной метильной и одной ви-нильной боковой цепи, а в двух других пиррольных кольцах — по одной метильной и по одной пропионовокислой боковой цепи, растворимы в пиридине или лутидине и в эфире, но с трудом растворяются в щелочных водных растворах. [15]
источник
Острые порфирии – группа редких наследственных метаболических заболеваний, обусловленных частичным дефицитом одного из ферментов цепи биосинтеза гема (см. рисунок) [3, 9]. К ним относят острую перемежающуюся порфирию (ОПП), вариегатную порфирию, наследственную копропорфирию и порфирию, обусловленную дефицитом дегидратазы аминолевулиновой кислоты (АЛК). Клинически острые порфирии проявляются атаками, сопровождающимися болью в животе, легкими аффективными нарушениям, тахикардией, артериальной гипертензией, запором и другими симптомами автономной дисфункции [3]. В случае несвоевременной диагностики и неправильного лечения также может развиваться острая полиневропатия и тяжелая энцефалопатия [13]. Причиной атак является активация биосинтеза гема, которая у пациентов с острыми порфириями приводит к накоплению токсичных предшественников порфиринов – порфобилиногена (ПБГ) и АЛК в печени (см. рисунок), откуда они попадают в кровоток, а затем разносятся к тканям и органам. Основными провоцирующими факторами атак обычно являются употребление определенных лекарств, алкоголя, низкокалорийная диета, колебания гормонального фона, т. е. все то, что стимулирует синтез гема [3].
Рис. 1. Биосинтез гема и порфирии.
Как терапевтические, так и неврологические проявления острой порфирии могут имитировать другие заболевания, затрудняя выявление острой порфирии [3]. К сожалению, проблеме острых порфирий уделяется недостаточно внимания, что приводит к отсутствию настороженности врачей в отношении этой патологии. А между тем неправильная диагностика этого потенциально курабельного состояния с большой долей вероятности может привести к инвалидизации больного или его смерти [13].
Несмотря на то что существует совершенно определенное условие диагностики острых порфирий: обязательное более чем 5-кратное повышение в моче уровня предшественника порфиринов – ПБГ – во время атаки [8], нередко у пациентов с незначительным повышением уровней порфиринов и их предшественников ошибочно устанавливают диагноз острой порфирии. Даже среди случаев, описанных в периодической научной литературе, имела место гипердиагностика острых порфирий [3, 4, 6, 16, 17]. Речь идет о случаях, имеющих клиническое сходство с острой порфирией, когда незначительное повышение уровня предшественников порфиринов – АЛК и ПБГ (менее чем в 3 раза) или повышение уровня порфиринов при нормальных значениях АЛК и ПБГ, трактовали как острую порфирию. Представленные наблюдения, по-видимому, можно отнести к порфиринурии, ассоциированной с неврологической симптоматикой. Следует отметить, что они вносят путаницу в представление о неврологических проявлениях порфирии.
Ряд заболеваний и состояний сопровождается транзиторным повышением уровня порфиринов, что обозначают термином «вторичная порфиринурия» [2]. Чаще всего вторичная порфиринурия обусловлена нарушением выведения порфиринов билиарной системой на фоне различной патологии печени в отличие от повышенного синтеза порфиринов и их предшественников при порфириях. В биохимическом профиле пациентов с вторичными порфиринуриями преобладает экскреция порфиринов [2] в отличие от превалирования АЛК и ПБГ при острых порфириях [8] (см. рисунок). При вторичных порфиринуриях как терапевтическая, так и неврологическая симптоматика вызвана другой причиной, которая не должна быть упущена, а кроме того, специфическая терапия порфирии у таких пациентов бессмысленна. Таким образом, перед тем, как установить диагноз наследственной острой порфирии, необходимо провести тщательное биохимическое исследование и получить доказательные значения уровня предшественников порфиринов [8].
Мы представляем наш опыт выявления 12 пациентов со вторичными порфиринуриями, у которых изначально устанавливали диагноз острой порфирии, и приводим принципы дифференциальной диагностики этих состояний.
В материалы статьи включены данные 12 пациентов, которые были госпитализированы в неврологические отделения стационаров Санкт-Петербурга в 1998–2011 гг. и у которых первоначально был ошибочно установлен диагноз «острой порфирии». Острая порфирия была заподозрена на основании клинических симптомов, включая острую/подострую полиневропатию и энцефалопатию в сочетании с выраженным болевым синдромом и/или автономной дисфункцией. Биохимически первоначальный диагноз острой порфирии основывался на выявлении повышенных уровней порфиринов и/или их предшественников (АЛК, ПБГ) во время острой фазы заболевания, однако не превышавших 5-кратный уровень верхней границы нормы. При выявлении пациента с подозрением на острую порфирию приглашали специалиста нервно-мышечного центра для проведения дальнейшей дифференциальной диагностики.
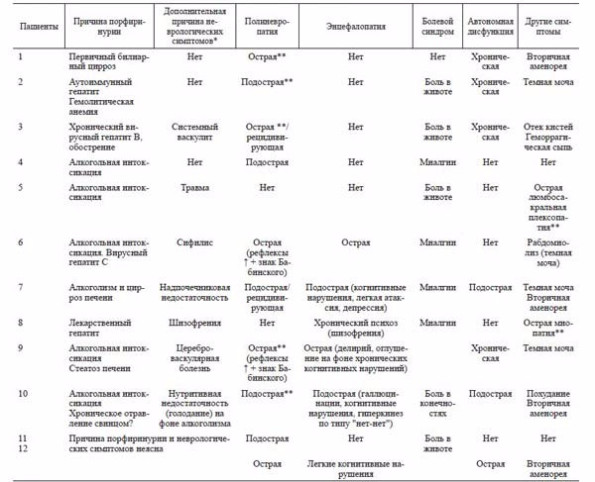
Из 12 пациентов было 6 мужчин и 6 женщин; средний возраст составил 41 год (20–56 лет; табл. 1). Десять пациентов изначально были госпитализированы в неврологические отделения в связи с преобладающей неврологической симптоматикой, 2 пациента поступили в отделение терапевтического профиля, и неврологическая симптоматика развилась у них уже во время госпитализации. У 6 пациентов имелось указание на употребление значительного количества алкоголя незадолго до развития симптоматики, при этом у 4 – на хроническое злоупотребление алкоголем. Ни у одного из пациентов не было указаний на подобные случаи заболеваний в семье. Одна из наблюдаемых (пациентка 10; см. табл. 1) в течение длительного времени работала на производстве хрусталя, где использовали свинецсодержащий припой.
В группу сравнения вошли 16 российских и 2 финских пациента с наследственной острой порфирией, диагностированной с помощью ДНК-анализа в 1996–2011 гг. У 17 больных диагностирована ОПП, у одной пациентки – наследственная копропорфирия. Клинически острая порфирия у этой группы больных была заподозрена во время тяжелой атаки, сопровождавшейся острой полиневропатией или энцефалопатией в сочетании с выраженным болевым синдромом и/или автономной дисфункцией, и верифицирована как биохимически, так и в дальнейшем молекулярно-генетически [8, 14].
Т а б л и ц а 1. Клинические симптомы и синдромы у пациентов с вторичной порфиринурией
П р и м е ч а н и е . * – факторы, вызывающие порфиринурию, во многих случаях также могут напрямую вызывать неврологические симптомы; ** – выполнена ЭНМГ.
Методы исследования во время острой фазы заболевания. Методы исследования порфиринов и их предшественников варьировали в зависимости от лаборатории и возможностей стационара. Этим же объясняются и разные показатели нормальных значений для исследованных метаболитов. Основными методами диагностики были качественный тест Watson–Schwartz, определяющий более чем 4-кратное повышение уровня ПБГ в моче [2], а также количественная оценка АЛК и ПБГ [2, 11] и/или копропорфирина и уропорфирина в моче [15]. При этом в двух лабораториях хроматографические колонки заполняли вручную активированным углем [11], а в двух других лабораториях использовали хроматографические колонки Bio-Rad (Bio-Rad Laboratories, США) [11]. Для исследования собирали утреннюю порцию мочи в темную стеклянную банку. Анализы проводили не более чем через 3 ч после сбора мочи.
Методы исследования во время ремиссии. Исследования проводили в Центре исследования порфирии медицинского факультета Хельсинкского университета (Финляндия). Для количественной оценки уровня экскреции АЛК и ПБГ использовали Bio-Rad анионообменные хроматографические колонки (BioRad, США) [11]. Уровень уропорфирина и копропорфирина в моче, копропорфирина и протопорфирина в кале [15] оценивали при помощи высокоэффективной жидкостной хроматографии (ВЭЖХ, HPLC) [10]. Спектры флюоресценции порфиринов плазмы исследовали методом спектрофлюометрии [2]. Исследование активности гидроксиметилбилиансинтетазы эритроцитов осуществляли с помощью спектрофотометрии путем измерения конверсии ПБГ в уропорфирин [5]. ДНК-анализ генов HMBS и CPOX проводили путем прямого секвенирования экзонов, а также интронных областей [8, 14]. Биологический материал сохраняли при -20oC защищенным от света до момента транспортировки в лабораторию.
Вторичная порфиринурия
Общая характеристика пациентов с вторичной порфиринурией
У 12 пациентов, несмотря на клиническую картину возможной атаки острой порфирии, а также 1,5–3,5-кратное повышение уровней порфиринов и/ или их предшественников в моче, острая порфирия была исключена. Основным критерием исключения явилось менее чем 5-кратное повышение уровней предшественников порфиринов (ПБГ) в моче. Кроме того, у большинства пациентов была установлена как причина порфиринурии (в основном патология печени или употребление алкоголя), так и причина неврологической симптоматики.
Клиническая картина у пациентов с вторичной порфиринурией
У 10 пациентов ведущим клиническим синдромом была симметричная полиневропатия (см. табл. 1). Из них у 7 пациентов полиневропатия развилась до развернутой клинической картины в пределах 30 дней, т. е. соответствовала критериям острой полиневропатии, а у 3 – в течение 60 дней, т. е. была подострой в отличие от пациентов с острой порфирией, у которых полиневропатия всегда имела острое течение. У большинства пациентов полиневропатия была смешанной моторно-сенсорной с преобладанием моторного компонента, как и у пациентов с острой порфирией. Чувствительные нарушения соответствовали дистальной полиневропатии с вовлечением как поверхностной, так и, реже, глубокой чувствительности, что также принципиально не отличало их от пациентов второй группы.
Среди 5 пациентов с полиневропатией, которым была проведена электронейромиография (ЭНМГ), у 3 пациентов (2, 9, 10; см. табл. 1) выявлен преимущественно аксональный тип поражения периферических нервов, а у 2 (1 и 3) – диффузная демиелинизация. Обращает на себя внимание то, что аксонопатия была выявлена у пациентов с преимущественно токсическим генезом заболевания, а демиелинизация – с аутоиммунным. При этом для острой порфирии было бы характерно преобладание аксонопатии. Рутинное исследование цереброспинальной жидкости, выполненное у 3 пациентов группы наблюдения, патологии не выявило, также как и у больных с порфирией. У пациента 5 с клинической картиной асимметричного периферического пареза в ногах ЭНМГ верифицировала поясничную плексопатию, генез которой в дальнейшем был расценен как травматический (падения на фоне алкогольного опьянения).
Признаки острой энцефалопатии отмечались у 6 пациентов и проявлялись когнитивными нарушениями, реже делирием, галлюцинациями, угнетением сознания, очаговыми симптомами, что сближает их с пациентами второй группы, однако ни у одного пациента не было эпилептических припадков в отличие от пациентов с острыми порфириями (40% атак с энцефалопатией).
Магнитно-резонансная и компьютерная томография головного мозга не выявила острых очаговых изменений ни у одного из пациентов с энцефалопатией в отличие от 3 пациентов (из 11 пациентов, у которых выполнялась магнитно-резонансная и компьютерная томография головы) с острой порфирией, с картиной PRES (posterior reversible encephalopathy syndrome) [17].
У двух пациентов (6 и 9; см. табл. 1) отмечались признаки сочетанного поражения центрального и периферического мотонейронов, что нередко наблюдалось и у пациентов с порфирией с одномоментным развитием полиневропатии и энцефалопатии. При этом у пациентов с вторичной порфиринурией пирамидная недостаточность была обусловлена другой причиной (сифилис, сосудисто-мозговая недостаточность).
Болевой синдром был выражен у 9 пациентов, но только у 4 был представлен интенсивной болью в животе – оценка по визуально-аналоговой шкале (ВАШ) более 7 баллов [7] в отличие от пациентов с острыми порфириями, у которых полиневропатия всегда сочеталась с интенсивной болью в животе. У пациентов с вторичной порфиринурией гораздо чаще, чем боль в животе, встречались миалгии, невропатические болевые ощущения в конечностях, боль в спине. При этом чаще болевой синдром развивался одномоментно с полиневропатией или накануне ее появления.
Признаки автономной дисфункции у больных с вторичной порфиринурией чаще всего включали тахикардию, артериальную гипертензию, тошноту, рвоту. Таким образом, спектр автономной дисфункции был практически идентичен таковому у пациентов с порфириями. Вместе с тем в отличие от острой порфирии у большинства пациентов с вторичными порфиринуриями автономная дисфункция имела подострый характер.
Интересными оказались электролитные и ферментные изменения у больных с вторичной порфиринурией. Так, умеренная гипонатриемия и гипокалиемия отмечалась только у одного пациента с вторичной порфиринурией и гораздо чаще обнаруживалась у пациентов с первичными порфириями. Обращало на себя внимание частое повышение уровня трансаминаз до умеренных величин (табл. 2), что, по-видимому, указывает на гепатопатию как причину вторичной порфиринурии у этих пациентов. Этот показатель, однако, не может служить критерием дифференциального диагноза, так как повышение уровня трансаминаз – частое явление у пациентов с порфириями с неврологическими симптомами (табл. 3).
Повышение уровней порфиринов и/или их предшественников у пациентов с вторичной порфиринурией
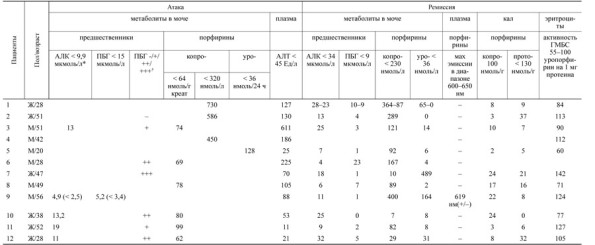
Степень повышения уровней порфиринов и/или их предшественников у пациентов группы наблюдения не превышала даже 4-кратного уровня (см. табл. 2), т. е. не соответствовала критериям диагноза атаки острой порфирии. Несмотря на это, у 8 пациентов диагноз острой порфирии был установлен в качестве безальтернативного основного диагноза, а у 2 пациентов даже была проведена специфическая патогенетическая терапия острой порфирии аргинатом гемма (Нормосанг, Orphan Drugs), при этом улучшение состояния пациентов совпало с проводимой терапией.
Для исключения острой порфирии у пациентки 7 с резко положительным качественным тестом на ПБГ (см. табл. 2) был исследован весь спектр порфиринов и их предшественников в фазе ранней ремиссии. У 7 пациентов уровни метаболитов порфиринового обмена нормализовались уже к моменту выписки из стационара. В 3 случаях нельзя было однозначно исключить острую порфирию во время острой фазы заболевания из-за постоянной копропорфиринурии (2–3-кратного повышения) и небольшого повышения уровня АЛК в одном случае. В течение 6-месячного наблюдения и повторных лабораторных исследований уровни порфиринов и их предшественников стабилизировались и у пациентов были установлены другие диагнозы.
Т а б л и ц а 2. Данные биохимических исследований у пациентов с вторичной порфиринурией
П р и м е ч а н и е . Здесь и в табл. 3: АЛК – аминолевулиновая кислота; ПБГ – порфобилиноген; АЛТ – аланинаминотрансфераза; ГМБС – гидроксиметилбилиансинтетаза; * – хроматографические колонки были вручную заполнены активированным углем; † – при проведении качественного теста Watson–Schwartz 4–5-кратное повышение уровня ПБГ соответствует +++ [2]. Незаполненные ячейки означают отсутствие соответствующих данных.
Сравнение с пациентами с острой порфирией
В отличие от пациентов с вторичной порфиринурией среди пациентов с острой порфирией были преимущественно женщины в возрасте 18–57 лет (средний возраст 32 года). Указание на подобные заболевания в семье у большинства пациенток также отсутствовали. Подробное описание клинической картины у 12 пациентов приведено в нашей предыдущей публикации [13].
В целом клиническая картина пациентов, страдающих острой порфирией, была сходной. Это можно отнести как к отдельным симптомам и синдромам, так и к их совокупности, однако можно отметить некоторые нюансы, клинически различающиеся у пациентов этих двух групп. В частности, у пациентов с острыми порфириями клиническая картина отличалась меньшей гетерогенностью. В отличие от пациентов с вторичной порфиринурией у всех пациентов с порфирийной полиневропатией она была острой и ей всегда предшествовали сильная боль в животе (оценка по ВАШ более 7 баллов [7]) и автономная дисфункция. У большинства пациентов острая полиневропатия развивалась вместе с энцефалопатией.
Ключевым моментом, позволяющим заподозрить острую порфирию является не столько сочетание определенных симптомов (идентичных у наших пациентов с вторичной порфинурией), но временн΄ые характеристики и последовательность их появления. В начале атаки возникает боль в животе, затем присоединяются симптомы острой автономной дисфункции, и только через 1–3 недразвивается острая полиневропатия и/или энцефалопатия.
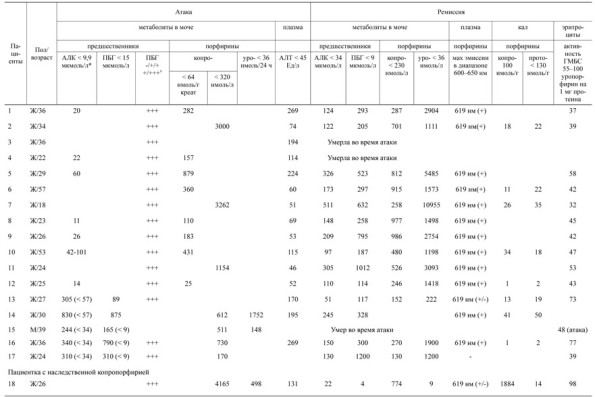
Т а б л и ц а 3. Данные биохимических исследований у пациентов с верифицированной ОПП
Т а б л и ц а 4. Алгоритм диагностики острых порфирий
П р и м е ч а н и е . АЛК – аминолевулиновая кислота; ВП – вариегатная порфирия; ГМБС – гидроксиметилбилиан синтетаза; НК – наследственная копропорфирия; ОПП – острая перемежающаяся порфирия; ПБГ – порфобилиноген; ПКП – поздняя кожная порфирия.
Следует помнить, что ряд заболеваний гепатобилиарной системы, отравления алкоголем, тяжелыми металлами, мышьяком, анемии, некоторые метаболические и инфекционные заболевания сопровождаются транзиторным повышением уровней порфиринов, в основном копропорфирина, и, реже, их предшественников [2]. Это обусловлено нарушением экскреции порфиринов с желчью, реже – частичной блокадой некоторых ферментов синтеза гемма (при отравлениях). Самой частой причиной порфиринурии считается острое или хроническое отравление алкоголем [2]. Самой тяжелой порфиринурией является отравлением свинцом, при котором уровень АЛК значительно повышен и имеет ведущее значение в патогенезе [2]. В остальных случаях порфиринурия является бессимптомным маркером, а все неврологические проявления вызваны другой причиной [2]. В литературе описаны всего 2 случая вторичных порфиринурий с неврологическими симптомами, и авторы статей предполагали, что эти симптомы обусловлены порфиринами [1, 12]. Это предположение мало вероятно, так как значительное повышение уровней порфиринов на фоне практически нормальных значений АЛК и ПБГ характерно для кожных порфирий, при которых никогда не развиваются неврологические симптомы [9].
Острую порфирию называют малым имитатором [3], и у большинства пациентов с клиническими симптомами, подозрительными в отношении острой порфирии, при обследовании выявляются другие заболевания. Это неудивительно, так как клиническая картина острой порфирии неспецифична [9]. Болевой синдром, автономная дисфункция, гипонатриемия, когнитивные нарушения и их комбинация могут также встречаться и при других полиневропатиях. Таким образом, скрининг на АЛК и ПБГ в моче должен быть выполнен у любого пациента с острой полиневропатией или энцефалопатией в сочетании с автономной дисфункцией или болевым синдромом.
Острые порфирии – редкие заболевания. Средняя распространенность ОПП в странах Западной Европы составляет 1,0–10,0 на 100 тыс. населения [9], что позволяет относить ее к редким заболеваниям, однако количество недиагностированных больных, скорее всего, превышает таковое выявленных, и, таким образом, истинная распространенность этого заболевания может быть выше.
Лабораторная диагностика имеет ключевое значение в диагностике острых порфирий [8] (табл. 4). Биохимические критерии атаки порфирии включают более чем 5-кратное повышение уровня ПБГ в моче, что может быть выявлено простыми качественными тестами Watson–Schwartz или Hoesch [2], которые очень дешевы и должны быть доступны в любом крупном стационаре. Результаты этих тестов должны всегда подтверждаться количественным измерением ПБГ в моче методом ионно-обменной хроматографии [11], так как при исследовании качественными методами возможны ложноположительные результаты (по данным литературы, до 30% [2]). В то же время необходимо иметь в виду, что разрушение ПБГ на свету (в случае, если исследуемые образцы не защищены от света) и отсроченное исследование ПБГ у больного с уже длительно текущей атакой являются основными причинами ложноотрицательных результатов.
При своевременном сборе материала, защите его от света во время сбора и транспортировки в лабораторию, а также при правильном проведении биохимических исследований установление диагноза острой порфирии во время атаки или его исключение не должно вызывать затруднений. К сожалению, некоторые лаборатории используют нестандартизованные методы количественной оценки порфиринов и их предшественников, которые менее чувствительны к повышению указанных метаболитов, что, возможно, приводит к отрицанию диагноза острой порфирии у части пациентов, обследованных в этих лабораториях. Так, обращают на себя внимание низкие показатели АЛК у наших пациентов с верифицированной в дальнейшем острой порфирией во время атаки. Эти результаты были получены при исследовании в лаборатории, использующей ручное заполнение хроматографических колонок активированным углем, что не соответствует современным лабораторным стандартам.
Анализ спектра порфиринов плазмы позволяет дифференцировать различные виды порфирий (см. табл. 4), а также подтверждает диагноз острой порфирии во время атаки [8]. Оценка биохимических показателей должна проводиться именно в момент острых симптомов, так как в дальнейшем этот уровень может снизиться, особенно при наследственной копропорфирии. У пациентов с ОПП, перенесших атаку с неврологической симптоматикой, уровень порфиринов и предшественников порфиринов обычно остается высоким пожизненно [8].
Таким образом, неврологические симптомы острых порфирий и состояний, сопровождающихся вторичной порфиринурией, могут быть идентичными. В связи с этим особое внимание должно быть уделено правильности применения алгоритма биохимической диагностики, включая не менее чем 5-кратное повышение уровня ПБГ в моче, оцененного на высоте неврологических симптомов. Основные причины ошибок интерпретации включают несвоевременный сбор биологического материала для исследования, незащищенность материала от света, проведение исследований в неспециализированных лабораториях, использование в качестве основного маркера острой порфирии только уровни копро- или уропорфиринов без исследования концентраций предшественников порфиринов – ПБГ и АЛК.
- Ahle G., Wierzba S., Haupts M. et al. Acute left hemispheric syndrome with cortical lesions in a patient with secondary porphyrinuria // J. Neurol. – 2005. – Vol. 252. – P. 983–984.
- Bonkovsky H. L., Barnard G. F. Diagnosis of porphyric syndromes: a practical approach in the era of molecular biology // Semin. Liver Dis. – 1998. – Vol. 18. – P. 57–65.
- Crimlisk H. L. The little imitator -porphyria: a neuropsychiatric disorder // J. Neurol. Neurosurg. Psychiatry. – 1997. – Vol. 62. – P. 319–328.
- Engelhardt K., Trinka E., Franz G. et al. Refractory status epilepticus due to acute hepatic porphyria in a pregnant woman: induced abortion as the sole therapeutic option? // Eur. J. Neurol. – 2004. – Vol. 11. – P. 693–697.
- Ford R. E., Ou C.-N., Ellefson R. D. Assay for erythrocyte uroporphyrinogen I synthase activity, with porphobilinogen as a substrate // Clin. Chem. – 1980. – Vol. 26. – P. 1182–1185.
- Goren M. B., Chen C. Acute intermittent porphyria with atypical neuropathy // South. Med. J. –1991. – Vol. 84. – P. 668–669.
- Jensen M. P., Karoly P. Self-report scales and procedures for assessing pain in adults // Handbook of Pain Assessment / Ed. R. Melzack. – New York: Guildford Press, 1992. – P. 135–151.
- Kauppinen R., von und zu Fraunberg M. Molecular and biochemical studies of acute intermittent porphyria in 196 patients and their families // Clin. Chem. –2002. – Vol. 48. – P. 1891–1900.
- Kauppinen R. Porphyrias // Lancet. – 2005. – Vol. 365. – P. 241– 252.
- Li F., Lim C. K., Peters T. J. Analysis of urine and faecal porphyrins by HPLC coupled to an advanced automated sample processor // Biomed. Chromatogr. – 1986. – Vol. 1. – P. 93–94.
- Mauzerall D., Granick S. Occurrence and determination of 5-aminolevulinic acid and porphobilinogen in urine // J. Biol. Chem. – 1959. – Vol. 219. – P. 435–446.
- Oberndorfer S., Hitzenberger P., Gruber W. et al. Secondary coproporphyrinuria in a patient with the full clinical picture of a hereditary acute hepatic porphyria. A misleading clinical and biochemical course // J. Neurol. – 2002. – Vol. 249. – P. 1325–1326.
- Pischik E., Bulyanitsa A., Kazakov V., Kauppinen R. Clinical features predictive of a poor prognosis in acute porphyria // J. Neurol. –2004. – Vol. 251. – P. 1538–1541.
- Pischik E., Mehtala S., Kauppinen R. Nine mutations including three novel mutations among Russian patients with acute intermittent porphyria // Hum. Mutat. – 2005. – Vol. 265. – P. 496.
- Rimington C. Quantitative determination of porphobilinogen and porphyrin in urine and faeces // Assoc. Clin. Path. Broadsheet. – 1958. – N 21. – P.
- Tan E., Kansu T., Zileli T. Severe ptosis without ophtalmoplegia due to porphyric neuropathy // Clin. Neurol. Neurosurg. – 1990. – Vol. 92. – P. 287–288.
- Yen P. S., Chen C. J., Lui C. C. et al. Diffusion-weighted magnetic resonance imaging of porphyric encephalopathy: a case report // Eur. Neurol. – 2002. – Vol. 48. – P. 119–121.
Источник: Пищик Е.Г., Казаков В.М., Руденко Д.И., Стучевская Т.Р., Посохина В.О., Обрезан А.Г., Кауппинен Р.Вторичная порфиринурия и гипердиагностика наследственных острых порфирий \\ Неврологический журнал. 2012. № 4. С. 13-21.
источник