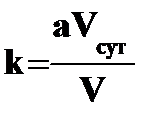При нагревании в мышцах из креатинфосфата образуется его альдегид – креатинин. Наибольшее количество креатинина образуется в мышцах при дефосфорилировании креатинфосфата.
В основе обнаружения и количественного определения креатинина положена цветная реакция креатинина в щелочной среде с пикриновой кислотой, в результате которой образуется окрашенный в оранжевый цвет пикрат креатинина.
По интенсивности окрашивания, определяемой колориметрически, контрольно (стандартный раствор бихромата калия) и иcследуемой смеси проб, можно расcчитать массовую концентрацию креатинина в исследуемой смеси.
Ход работы. В пробирку наливают 0,1 мл исследуемой мочи, прибавляют 0,1мл 10% раствора гидроксида натрия и оставляют стоять на 5 минут. Затем добавляют 0,15 мл насыщенного раствора пикриновой кислоты, взбалтывают и оставляют стоять 5 минут. Затем доводят объем до 10 мл дистиллированной водой и тщательно перемешивают. Измеряют светопоглощение опытной пробы против контрольной на ФЭК-е при 490 нм (зеленый светофильтр №5) в кювете с толщиной слоя 0,3. Контрольную пробу готовят как опытную, только вместо мочи берут равный объем дистиллированной воды.
Расчет: С1 = Д1Q/Д2V,
где Д1 и Д2 – значение оптических плотностей стандартного раствора бихромата калия и соответственно исследуемого раствора; Q — масса креатинина в 250 мл раствора, эквивалентная по окраске 1% стандартному р-ру бихромата калия (2,5); V – объем мочи, взятой для анализа.
10 мл раствора – 0,1 мг соответственно креатинина, норма – 9-18 ммоль/сутки.
Контрольные вопросы
1. Химический состав мышечной ткани.
2. Строение и функции миоглобина.
3. С чем связана АТФ-азная активность миозина?
4. Перечислить важнейшие функции миозина.
5. Пространственная организация молекулы актина.
6. Механизм процесса агрегации актина.
7. Механизм образования актомиозинового комплекса.
8. Пространственная организация молекулы тропомиозина.
9. Пространственная организация регуляторного белка — тропонина. Роль отдельных субъединиц тропонина в регуляции мышечного сокращения.
10. Роль кальция в регуляции мышечного сокращения.
11. Из каких последовательных процессов складывается мышечное сокращение?
12. За счет каких механизмов происходит уменьшение концентрации кальция в саркоплазме?
13. Перечислить основные источники энергии мышечной ткани.
14. Роль креатинфосфокиназной системы в процессе мышечного сокращения. Написать уравнение реакции, катализируемой креатинфосфокиназой.
15. Какие энергетические системы относятся к «быстрым» резервам и как осуществляется их взаимосвязь?
16. За счет каких источников покрываются энергетические затраты в покоящейся мышце?
17. За счет каких процессов обеспечивается энергией работающая мышца?
18. В чем причина накопления молочной кислоты в мышечной ткани?
19. Пути утилизации молочной кислоты в условиях покоя.
20. Направленность метаболистических процессов в мышечной ткани в состоянии покоя, в условиях интенсивной работы.
21. Роль карнозина и анзерина в мышечном сокращении.
22. Чем объясняется усиление биосинтеза мочевины в печени в период мышечной работы?
23. В чем заключается эндокринная функция миокарда?
Дата добавления: 2015-07-02 ; Просмотров: 515 ; Нарушение авторских прав? ;
Нам важно ваше мнение! Был ли полезен опубликованный материал? Да | Нет
источник
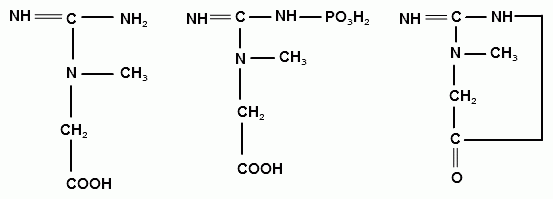
Креатин Креатинфосфат Креатинин
Повышенное содержание креатинина в моче наблюдается при острых инфекциях, лихорадочных состояниях, у больных сахарным и несахарным диабетом. Моча здорового человека не содержит креатина, и выделение его с мочой свидетельствует о патологии поперечнополосатых мышц (миостения, мышечная дистрофия).
Принцип метода. Метод количественного определения креатинина в моче основан на цветной реакции Яффе с пикриновой кислотой с последующим определением интенсивности окраски на ФЭКе. Концентрацию креатинина в исследуемой моче находят по калибровочной кривой, выражающей зависимость окраски стандартных растворов от их концентрации.
Ход определения. В одну мерную колбу отмеривают 0,5 мл мочи, в другую – 0,5 мл дистиллированной воды (контрольная проба). В обе колбы добавляют по 3 мл насыщенного раствора пикриновой кислоты, смесь перемешивают, добавляют по 0,2 мл 10% раствора NaOH и доводят объем дистиллированной воды до 100 мл. Перемешивают содержимое колб, выдерживают в течение 10 мин при комнатной температуре и измеряют на ФЭКе оптическую плотность опытной пробы против контроля в кюветах с толщиной слоя 1 см со светофильтром (зеленый, длина волны 540 нм).
Зная оптическую плотность опытного раствора, по калибровачному графику определяют содержание креатинина в пробе, взятой для анализа, и расчитывают количество креатинина, выделенного с мочой за сутки по формуле:
где α- содержание креатинина в пробе с мочой, найденное по калибровочному графику, ммоль; V-объем мочи, взятой для анализа, мл; Vсут – суточный объем мочи, мл.
| 0 5 10 15 20 мкмоль/проба |
| Еопт. плотн. |
| 0,4 0,3 0,2 0,1 |
Оформление работы. Записывают принцип метода, рисуют калибровочный график и указывают содержание креатинина в моче в норме.
Тема 4.4. Обмен фенилаланина, тирозина, аспарагиновой,
Глутаминовой кислот, валина, лейцина и изолейцина.
Вопросы для самоподготовки.
1.Напишите формулы фенилаланина и тирозина.
2.Напишите процесс превращения фенилаланина и тирозина в фумаровую и ацетоуксусную кислоты.
3.Напишите процесс синтеза адреналина.
4.Напишите процесс синтеза тироксина.
5.Нарисуйте схему превращения тирозина в меланин.
6.Нарисуйте схему обмена фенилаланина и тирозина.
7.Укажите на схеме места возможных генетически обусловленных блоков.
8.Назовите генетический дефект, приводящий к развитию фенилкетонурии.
9.Назовите основные клинические проявления фенилкетонурии.
10.Какой режим питания следует рекомендовать при фенилкетонурии и тирозинозе?
11.Назовите основные принципы коррекции фенилкетонурии.
12.Назовите локализацию генетического дефекта, приводящего к развитию тирозиноза.
13.Назовите лабораторно-диагностические признаки тирозиноза.
14.Назовите локализацию генетического дефекта, приводящего к развитию алкаптонурии.
15.Назовите диагностические признаки алкаптонурии.
16.Назовите локализацию генетического дефекта, приводящего к развитию альбинизма.
17.Назовите диагностические признаки альбинизма.
18.Что такое скрининг программа?
19.Назовите условия, необходимые для проведения скрининг-программ по выявлению наследственных заболеваний обмена аминокислот.
20.Назовите аминокислоты, являющиеся медиаторами нервной системы.
21.Назовите аминокислоты, являющиеся предшественниками медиаторов нервной системы.
22.Перечислите биологически активные вещества, для синтеза которых необходима глутаминовая кислота.
23.Составьте схему обмена глутаминовой кислоты в организме.
24.Напишите процесс превращения глутаминовой кислоты в глутамин.
25.Укажите биологическое значение глутамина.
26.Составьте схему использования амидного азота глутамина для синтеза различных соединений.
27.Перечислите биологически активные вещества, для синтеза которых необходима аспарагиновая кислота.
28.Назовите аминокислоту, из которой в организме человека образуется α-аланин.
29.Из какой аминокислоты в организме человека образуется β-аланин?
30.Составьте схему обмена аспарагиновой кислоты в организме.
31.Напишите процесс образования аспарагина.
32.Укажите биологическое значение аспарагина.
33.Напишите структурные формулы валина, лейцина и изолейцина.
34.Назовите места катаболизма аминокислот с разветвленной углеродной цепью.
35.Напишите уравнение реакции трансдезаминирования валина.
36.Назовите ферменты и коферменты, катализирующие реакцию трансдезаминирования валина.
37.Напишите уравнение реакции трансдезаминирования лейцина.
38.Назовите ферменты и коферменты, катализирующие реакцию трансаминирования лейцина.
39.Напишите уравнение реакции трансаминирования изолейцина.
40.Назовите фермент и кофермент, катализирующий реакцию трансаминирования изолейцина.
41.Назовите биохимические признаки заболевания «болезнь с запахом кленового сиропа».
42.Назовите клинические проявления заболевания «болезнь с запахом кленового сиропа».
Вопросы, задачи и упражнения для самоконтроля.
1.В каких процессах используются безазотистые остатки аминокислот:
| 1. фенилаланин; 2. глутаминовая кислота; 3. лейцин; 4. изолейцин. | а) глюконеогенез; б) кетогенез; в) оба процесса. |
2.Через какие метаболиты включаются в окисление пировиноградной кислоты безазотистые остатки аминокислот:
| 1. пируват; 2. α-кетоглутарат; 3. сукцинил-КоА; 4. оксалоацетат. | а) валин; б) аспарагиновая кислота; в) глутамин; г) глутаминовая кислота; д) лейцин. |
3.Укажите соответствие:
| 1. фенилаланин; 2. тирозин; 3. пролин; 4. аспарагиновая кислота; 5. валин. | а) заменимая; б) незаменимая; в) условно заменимая. |
4.Напишите схему синтеза глутамата из глюкозы.
5.Укажите, где синтезируется:
| 1. печень; 2. почки; 3. надпочечники; 4. меланоциты; 5. щитовидная железа. | а) меланины; б) йодтиронины; в) адреналин; г) гомогентизиновая кислота. |
6.В синтезе тирозина участвует:
2) тетрагидрофолевая кислота;
7.Катаболизм фенилаланина начинается с реакции:
8. Предшественники и биологическая роль основных биогенных аминов
| Сер | Три | Тир | Глу | Гис |
| Продкуты декарбоксилирования | ||||
| Биологически активные вещества | ||||
| Формулы | ||||
| Физиологическая роль |
9.Дополните схему недостающими компонентами:
Фен 1_____ 2_____ 3_____ 4_____ адреналин
10.Сравните ферменты:
| 1. фенилаланинтрансаминаза; 2. фенилаланингидроксилаза; 3. тирозингидроксилаза; 4. дофамингидроксилаза; 5. ДОФА-декарбоксилаза | а) необходим для синтеза тирозина; б) участвует в образовании ДОФА; в) катализирует синтез дофамина. |
Дата добавления: 2016-10-22 ; просмотров: 497 | Нарушение авторских прав
источник
Принцип метода.Метод основан на способности креатинина в щелочной среде взаимодействовать с пикриновой кислотой с образованием пикрата креатинина оранжево-красного цвета.
Ход работы.Приготовить опытную пробу:в цилиндр объемом 100 мл внести 0,5 мл мочи и 3 мл насыщенного раствора пикриновой кислоты. Смесь тщательно встряхнуть и добавить 0,2 мл 10% раствора едкого натра, выдержать 10 мин при комнатной температуре и довести дистиллированной водой до 100 мл. Приготовить контрольную пробу: к 3 мл раствора пикриновой кислоты добавить 0,2 мл 10% раствора едкого натра и довести объем смеси дистиллированной водой до 100 мл. Приготовить стандартную пробу: к 0,5 мл стандартного раствора (содержит 8,8 ммоль/л, или 1 г/л креатинина) прилить 3 мл раствора пикриновой кислоты и 0,2 мл 10% раствора едкого натра, выдержать 10 мин при комнатной температуре и довести дистиллированной водой до 100 мл. Интенсивность окраски опытной и стандартной проб измерить на ФЭКе против контрольного раствора в кювете с толщиной слоя 10 мм при зеленом светофильтре.
Расчет:концентрация креатинина(моль/сут) = (Еоп/Ест) × 8,8
Норма:4,4 – 17,6 моль/сут, или 0,5 – 2 г/сут.
Клинико-диагностическое значение.Содержание креатинина в моче зависит от характера питания, увеличиваясь при употреблении мясной пищи. Повышение его экскреции с мочой наблюдается при усиленной мышечной работе, лихорадочных состояниях, пневмонии авитаминозе Е, тиреотоксикозе и др.; понижение экскреции с мочой наблюдается при мышечной атрофии, лейкемии, амилоидозе почек, голодании.
Принцип определения креатинина методом Поппера
В щелочной среде пикриновая кислота взаимодействует с креатинином с образованием оранжево-красной окраски (реакция Яффе — образование таутомера пикрата креатинина), которую измеряют фотометрически. Определение в сыворотке крови проводят после депротеинизирования, в моче — после разведения водой. Определение не совсем специфично, интерферируют вещества с активной метиленовой группой и некоторые восстанавливающие вещества, например глюкоза, ацетон, ацетоуксусная и пировиноградная кислоты.
12. Количественное определение мочевой кислоты в крови.
Количественное определение мочевой кислоты в сыворотке крови по методу Мюллера-Зейферта.
Определение мочевой кислоты в сыворотке крови производится с диагностической целью. При подагре, пневмонии, анемии, почечной недостаточности, лечение опухолей рентгенотерапией наблюдается повышение содержания мочевой кислоты. Снижение уровня мочевой кислоты возможно при акромегалии, применении дикумарола, кортизона, салицилатов и инъекций инсулина.
В норме содержание мочевой кислоты в сыворотке крови взрослых составляет у мужчин — 0,24 – 0,50 млмоль/л (4,0-8,5мг/дл), у женщин – 0,16 – 0,40 млмоль/л (2,8-7,5 мг/дл).
Принцип метода.Мочевая кислота определяется в безбелковых фильтратах сыворотки крови по интенсивности синей окраски, развивающейся при восстановлении фосфорновольфрамого реактива.
Техника выполнения работы.
В центрифужные пробирки вносят 1 мл сыворотки крови, добавляют 8 мл дистиллированной воды, 0,5 мл 0,35М серной кислоты, перемешивают. Затем добавляют 0,5 мл 10% раствора вольфрамата натрия, опять переемешивают и через 10 мин. Центрифугируют в течение 10 мин при 1500 об/мин. После осаждения белков сыворотки крови центрифугированием ставят опытную, стандартную и контрольную пробы.
Опытная проба: 3 мл надосадочной жидкости переносят в чистую прбирку.
Стандартная проба: 3 мл 0,03М стандартного раствора мочевой кислоты (1 мл содержит 0,006 ммоль мочевой кислоты) налить в чистую пробирку.
Контрольная проба: В чистую пробирку прилить 3 мл дистиллированной воды.
Во все три пробирки добавляют 1,5 мл 10,3% раствора карбоната натрия, 1 мл фосфорновольфрамового реактива, тщательно перемешивают и через 30 мин опытную и стандартную пробы фотометрируют при длине волны 590-700 нм (красный светофильтр) в кювете длиной оптического пути 1 см против контрольной пробы.
Расчет:концентрацию мочевой кислоты рассчитывают по формуле:
С – концентрация мочевой кислоты, ммоль/л;
Еопыт. – экстинкция опытной пробы;
Естанд.— экстинкция стандартной пробы;
Сстанд. – концентрация стандартного раствора мочевой кислоты,
10 – коэффициент пересчета на объём сыворотки крови.
13. Общий анализ мочи: физико-химические свойства, химический состав мочи, определение патологических компонентов мочи.
Определение химических компонентов нормальной мочи.
Качественное определение хлоридов
Налить в пробирку 1 мл мочи, добавить 2 — 3 капли 30% раствора азотной кислоты и 3 — 4 капли 1% раствора азотнокислого серебра. Образуется творожистый осадок хлорида серебра. Написать реакцию.
Качественное обнаружение сульфатов
К 1 мл мочи добавить 2 — 3 капли 1% раствора уксусной кислоты и 2 — 3 мл раствора хлористого бария. Выпадает нерастворимый осадок сульфата бария. Написать реакцию.
В пробирку налить 1 мл молибденового реактива и нагреть его до кипения. После этого прибавить 5 — 6 капель мочи. Выпадает желтый кристаллический осадок фосфорно-молибденовокислого аммония, нерастворимый в азотной кислоте, но растворимый в аммиаке.
Обнаружение ионов кальция
К 1 мл мочи добавить 1 — 2 капли 3% раствора уксусной кислоты и 1 — 2 капли раствора щавелевокислого аммония. Выпадает осадок щавелевокислого кальция (кристаллы под микроскопом имеют вид конвертиков). Написать реакцию.
В пробирку налить 2 мл мочи, добавить равный объем раствора гидроксида кальция и над пробиркой держать смоченную водой красную лакмусовую бумажку. Через некоторое время бумажка синеет от выделяющегося аммиака.
Обнаружение креатинина (реакция Вейля)
К 1 мл мочи добавить 1 мл 10% раствора гидроксида натрия и 2 капли 10% раствора нитропруссида натрия, появляется красное окрашивание, которое впоследствии переходит в желтое.
Патологические компоненты мочи.
Качественное определение белка.
Белок мочи состоит из сывороточного альбумина и глобулинов. Кроме того, на белок дает реакцию моча, содержащая кровь и гной. Белок в моче обнаруживается с помощью реакций осаждения.
В нормальной моче содержится незначительное количество белка (0,05-0,15 г/сут), что не обнаруживается обычными качественными пробами. Белок в моче обнаруживается при нефрозе, нефрите, сердечной декомпенсации и при некоторых других патологиях. Пробы на белок мочи основаны на его денатурации различными агентами.
2 — 3 мл мочи (профильтрованной, если она щелочная, то ее подкисляют уксусной кислотой до слабокислой реакции) довести до кипения и добавить 2 — 3 капли уксусной кислоты. Появление осадка, не растворяющегося при прибавлении кислоты, указывает на присутствие в исследуемой моче белка. Осадки фосфатов и карбонатов кальция и магния растворяются в более кислом растворе.
К 1 мл концентрированной азотной кислоты осторожно, держа пробирку наклонно, наслоить 1 мл профильтрованной мочи (лучше наслаивать мочу пипеткой). На границе двух слоев при наличии белка появляется белое кольцо.
Проба с сульфосалициловой кислотой
К 1 мл профильтрованной мочи прилить 3 — 4 капли 20% раствора сульфосалициловой кислоты. Появление осадка или мути указывает на присутствие белка.
Примечание!Избыток сульфосалициловой кислоты может привести к растворению.
Качественное определение сахара в моче с помощью реактива Фелинга.
В норме в моче содержится 0,2-0,4 г/л глюкозы и она не обнаруживается обычными реакциями. При диабете и некоторых других заболеваниях, а также после обильного приема с пищей углеводов, эмоционального стресса, при отравлениях эфиром, оксидом, хлороформом, поражения почек он в значительных количествах появляется в моче.
В пробирку налить 1 — 2 мл мочи, добавить равный объем реактива Фелинга и осторожно нагреть верхний слой жидкости. При наличии сахара отметить выпадение кирпично-красного осадка.
Последнее изменение этой страницы: 2016-08-26; Нарушение авторского права страницы
источник
Креатин – важнейший компонент ткани скелетных мышц, сердца, головного мозга. В почках, печени и поджелудочной железе, синтезирующих креатин, содержание его невелико. В клетках креатин участвует в переносе энергии в виде креатинфосфата.
Одним из продуктов распада креатина выступает креатинин, который образуется неферментативным путем.
В креатинин превращается приблизительно 2% креатина, содержащегося в организме.
Определение содержания креатинина в сыворотке крови с использованием набора «Lachema-biotest»
Креатинин (42,5ммоль/л); альбумин (раствор 0,16г/л); трихлоруксусная кислота (1,22моль/л); пикриновая кислота (0,04моль/л); натрий гидроокись (0,75моль/л); реакционная смесь (раствор трихлоруксусной кислоты 0,15моль/л, пикриновая кислота 10,0моль/л, натрий гидроокись 0,19моль/л), соотношение сыворотка/реакционная смесь 1:8.
Штатив с пробирками, пипетки емкостью 1 и 2мл, центрифуга, ФЭК.
Метод основан на взаимодействии креатинина в щелочной среде с пикриновой кислотой с образованием оранжево – красной окраски, интенсивность определяется фотометрически.
Внести ингредиенты в следующих количествах:
| Отмерить в мл | Опыт | Контроль | Стандартный раствор |
| Сыворотка | 0,5 | — | — |
| Дистиллированная вода | 1,0 | 1,5 | 1,0 |
| Раствор 3 | — | — | 0,5 |
| Реактив 3 | 0,5 | 0,5 | 0,5 |
Перемешать и центрифугировать в течение 5-7 минут при 3000 об/мин.
| Реактив 4 | 0,50 | 0,50 | 0,50 |
| Реактив 5 | 0,50 | 0,50 | 0,50 |
Измерить точно через 20 минут оптическую плотность опыта (А1) и стандарта (А2) против контрольного раствора на ФЭКе при длине волны 500-510нм в кювете на 1см.
Количественное определение креатина и креатинина
Реактивы. Пикриновая кислота, насыщенный раствор * ; соляная кислота, 0,1 моль/л; основной калибровочный раствор креатинина * ; 12,5% раствор едкого натрия.
Оборудование. Штатив с пробирками; пипетки на 0,2; 1,0; 2,0 и 5,0 мл; ФЭК; водяная баня.
Материал. Исследуемая моча.
Принцип метода. Основан на способности креатинина в щелочной среде с пикриновой кислотой образовывать комплекс оранжевого цвета, интенсивность которого пропорциональна концентрации креатинина. Определение креатина проводится после перевода его в креатинин при нагревании мочи в солянокислой среде.
Ход определения. В три меченные обычные пробирки внести по 0,2 мл концентрированной соляной кислоты (осторожно, только пипеткой с резиновой грушей!). В 1-ю и 2-ю пробирки добавить по 0,2 мл исследуемой мочи, предварительно разведенной в 5 раз: 1 пробирка служит для определения креатинина, 2 – креатина, 3 – контрольная. Вторую пробирку нагреть в течение 5 минут на бурно кипящей водяной бане, после чего охладить под струей водопроводной воды. Во все пробирки внести дистиллированную воду в следующих количествах: первая пробирка – 2,0 мл, вторая – 2,0 мл, третья – 2,2 мл и в каждую добавить по 0,6 мл насыщенного раствора пикриновой кислоты и по 1,0 мл 12,5% раствора гидроксида натрия, тщательно перемешивают. Оставляют стоять на 10 минут при комнатной температуре, после чего во все три пробирки добавляют по 6,0 мл дистиллированной воды. Оптическую плотность исследуемых растворов определяли на ФЭКе с длиной волны 507 нм в кювете на 10 м против контрольной пробы (третья пробирка). Количество определялось по калибровочному графику.
Расчет. Находят содержание свободного креатинина в первой пробирке по калибровочному графику, а затем, используя нижеприведенную формулу, проводят расчет:
где х – количество креатинина в г на 1 л мочи;
а – количество креатинина в мкг в 0,2 мл разведенной мочи, взятой для анализа;
5 – для перевода количества креатинина с 0,2 мл мочи на 1 мл;
1000 – перерасчет на 1 л, числитель;
1000 – для перевода мкг в мг, знаменатель;
1000 – для перевода мг креатинина в г, знаменатель.
Расчет креатина – вторая пробирка содержит сумму свободного креатинина и креатинина, переведенного из креатина при нагревании в солянокислой среде. Из количества креатинина, полученного при определении суммы креатин-креатинин, вычитают количество параллельно исследуемого свободного креатинина и полученную разность умножают на 1,16 – коэффициент перевода креатинина в креатин.
Построение калибровочного графика: из рабочего калибровочного раствора креатинина готовят разведение, как указано ниже:
| №№ пробы | Рабочий калибр. р-р креатинина, мл | Раствор пикриновой кислоты, мл | 2,5 моль/л раствора NaOH, мл | Дистиллированная вода, мл | Концентр. креатинина в пробе, ммоль/л |
| 0,4 | 3,0 | 0,2 | До объема 10 мл | ||
| 0,8 | 3,0 | 0,2 | |||
| 1,6 | 3,0 | 0,2 | |||
| 2,4 | 3,0 | 0,2 | |||
| 3,2 | 3,0 | 0,2 |
Оформление работы. Рассчитать содержание креатина и креатинина в исследуемой пробе и в выводах дать оценку полученным результатам, сравнивая с нормой.
Практическое значение работы. Креатинин, наряду с мочевиной и солями аммония являются нормальными продуктами азотистого обмена и на его долю приходится около 2,5-7% всего азота мочи. Креатинина в норме выделяется с мочой: 4,4-17,7 ммоль/сутки или 0,5-2,0 г/сутки. В норме моча взрослых людей креатина не содержит. У детей имеет место физиологическая креатинурия, поэтому в моче он обнаруживается в небольших количествах. Появление креатина в моче взрослого человека связано с нарушением обмена креатина и наиболее часто встречается при поражении мышечной ткани (мышечная дистрофия, мышечная атрофия, миастения, миозит, миотония), Е-авитаминозе, при тонических судорогах, усиленном распаде тканевых белков. При этом содержание креатинина в моче понижается.
источник
Инструкция по применению набора реагентов для количественного определения содержания креатинина в сыворотке или плазме крови и моче человека «Креатинин-UTS»
Для выполнения измерений на полуавтоматическом или автоматическом биохимическом анализаторах следует:
8.15. Установить программу определения концентрации креатинина согласно таблице:
Число знаков после запятой
Максимум изменения оптической плотности, ед. опт. плотн.
Концентрация калибратора, мкмоль/л
Границы линейности, мкмоль/л
*- Нормальные величины концентрации креатинина в сыворотке или плазме крови мужчин.
8.16. При первом использовании набора, а также при получении новой серии необходимо провести калибровку с использованием входящего в состав набора калибратора креатинина.
8.17. Концентрация креатинина в анализируемом образце рассчитывается в мкмоль/л на основании калибровочной прямой, рассчитанной автоматически и сохраненной в памяти биохимического анализатора.
8.18. Если полученная концентрация креатинина в анализируемом образце выше 1760 мкмоль/л, то исследование следует повторить: разбавить анализируемый образец 0,9% раствором NaCl в соотношении 1:1, повторно измерить и полученный результат определения умножить на 2.
9.1. Набор реагентов «КРЕАТИНИН –UTS» должен храниться в упаковке предприятия-изготовителя при температуре +2..+8 ОС в течение всего срока годности, указанного на упаковке. Замораживание компонентов набора не допускается.
9.2. Реагенты Р1 и Р2 после вскрытия флаконов могут храниться при температуре +2..+8 ОС в защищенном от света месте в течение всего срока годности в плотно закрытом флаконе.
9.3. Калибратор после вскрытия флакона можно хранить при температуре +2-8 ОС не более 1 месяца при условии достаточной герметичности флакона.
9.4. Для получения надежных результатов необходимо строгое соблюдение инструкции по применению набора.
9.5. Правильность определения можно проверить по контрольным сывороткам, аттестованным по содержанию креатинина методом Яффе.
1. Tietz N W et al. Clinical Guide to Laboratory Tests, 3rd ed AACC 1995.
2. Murray R. L. Creatinine. Caplan A et al. Clin Chem The C. V. Mosby Co. St. Louis. Toronto. Princeton 1984; 1261-1266. and 418.
3. Young DS. Effects of disease on Clinical Lab. Tests, 4th ed AACC 2001.
Производится по заказу /О Юнимед».
По вопросам, касающимся качества набора «КРЕАТИНИН –UTS» следует обращаться в /О ЮНИМЕД» Москва, ул. Касаткина, 3а; Тел. (495) 734-91-31, 8-800-333-91-31, Факс: (495) 564-86-41.
по применению набора реагентов для количественного определения содержания креатинина в сыворотке или плазме крови и моче человека
Набор реагентов «КРЕАТИНИН-UTS» разрешен к производству, продаже и применению на
Регистрационное удостоверение № ФСР 2009/05456
Информация для заказа набора «КРЕАТИНИН-UTS»
Р1 (50 мл) + Р2 (50 мл) + калибратор (1 мл)
Р1 (200 мл) + Р2 (200 мл) + калибратор (4 мл)
*v – объем фотометрической ячейки анализатора.
1.1. Набор реагентов «КРЕАТИНИН — UTS» предназначен для количественного определения содержания креатинина в сыворотке или плазме крови и моче человека в клинико-диагностических и биохимических лабораториях для целей диагностики заболеваний и контроля проводимого лечения пациентов.
1.2. Креатинин – конечный продукт распада креатина, компонента мышечной ткани, который может трансформироваться в АТФ, являющуюся источником высокой энергии клетки и играющую важную роль в энергетическом обмене мышечной и других тканях. Образование креатинина зависит от состояния мышечной массы и меняется очень незначительно. Экскретируется почками посредством клубочковой фильтрации. Повышение уровня креатинина является показателем почечной недостаточности, также может наблюдаться при сахарном диабете, кишечной непроходимости, ожогах и других заболеваниях[1,2]. На этом основано клиническое значение анализа.
1.3. Потенциальный риск применения набора – класс 2а. Основной риск косвенный и связан с возможностью получения неверного результата анализа, что может привести к неправильно поставленному диагнозу и назначению неэффективного лечения пациента. Для снижения указанного риска необходимо в каждой аналитической серии контролировать качество проведения результатов анализов с применением контрольных сывороток в соответствии с ОСТ 91500.13.0001-2003.
2.1. Метод основан на реакции, описанной Яффе. Креатинин в щелочной среде взаимодействует с пикриновой кислотой с образованием окрашенного комплекса.
2.2. Фотометрическое определение основано на наличии пика поглощения с максимумом при длине волны 510 (500 — 520) нм, образованного молекулами комплекса красного цвета [1]. Увеличение оптической плотности реакционной смеси пропорционально интенсивности окраски и, следовательно, прямо пропорционально содержанию креатинина в исследуемом образце.
3.1. Поскольку рабочий реагент, содержащий все компоненты для обеспечения химической реакции креатинина с пикриновой кислотой, нестабилен, набор реагентов «КРЕАТИНИН-UTS» поставляется в виде двух реагентов Р1, Р2 и раствора калибратора.
источник
Креатинин является одним из конечных продуктов азотистого обмена и нормальной составной частью мочи. За сутки с мочой выделяется креатинина у мужчин 8,8-17,7 ммоль (1-2 г/сут), а у женщин – 1,7-15,9 ммоль (0,8-1,8 г/сут). Креатинин — ангидрид креатина. Креатин содержится в мышцах (около 80%), особенно в сердечной, где из него при участии АТР образуется макроэргическое соединение креатинфосфат, при распаде которого образуется креатинин и фосфат. Креатин в моче взрослого здорового человека отсутствует, появление его в моче называют креатинурией. Однако у детей и подростков моча всегда содержит креатин.
Принцип метода. Креатинин при взаимодействии с пикриновой кислотой в щелочной среде образует окрашенные соединения, интенсивность окраски которых пропорциональна концентрации креатинина в моче и сыворотке крови.
Исследуемый материал: моча, сыворотка крови.
Реактивы: стандартный раствор креатинина (177 мкмоль/л), 2%-ный раствор пикриновой кислоты, 10%-ный раствор NaOH, 5%-ный раствор ТХУ, дистиллированная вода.
Оборудование: пробирки. пипетки, ФЭК, кюветы.
ХОД РАБОТЫ. В трех пробирках смешивают реактивы по схеме:
| Реактивы (мл) | Опытная проба | Стандарт | Контроль |
| Сыворотка | 0,5 | — | — |
| Дистиллированная вода | 1,5 | ||
| ТХУ | 0,5 | 0,5 | 0,5 |
| Стандартный раствор | — | 0,5 | — |
Через 5 мин опытную пробу и стандартную пробы центрифугируют при 3000 об/мин в течение 5 мин. С надосадочной жидкостью готовят следующие пробы:
| Реактивы (мл) | Опытная проба | Стандарт | Контроль |
| Надосадочная жидкость | 1,0 | 1,0 | 1.0 |
| Пикриновая кислота | 0,5 | 0,5 | 0,5 |
| NaOH | 0,5 | 0,5 | 0,5 |
Перемешивают и через 20 мин колориметрируют опытную и стандартную пробы при зеленом светофильтре (540 нм) в кювете толщиной 0,5 см против контроля. Расчет проводят по формуле:
Перед определением содержания крекатинина мочу разводят в 100 раз. Это разведение учитывают при расчетах. В опытной пробе смешивают о,5 мл мочи, 0,25 мл дистиллированной воды, 0,25 мл ТХУ, 0,5 мл пикриновой кислоты, 0,5 мл NaOH. Через 20 мин колориметрируют на зеленом светофильтре (длина волны 540 нм) в кювете толщиной 0,5 см против контроля, приготовленного в предыдущей работе. Расcчитывают концентрацию креатинина в моче по формуле с учетом ее разведения:
Содержание креатинина суточной моче рассчитываю по формуле
где С – концентрация креатинина в моче в мкмоль/л; 1,5 – суточный диурез в литрах, 1000 – коэффициент перевода мкмоль в ммоль.
Норма креатинина в сыворотке крови – 53-106 мкмоль/л, в суточной моче – 4,4-17,6 ммоль/сутки.
Клиренс креатинина (его очищение рассчитывают по формуле
где1,07 минурный диурез. В норме клиренс по креатинину составляет 80 – 120 мл/мин.
Клинико-диагностическое значение. Определение креатинина проводят для исследования функции почек. Содержание его в сыворотке крови увеличивается при значительном ухудшении функции почек. Креатинемия наблюдается также при закупорке мочевых путей, кишечной непроходимости, тяжелом диабете, механической желтухе, гипофункции надпочечников, голодании. Увеличение креатинина в моче наблюдается при усиленной мышечной работе, лихорадочных состояниях, пневмонии, выраженной недостаточной функции печени. Понижение креатинина в моче – при мышечной дистрофии, голодании, дегенерации почек, лейкемии. Расчет клиренса креатинина позволяет получить информацию об интенсивности основных функций фильтрации, реабсорбции, секреции и почечном кровообращении.
Не нашли то, что искали? Воспользуйтесь поиском:
Лучшие изречения: При сдаче лабораторной работы, студент делает вид, что все знает; преподаватель делает вид, что верит ему. 9224 — 

195.133.146.119 © studopedia.ru Не является автором материалов, которые размещены. Но предоставляет возможность бесплатного использования. Есть нарушение авторского права? Напишите нам | Обратная связь.
Отключите adBlock!
и обновите страницу (F5)
очень нужно
источник
· Колориметрический химический. Метод Поппера, основанный на реакции Яффе. Принцип метода:в щелочной среде пикриновая кислота реагирует с креатинином с образованием соединения оранжево-красного цвета, интенсивность окрашивания оценивают фотометрически при длине волны 505 нм.
· Колориметрический ферментативный саркозиноксидазный/ перок-сидазный метод. Принцип метода:



Концентрация продукта реакции пропорциональна концентрации креатинина в пробе.
· Спектрофотометрический (УФ), ферментативный креатинин-иминогидразный (КИГ)/глутаматдегидрогеназный метод. Принцип метода:
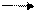

Скорость окисления НАДФН пропорциональна концентрации креатинина.
Клинико-диагностическое значение исследования концентрации креатинина в сыворотке крови и моче.
Гиперкреатининемия – увеличение уровня креатинина плазме/сыворотке крови обусловлено как усиленным образованием, так и задержкой его в организме. Критическая концентрация креатинина в сыворотке крови: ˃400 мкмоль/л. Ретенционная гиперкреатининемия обусловлена нарушением (острым и хроническим) функции почек любого происхождения. Продукционная гиперкреатининемия отмечается при кишечной непроходимости, декомпенсации деятельности ССС, пневмонии, лихорадочных состояниях, гипертиреозе, голодании, усиленной мышечной работе. Снижение уровня креатинина в сыворотке крови коррелирует с уменьшением мышечной массы (мышечные дистрофии и атрофии, параличи и др.).
Увеличение суточного выведения креатинина с мочойуказывает на увеличение почечной фильтрации и/или повышенное образование креатинина и креатинина в скелетных мышцах. Увеличением концентрации сопровождаются: усиленная мышечная работа, лихорадочные состояния, пневмония, акромегалия, сахарный диабет, острые инфекционныхе заболеванияя. Уменьшение выведения креатинина с мочой наблюдается при мышечной атрофии, паралечах, хронических заболеваниях почек, острой почечной недостаточности, голодании. В моче помимо эндогенного креатинина содержится экзогенный креатинин, поступающий в организм с мясной пищей.
На концентрацию креатинина в крови и моче влияет характер диеты преимущественно мясная диета приводит к увеличению, и наоборот, вегетарианская диета – к снижению концентрации креатинина в крови и моче.
Соотношение мочевины азот/креатинин.
Нормальные величины 12:1 – 20:1. КДЗ: ↑при снижениипочечной перфузии (застойная сердечная недостаточность, гипогидратация); повышенный катаболизм; диета с высоким содержанием белка; обструктивная уропатия; ↓ при остром некрозе почечных канальцев.
Измерение скорости клубочковой фильтрации (СКФ).
Креатинина клиренс-тест.
Клубочковая фильтрация является основным процессом мочеобразования, который протекает в почечном клубочке. В сутки образуется 150-180 л первичной мочи, поступающей в канальцы. Скорость, с которой образуется первичная моча, называется скоростью клубочковой фильтрации (СКФ).
СКФ – объем плазмы, фильтруемый в клубочках в единицу времени.
Для оценки СКФ в клинической практике определяют клиренс эндогенного креатинина (проба Реберга-Тареева). Вопрос: «Почему именно креатинин используют для расчета СКФ?» Ответ: «Продукция креатинина скелетными мышцами прямо пропорциональна мышечной массе и ее величина относительно постоянна. Креатинин не реабсорбируется в почечных канальцах, а тубулярная секреция креатинина в норме составляет очень малую часть от общего клиренса креатинина. Эти свойства креатинина делают его удобным эндогенным маркером СКФ». Клиренс креатининаэто объем плазмы крови, который очищается от креатинина за 1 минуту при прохождении через почки. Чем эффективнее работают почки по очищению крови от креатинина и выведению его с мочой, тем выше клиренс.
3.1. Проба Реберга-Тареева
В клинической практике наиболее широко применяется проба Реберга-Тареева, основанная на определении концентрации креатинина в сыворотке крови и моче (часовой или суточный креатинина клиренс-тест). При выполнении пробы мочу собирают за 2 ч (часовой) или 24 ч (суточный клиренс), сыворотку (плазму) получают в середине времени сбора мочи. До и во время проведения теста больной должен получать адекватное количество жидкости, чтобы обеспечить скорость тока мочи около 2 мл/мин. Во время исследования больной должен находиться на полупостельном режиме, исключается прием диуретиков.
В лаборатории определяют концентрацию креатинина в сыворотке крови (Ккр) и моче (Км) пациента, а также рассчитывают минутный диурез (Д), исходя из объема мочи. Например, объем суточной мочи равен 1350 мл; это количество в мл делим на 24 ч в минутах – 1440 мин, получим Д = 0,94 мл/мин.
Клиренс креатинина (С) рассчитывают по формуле:
К м (мкмоль/л)

Ккр (мкмоль/л)
Может потребоваться определение клиренса креатинина из однократного клиренса савороточного креатинина для оценки терапии нефротоксическими препаратами или при невозможности аккуратного суточного сбора мочи. В таком случае применяют номограмму или формулу:
СКФ = [(140 – возраст, лет) х (вес, кг)]+ (72 х креатинин сыворотки, мг/дл)
(Показатель для женщин – 85% от вычисленного. Умножить на 0,85).
Представленная формула корректна для пациентов со стабильной почечной функцией, без значительного ожирения или отечности.
источник
Креатинин – это конечный продукт обмена белка. Образуется в мышцах, используется для их сокращения и поступает в кровь. Выводится почками, при нарушении их работы уровень в крови возрастает, что может быть одним из признаков почечной недостаточности. Подробнее о возможностях исследования функции почек при помощи определения креатинина в крови и моче, а также причинах нарушений и способах их нормализации узнайте из этой статьи.
Это соединение относится к азотистым шлакам и должно быть выведено из организма. Концентрация креатинина в крови зависит от двух факторов – скорость образования в мышечных волокнах и быстрота фильтрации мочи в почках. Поэтому анализы отражают повреждение мышечной ткани и работу почек. Все показания к обследованию можно разделить на несколько групп в зависимости от целей.
Врач назначает определение креатинина в крови при таких симптомах:
- отеки под глазами по утрам;
- отечность ног при активном движении или поясницы у лежачих больных;
- необъяснимое повышение веса (указывает на скрытые отеки);
- увеличение объема живота (подозрение на асцит);
- боль, жжение при мочеиспускании, прерывистая струя;
- учащенное выделение мочи, преимущественно по ночам;
- помутнение мочи, красный или бурый оттенок;
- устойчивое повышение артериального давления;
- повышенная температура тела;
- боль в пояснице, в подреберных областях;
- резкая слабость, тошнота, головокружение;
- нарушение сна, памяти, аппетита;
- мышечные боли, снижение переносимости физических нагрузок.
Эти симптомы указывают на возможное поражение почек, снижение их фильтрационной способности, накопление в крови продуктов обмена веществ, интоксикацию.
Для анализа мочи к показаниям может быть отнесена сухость во рту, повышенная жажда, приступы голода, обильное выделение мочи. Такие признаки встречаются при сахарном диабете и симптоматической гипергликемии (заболевания гипофиза, надпочечников и щитовидной железы).
А здесь подробнее о лабораторной диагностике инфаркта миокарда.
Анализ крови и мочи на креатинин может применяться для диспансеризации или при поступлении в стационар. С их помощью отбирают (проводят скрининг) пациентов с нарушениями функции почек. Это может понадобиться в таких случаях:
- планируется операция;
- назначена томография (компьютерная, магнитно-резонансная), ангиография с введением контрастного вещества;
- есть подозрение на острую или хроническую почечную недостаточность;
- требуется рассчитать дозировки сильнодействующих препаратов, выводящихся почками;
- при беременности;
- тяжелая травма, ожоги, шоковое состояние.
Ангиография почек с введением контрастного вещества
Мониторинг концентрации креатинина требуется при лечении заболеваний почек, проведении интенсивной медикаментозной терапии, гемодиализа, после операций, при артериальной гипертонии, сахарном диабете, болезнях крови, сердечной недостаточности, дерматомиозите.
Определение креатинина в сыворотке крови врач может назначить как самостоятельный вид исследования, так и в сочетании с анализом мочи. Общими условиями для получения достоверного результата являются:
- ограничение занятий спортом и физических нагрузок за сутки до диагностики;
- исключение из рациона за 2 — 3 дня крепкого кофе, чая, алкоголя, существенное снижение мясных, рыбных и молочных блюд (не более 300 г суммарно в сутки);
- водный режим не ограничивается, он должен быть обычным для пациента;
- прекращение приема пищи за 12 часов до взятия крови;
- отсутствие эмоциональной, физической активности и курения за полчаса до исследования крови.
Гормональные препараты, противовоспалительные и мочегонные средства, антибиотики, витамин С, нитрофураны и медикаменты для лечения паркинсонизма могут изменить результаты. Поэтому врач может их отменить или порекомендует предоставить список в лабораторию, где будет проходить исследование.
Для сбора мочи потребуется утром удалить первую порцию, а все последующие – собирать в чисто вымытую банку, которая хранится в холодильнике. Последней нужно перелить утреннюю мочу следующего дня. Обязательно следует измерить общий объем, записать его на бланке направления и отлить в стерильную посуду 50 мл.
Помимо стандартных исследований крови и мочи на креатинин могут понадобиться и дополнительные тесты. Проба Реберга является способом определения фильтрации мочи, ее обратного всасывания и эффективности почечного кровообращения. Ее используют для выявления поражения ткани почек, степени недостаточности их функции.
Реже для пробы применяется суточный сбор мочи.
По уровню креатинина можно определить потерю белка с мочой (протеинурию). В таком случае достаточно взять разовую (утреннюю) порцию мочи и рассчитать коэффициент соотношения альбумина и креатинина. Эта методика достаточно информативная, простая в проведении, она используется при заболеваниях почек, оценке риска гипертонической и диабетической нефропатии.
У здорового человека небольшое количество креатинина всегда присутствует в крови и моче, так как белковый обмен происходит непрерывно. У мужчин, людей плотного телосложения и спортсменов его содержание выше, так как объем мышечной массы у них больше.
После 60 лет незначительный рост концентрации объясняется возрастным снижением фильтрационной способности почек. Отмечается также градация уровня и у детей в разные периоды жизни.
Нормальные показатели креатинина в крови и моче
Проба Реберга считается нормальной, если скорость выведения вещества (клиренс) соответствует приведенным референсным значениям. В классическом варианте креатинин вводился извне, а советский врач Тареев усовершенствовал метод, использовав концентрацию собственного (эндогенного). Поэтому чаще этот способ называют пробой Реберга-Тареева.
Показатели очистительной функции почек (скорости клубочковой фильтрации) в норме
Если обнаружено небольшое отклонение от нормальных показателей, то это может быть связано с такими причинами:
- интенсивные физические или эмоциональные нагрузки непосредственно перед обследованием;
- преобладание в рационе белковой пищи – мясные, рыбные, молочные продукты, коктейли с протеином, яйца;
- беременность;
- применение медикаментов.
Патологическое повышение обнаруживается при заболеваниях:
- почек – гломерулонефрит с острым или хроническим течением, амилоидоз, пиелонефрит, почечные опухоли, туберкулез, нефропатия при диабете, гипертонии и у беременных, мочекаменная болезнь;
- распад мышечной ткани – травмы, длительное сдавление, дерматомиозит, обширный инфаркт миокарда, миокардит, недостаточность кровообращения, гипертоническая болезнь, симптоматические гипертензии, применение статинов для снижения холестерина крови;
- кровотечение из пищеварительного тракта, непроходимость кишечника;
- новообразования – злокачественный процесс с распадом тканей, лейкемия, опухоль тимуса;
- обширные ожоги, интенсивная потеря крови, обезвоживание;
- шоковое состояние;
- нарушение работы органов эндокринной системы – повышенная активность надпочечников, щитовидной железы, гипофиза и гипоталамуса.
Инфаркт миокарда
В моче повышенный креатинин обнаруживают при аналогичных состояниях, но к причинам также относятся инфекции, гипотиреоз, отравление угарным газом, анемия.
Факторами, которые приводят к снижению содержания креатинина в крови, являются:
- отсутствие в пище животного белка – веганский и вегетарианский стиль питания;
- дистрофия или атрофия мышц врожденная или приобретенная;
- паралич или ампутация конечностей;
- первый триместр беременности (повышен объем крови и фильтрация почек);
- гемодиализ;
- нарушение синтеза вазопрессина с уменьшением выведения мочи (избыток жидкости в организме).
Креатинин также снижается в моче, которая оттекает от почки с суженной артерией из-за слабого прохождения через нее крови.
Смотрите на видео о биохимическом анализе — креатинин:
Так как причин для нарушений содержания креатинина в крови и моче достаточно много, то эти анализы используют только в дополнение к клиническим симптомам. На основании полученных данных обычно определяется тактика дальнейшего инструментального обследования.
Терапия назначается в соответствии с обнаруженной патологией, если показатель превышает 500 мкмоль/л, то пациента срочно госпитализируют и подключают к гемодиализу для искусственного очищения крови. Чтобы снизить содержание креатинина (вне зависимости от фонового заболевания) рекомендуется:
- ограничить мясо и все мясные продукты (колбасы, полуфабрикаты, копчения), рыбу, яйца, грибы и молоко, творог, сыр, кисломолочные напитки, чай, кофе и алкоголь в меню;
- бобовые (фасоль, нут, маш, чечевица, горох) и киноа разрешаются в небольших количествах;
- основу рациона должны составлять овощи, крупы, фрукты;
- объем жидкости зависит от суточного диуреза, если нет отеков, то оптимально пить чистую воду в количестве 1,5 — 1,8 литра в день;
- при удовлетворительном общем состоянии полезны пешие прогулки в среднем темпе, плавание.
А здесь подробнее о протеине в крови.
Содержание креатинина в крови отражает состояние фильтрационной способности почек и повреждения мышечной ткани. Он выводится только с мочой и при недостаточности почечной функции концентрация в плазме возрастает. Для анализа применяется как стандартное исследование уровня, так и проба Реберга-Тареева, соотношение креатинина и альбумина.
Для получения достоверных результатов требуется подготовка. Итоги диагностики врач оценивает в комплексе с клинической картиной. Для снижения уровня, помимо специального лечения, нужно изменить стиль питания.
Смотрите на видео о диете для снижения креатинина:
Довольно неприятный показатель — давление при почечной недостаточности. Если при хронической регистрируют высокие или низкие показатели АД, его срочно необходимо привести в норму таблетками и препаратами. Какие лекарства подходят?
Сделать анализ крови на холестерин полезно даже абсолютно здоровому человеку. Норма у женщин и мужчин отличается. Биохимический и развернутый анализ ЛПВП правильно сделать натощак. Подготовка требуется. Обозначение поможет расшифровать врач.
Опасный для жизни тромбоз почечной артерии сложно поддается лечению. Причины его появления — пороки клапанов, удар в живот, установка стента и прочие. Симптомы схожи с острой почечной коликой.
Назначают анализы при гипертонии для выявления ее причин. В основном это обследования крови и мочи. Иногда диагностика проводится в стационаре. Кому стоит сдать анализы для профилактики?
Определяют протеин в крови при подозрениях на многие патологии, в том числе онкологию. Анализ помогает определить норму, повышенные показатели реактивного с и протеина s. Стоит разобраться и со значениями: кровь на эозинофильный катионный протеин, тотал. Сгущает или нет кровь?
Лабораторная диагностика инфаркта миокарда включает общие анализы крови и мочи. Своевременность проведения, правильная расшифровка поможет назначить лечение.
Берутся анализы на васкулит для подбора дозировки лекарств и степени прогрессирования заболевания. О чем расскажет диагностика по анализам крови? Какие сдают лабораторные и инструментальные при геморрагическом васкулите, чтобы его определить?
К сожалению, все чаще диагностируется гипертония у молодых. В основном причины ее появления заключаются в неправильном образе жизни у мужчин и женщин, внешних факторах. Препараты выбора для лечения гипертонии в этом возрасте направлены на стабилизацию показателей.
Развивается атеросклероз почечных артерий из-за возраста, вредных привычек, избыточной массы тела. Вначале симптомы скрыты, если они проявились, то болезнь сильно прогрессирует. В этом случае необходимо медикаментозное лечение или операция.
источник
Креатинин является компонентом остаточного азота крови. Это конечный продукт превращения креатинфосфата в мышцах, мозге. Креатинфосфат в свою очередь участвует в энергообеспечении данных тканей. При участии фермента креатинкиназы происходит расщепление креатинфосфата с образованием энергии и креатинина, который экскретируется из организма с мочой. Основное диагностическое использование креатинина – это оценка почечной фильтрации. При нарушении фильтрации в почках происходит нарастание креатинина в крови и снижение его в моче. По содержанию креатинина в крови и моче можно рассчитать клиренс креатинина, данный показатель позволяет оценить скорость почечной фильтрации. При нарушении
функции почек клиренс креатинина снижается. Повышение экскрекции креатинина с мочой может наблюдаться при лихорадочных состояниях, недостаточности печени, инфекционных заболеваниях, а также при высоких физических нагрузках. По количеству выделяемого креатинина можно судить об интенсивности физической нагрузки у спортсменов и тренированности мышц. Уменьшение креатинина в моче связано с мышечной атрофией, параличами, хроническими заболеваниями почек (амилоидоз). Определение содержания креатинина в сыворотке (плазме) крови и моче основано на реакции Яффе.
Принцип метода: креатинин в щелочной среде реагирует с пикриновой кислотой с образованием комплекса желто-красного цвета. Скорость
образования комплекса пропорциональна содержанию креатинина в исследуемом материале. Нормы: в сыворотке крови женщины – 44-88 мкмоль/л, мужчины – 44-100 мкмоль/л (нормы могут варьировать в зависимости от конкретного метода); в моче – 4,4-17,7 ммоль/сутки.
Тестовый контроль по теме «Обезвреживание аммиака.
Остаточный азот крови»
ВыбЕрИтЕ правильнЫЙ ответ.
Ферменты орнитинового цикла локализованы:
а) на мембране митохондрий
в) на мембранах комплекса Гольджи
г) и на мембранах митохондрий и в цитозоле клетки
д) и на мембранах комплекса Гольджи и в цитозоле
ВыбЕрИтЕ правильнЫЙ ответ.
Орнитиновый цикл в митохондриях протекает до образования:
ВыбЕрИтЕ правильнЫЙ ответ.
Транспортными формами аммиака в организме принято считать:
ВыбЕрИтЕ ВСЕ правильныЕ ответЫ.
Глюкозо-аланиновый цикл включает реакции:
а) декарбоксилирования ГЛУ
б) декарбоксилирование ПВК
в) восстановительное аминирование a-кетоглутаровой
г) восстановительное аминирование ПВК
д) переаминирование ГЛУ и ПВК
(для каждого вопроса – один или несколько правильных ответов, каждый ответ может быть использован один раз или не использован совсем)
| Процессы, в ходе которых образуются метаболиты: | Метаболиты: |
| 1) обезвреживание NН3 2) обезвреживание бензойной кислоты 3) обезвреживание продуктов гниения триптофана | 1) а) мочевина б) гиппуровая кислота в)индикан г) аммонийные соли д) креатинин |
ВыбЕрИтЕ правильнЫЙ ответ.
Общим метаболитом ЦТК и орнитинового цикла является:
(для каждого вопроса – один или несколько правильных ответов, каждый ответ может быть использован один раз)
| Органы синтеза данных метаболитов: | Метаболиты: |
| 1) Печень 2) почки 3) мышцы | а) мочевина б) аммонийные соли в) гиппуровая кислота г) индикан д) креатинин |
ВыбЕрИтЕ правильный ответ.
Патология почек сопровождается:
а) снижением содержания мочевины в крови и моче
б) снижением содержания мочевины в крови и повышением в моче
в) повышением показателей мочевины в крови и моче
г) увеличением содержания мочевины в крови; снижением мочевины и ростом аммонийных солей в моче
д) увеличением содержания мочевины в крови; снижением мочевины и аммонийных солей в моче
ВыбЕрИтЕ правильнЫЙ ответ.
Патология печени сопровождается:
а) повышением содержания мочевины в крови и понижением в моче
б) снижением содержания мочевины в крови и нарастанием в моче
в) снижением мочевины в крови, снижением мочевины и аммонийных солей в моче
г) снижением содержания мочевины в крови и моче, ростом аммонийных солей в моче
д) ростом мочевины в крови и моче
ВыбЕрИтЕ ВСЕ правильныЕ ответЫ.
Содержание аммонийных солей в моче может нарастать при:
Выберите ВСЕ правильнЫе ОТВЕТы.
Глюкозо-аланиновый цикл включает процессы :
а) переаминирования глутаминовой кислоты с ПВК
б) превращения глутаминовой кислоты в глутамин
в) транспорта аммиака в печень в виде аланина
г) транспорта ПВК в печень в виде аланина
д) переаминирования аланина в печени с a-кетоглутаровой кислотой
Значение глюкозо-аланинового цикла заключается в том, что в виде аланина из мышц одновременно выводятся два токсических продукта обмена: ____________ и __________, также поддерживается безопасный уровень __________ в крови.
ВыбЕрите все правильные ответы.
Реакциями первичного обезвреживания аммиака являются:
а) синтез аммонийных солей
в) восстановительное аминирование a-кетоглутаровой кислоты
г) декарбоксилирование глутамина
Первой реакцией орнитинового цикла является синтез ____________. Фермент, катализирующий реакцию — ______________.
Последней реакцией орнитинового цикла является гидролиз ________ с образованием ___________ и ______________.
(для каждого вопроса – один правильный ответ, каждый ответ может быть использован один раз или не использован совсем)
| Метаболиты: | Процессы, в ходе которых данные метаболиты образуются: |
| 1) мочевина 2) мочевая кислота 3) ГЛН, АСН 4) индикан | а) обезвреживание продуктов гниения б) обмен пуриновых оснований в) обмен пиримидиновых оснований г) орнитиновый цикл д) процессы первичного обезвреживания аммиака |
ОТВЕТЫ по теме: “ОБЕЗВРЕЖИВАНИЕ АММИАКА. ОСТАТОЧНЫЙ АЗОТ КРОВИ”
5.1аг 2б 3в
7.1авг 2б 3д
12. ПВК аммиак глюкозы
14. карбамоилфосфата, карбамоилфосфатсинтаза
15. аргинина, мочевины, орнитина
16. 1г, 2б, 3д, 4а
1. Тема 24. Возможные нарушения белкового обмена при действии факторов внешней среды и различных патологических состояниях
Самостоятельная работа студентов в аудиторное время
Место проведения — кафедра биохимии
Продолжительность занятия — 180 минут
2. Цель занятия:Научить студентов оценивать нарушения обмена белков путем решения ситуационных задач, используя литературу по предложенной теме.
3. Конкретные задачи:
3.1.2. Витамины и их биологическая роль.
3.1.3. Ферменты и механизм их ингибирования.
3.2.1. Анализировать, обобщать, излагать литературный материал для решения ситуационной задачи.
3.2.2. Интерпретировать данные биохимических и других лабораторных исследований для оценки нарушений белкового обмена.
4. Мотивация:знания и навыки, полученные на занятии, развивают аналитическое мышление и могут быть использованы в практической работе для контроля состояния здоровья людей при воздействии факторов внешней среды и нарушении обмена белков.
5. Задание для самоподготовки:студенты должны проработать рекомендуемую литературу, используя вопросы для самоподготовки.
5.1.1. Лекционный материал по теме: «Обмен простых белков».
5.1.2. Березов Т.Т., Коровкин Б.Ф. «Биологическая химия» М., Медицина. — 1998. – С.220-228, 409-468, 568-572, 580-582, 619-624, 658-659.
5.1.3. Биохимия: Учебник / Под ред. Е.С.Северина. – М.; ГЭОТАР-МЕД, 2003. – С.468, 502-504, 509-512, 529-531.
5.2. Подготовиться к тестовому контролю
6. Вопросы для самоподготовки:
6.1. Источники и пути использования аминокислот в организме.
6.2. Суточная потребность белков, виды азотистого баланса.
6.3. Какие витамины участвуют в промежуточном обмене аминокислот?
6.4. Каким образом и в каких органах происходит конечное обезвреживание аммиака в организме?
6.5. Каким путем удаляются из организма конечные продукты
6.6. Какие азотсодержащие компоненты присутствуют в крови и в моче?
6.7. Как изменяется количество азотсодержащих компонентов в крови и в моче при заболеваниях печени, почек и мышц?
6.8. Какие нарушения обмена индивидуальных аминокислот вам
известны? Какова причина нарушения обмена аминокислот?
6.9. Какие нарушения белкового обмена наблюдаются при действии солей тяжелых металлов?
6.10. Какие нарушения белкового обмена наблюдаются при действии гидразина?
6.11. Какие нарушения белкового обмена наблюдаются при действии этиленгликоля, дихлорэтана и др. химических агентов?
источник