Определение концентрации мочевины в крови широко используется в диагностике, применяется для оценки тяжести патологического процесса, для наблюдения за течением заболевания и оценки эффективности проводимого лечения. Однако не следует забывать, что на уровень мочевины в крови могут влиять не только патологические, но и физиологические факторы (характер питания, физическая нагрузка и т. д.), а также прием лекарственных препаратов. Уровень мочевины может изменяться как в сторону повышения, так и снижения. При физиологических процессах степень отклонения уровня мочевины от нормы, как правило, незначительна, в то время как при патологии наблюдаются значительные сдвиги, причем степень изменения уровня мочевины зависит от тяжести патологического процесса.
Концентрация мочевины в сыворотке крови здоровых взрослых людей составляет 2,5 — 8,3 ммоль/л (660 мг/л). У женщин, по сравнению со взрослыми мужчинами, концентрация мочевины в сыворотке крови обычно ниже. У пожилых людей (старше 60 лет) наблюдается некоторое увеличение концентрации мочевины в сыворотке крови (примерно на 1 ммоль/л по сравнению с нормой здоровых взрослых людей), что обусловлено снижением у пожилых способности почек концентрировать мочу.
У детей уровень мочевины ниже, чем у взрослых, однако у новорожденных в первые 2 — 3 дня содержание ее может достигать уровня взрослого (проявление физиологической азотемии, обусловленной повышенным катаболизмом на фоне недостаточного поступления жидкости в первые 2 — 3 сут жизни и низкого уровня клубочковой фильтрации). В условиях гипертермии, эксикоза цифры мочевины могут возрасти еще больше. Нормализация наступает к концу первой недели жизни. Уровень мочевины в крови у недоношенных 1 нед. — 1,1 — 8,9 ммоль/л (6,4 — 63,5 мг/100 мл), у новорожденных — 1,4 — 4,3 ммоль/л (8,6 — 25,7 мг/100 мл), у детей после периода новорожденности — 1,8 — 6,4 ммоль/л (10,7 — 38,5 мг/100 мл).
Повышение уровня мочевины в крови наблюдается при:
- употреблении в пищу чрезмерного количества белка (в результате усиленного синтеза мочевины);
- диете, бедной ионами хлора (компенсаторная, приспособительная реакция, направленная на поддержание коллоидно-осмотического давления крови);
- обезвоживании организма: неукротимая рвота, профузный понос и т. д. (вследствие усиленной пассивной реабсорбции в почечных канальцах);
- приеме некоторых лекарственных препаратов: сульфаниламидов, левомицетина, тетрациклина, гентамицина, фуросемида, изобарина, допегита, невиграмона, лазикса, анаболических стероидов, кортикостероидов, тироксина в большом количестве;
- чрезмерном катаболизме белка: лейкозе, паренхиматозной желтухе, тяжелых инфекционных заболеваниях, непроходимости кишечника, ожоге, дизентерии, шоке;
- нарушении выведения мочевины, связанного с заболеваниями почек и мочевыводящих путей: хронические заболевания почек (гломерулонефрит, пиелонефрит); обструкции мочевыводящих путей (опухоли мочевыводящих путей, предстательной железы, почечно-каменная болезнь); острая и хроническая почечная недостаточность;
- нарушении выведения мочевины при заболеваниях и состояниях, не связанных с заболеваниями почек и мочевыводящих путей: недостаточность деятельности сердца, острый инфаркт миокарда; сахарный диабет с кетоацидозом, аддисонова болезнь и другие заболевания.
Повышение уровня мочевины в крови, связанное с ее усиленным образованием или снижением ее фильтрации в почках в результате нарушения гемодинамики, как правило, не достигает больших значений, содержание мочевины обычно не превышает 13 ммоль/л.
Большие значения уровня мочевины в крови наблюдаются при заболеваниях почек. Так, концентрация мочевины в плазме крови пациентов с хронической почечной недостаточностью может достигать 40,0 — 50,0 ммоль/л. Особенно высокое содержание мочевины (49,8 — 81,0 ммоль/л и выше) наблюдается при острой почечной недостаточности. При этом резко снижается выделение мочевины с мочой. Однако, следует заметить, что увеличение содержания мочевины не является ранним признаком нарушения функции почек. Установлено, что первоначально возрастает уровень мочевой кислоты, а затем мочевины и креатинина, что является угрожающим симптомом. При различных заболеваниях почек степень повышения содержания мочевины определяется характером повреждения нефрона, уровнем интоксикации, усиленным распадом белка в ткани (в связи с ограничением белка в пище почечных больных) и другими факторами. Повышение содержания мочевины в крови до 16,0 ммоль/л сочетается с нарушением функции почек средней тяжести, до 33,2 ммоль/л — тяжелым, свыше 49,8 ммоль/л — очень тяжелым нарушением с неблагоприятным прогнозом.
Увеличение содержания мочевины в крови, сопровождающееся синдромом интоксикации, называется уремией. Обычно считается, что мочевина не токсична и что сопровождающий увеличение ее содержания синдром интоксикации обусловлен накоплением в организме других продуктов. Вместе с тем следует иметь ввиду, что мочевина, относительно легко проходя через плазматические мембраны клеток, будучи осмотически активным веществом, увлекает в клетки паренхиматозных органов и воду. Это приводит к увеличению объема клеток (клеточной гипергидратации) и нарушению их функционального состояния.
Уменьшение содержания мочевины в крови наблюдается редко:
- при беременности (вследствие физиологической гидремии);
- при диете с низким содержанием белка и высоким содержанием углеводов, голодании;
- при парентеральном введение жидкостей (вследствие гипергидратации);
- после гемодиализа;
- при пониженном катаболизме белков;
- при приеме СТГ;
- при нарушении всасывания в кишечнике, целиакии;
- при повышенной утилизации белка (в поздние сроки беременности, у детей до 1 года, при акромегалии);
- при врожденной недостаточности или отсутствии ферментов, участвующих в орнитиновом цикле мочевинообразования;
- при особенно тяжелых поражениях печени (печеночная недостаточность), вызванных, в частности, отравлением фосфором, мышьяком и другими гепатотропными ядами; остром некрозе печени, печеночной коме, декомпенсированном циррозе, гепатитах (известно, что печень обладает большими функциональными резервами, способность ее к дезаминированию и синтезу мочевины сохраняется при исключении из процессов обмена до 85% ее ткани).
- Цыганенко А. Я., Жуков В. И., Мясоедов В. В., Завгородний И. В. — Клиническая биохимия — Москва, «Триада-Х», 2002 г.
- Слепышева В. В., Балябина М. Д., Козлов А. В. — Методы определения мочевины
- Клиническая оценка лабораторных тестов — под редакцией Н. У. Тица — Москва, «Медицина», 1986 г.
- Камышников В. С. — Карманный справочник врача по лабораторной диагностике — Москва, МЕДпресс-информ, 2007 г.
- Маршалл Дж. — Клиническая биохимия — Москва, Санкт-Петербург, «Бином», «Невский Диалект», 2000 г.
Определение концентрации мочевины в моче проводится значительно реже, чем определение уровня мочевины в крови и используется обычно при при обнаружении повышенного уровня мочевины в крови и решении вопроса о состоянии выделительной функции почек. При этом определяют суточную экскрецию мочевины с мочой. Повышенное содержание мочевины крови при снижении суточной экскреции с мочой чаще свидетельствует о нарушении азотовыделительной функции почек.
Раздел: Клиническая биохимия
Мочевина является главным конечным продуктом обмена аминокислот. Синтезируется мочевина из аммиака, который постоянно образуется в организме при окислительном и неокислительном дезаминировании аминокислот, при гидролизе амидов глутаминовой и аспарагиновой кислот, а также при распаде пуриновых и пиримидиновых нуклеотидов.
Раздел: Клиническая биохимия
Определение мочевины используется для диагностики, определения прогноза и тяжести течения заболевания, а также для контроля за лечением. Определение мочевины в клинико-диагностических лабораториях проводится различными методами, однако все их многообразие можно разделить на три основные группы.
Раздел: Клиническая биохимия
Фотометрические методы определения мочевины основаны на реакции мочевины с различными веществами с образованием окрашенных соединений. Среди фотометрических методов определения мочевины наиболее распространенными являются методы, основанные на реакции мочевины с диацетилмонооксимом.
Раздел: Клиническая биохимия
Появление глюкозы в моче называется глюкозурией. Глюкозурия обычно сопровождается полиурией при повышении осмолярности мочи, поскольку глюкоза — осмотически активное вещество. Между степенью глюкозурии и полиурии обычно наблюдается параллелизм.
Раздел: Анализ мочи
источник
Реактивы. Цветной реактив*; мочевина, стандартный раствор 1 г/л, или 16,65 ммоль/л; набор «Уреатест».
Оборудование. Штатив с пробирками; пипетки вместимостью 0,1, 2 и 5 мл; алюминиевая фольга; водяная баня; ФЭК.
Моча, собранная за сутки, профильтрованная и разведенная перед анализом водой в 25 раз.
а. Определение содержания мочевины в сыворотке крови. Метод основан на способности мочевины в присутствии тиосемикарбазида и солей железа в сильнокислой среде образовывать с диацетилмонооксимом соединение красного цвета, интенсивность окраски которого пропорциональна содержанию мочевины в исследуемой жидкости.
Ход определения. В опытную пробирку отмеривают 0,1 мл разведенной в 10 раз сыворотки крови, в стандартную – такой же объем стандартного раствора мочевины и в контрольную – 0,1 мл дистиллированной воды. Добавляют во все пробирки по 2 мл цветного реактива и тщательно перемешивают их содержимое встряхиванием.
Все пробирки закрывают крышечкой из алюминиевой фольги и нагревают в кипящей водяной бане в течение 10 мин (точно!). Затем охлаждают их под струей холодной воды.
Измеряют экстинкцию стандартной и опытной проб против контрольной на ФЭКе при 540-560 нм (светофильтр зеленый) в кювете с толщиной слоя 0,5 см.
Примечание. Окраска неустойчива, поэтому измерение необходимо провести в течение 15 мин.
Расчет. Содержание мочевины х (ммоль/л) в сыворотке крови рассчитывают по формуле
где Еоп – экстинкция опытной пробы против контрольной;
Ест – экстинкция стандартной пробы против контрольной;
16,65 – концентрация мочевины в стандартной пробе, ммоль;
Азот мочевины (в ммоль/л) рассчитывают, разделив полученное значение содержания мочевины в сыворотке на 2,14 (число, выражающее отношение молекулярной массы азота мочевины к массе всей молекулы мочевины).
б. Определение содержания мочевины в моче. Принцип метода тот же, что и в предыдущей работе.
Ход определения. Для анализа используют 0,1 мл разведенной мочи и 0,1 мл стандартного раствора мочевины и обрабатывают эти пробы так же, как и сыворотку крови.
Расчет проводят по формуле
где х – количество мочевины, ммоль/сут;
1,665 – содержание мочевины в 0,1 мл стандартной пробы, мкмоль;
Ест – экстинкция стандарта;
0,1 – объем мочи, взятый на исследование, мл;
1000 – коэффициент пересчета мкмоль в ммоль.
в. Определение содержания мочевины в сыворотке крови экспресс-методом с помощью набора «Уреатест». Метод основан на способности уреазы разлагать мочевину с образованием аммиака, который окрашивает полоску реактивной хроматографической бумаги в голубой цвет. Высота окрашенной зоны пропорциональна концентрации мочевины, которую рассчитывают по калибровочному графику.
Ход определения. Сыворотку крови разводят водой в отношении 1:1. На пропитанный ферментом конец бумажной полоски в 3 мм от красной парафиновой полосы наносят специальной пипеткой 0,03 мл разведенной сыворотки крови. Полоску тотчас помещают в чистую сухую пробирку, герметически закрывают ее пробкой и ставят в термостат при 37˚С. Через 20 минут полоску извлекают, измеряют высоту окрашенной в голубой цвет зоны.
Расчет. По калибровочному графику, входящему в набор «Уреатест», находят концентрацию мочевины в сыворотке крови.
Оформление работы. Сделать расчет содержания мочевины и азота мочевины в исследуемой сыворотке и моче. В выводе отметить возможные изменения в азотном обмене.
Практическое значение работы. В норме содержание мочевины в сыворотке крови человека составляет 3,0-7,0 ммоль/л, а азота мочевины – 1,2-3,7 ммоль/л. Содержание мочевины в сыворотке крови значительно колеблется в зависимости от приема белков с пищей. Повышение уровня мочевины в крови (азотемия) отмечается при заболеваниях почек (когда нарушена их выделительная функция), при усиленном распаде белков, избыточном белковом питании, а также в случае обезвоживания организма (в данном случае имеет место относительная, а не абсолютная форма азотемии). Снижение уровня мочевины в крови и выделения ее с мочой (в сутки в норме выделяется 333-582,8 ммоль/сут) наблюдается при заболевании печени (паренхиматозная желтуха, дистрофия печени, цирроз), что связано с нарушением мочевинообразовательной функции.
С мочой у взрослого человека выделяется за сутки 20-35 г, или 333-583 ммоль мочевины. Мочевина – диамид угольной кислоты, образующийся в печени при обезвреживании аммиака. В норме в сыворотке крови содержится 3,33-8,32 ммоль/л мочевины.
Принцип метода. Мочевина образует с диацетилмонооксимом в присутствии тиосемикарбазида и солей железа в кислой среде окрашенные соединения. Интенсивность окраски прямо пропорциональна концентрации мочевины в исследуемой моче и сыворотке крови и определяется фотометрически.
Исследуемый материал: сыворотка крови, моча.
Реактивы:стандартный раствор мочевины (16,7 ммоль/л). 5%-ный раствор хлорного железа (основной раствор: 5 г хлорного железа доводят до 100 мл водой, после чего подкисляют 1 мл концентрированной H2SO4; рабочий раствор готовят из основного: 1 мл основного раствора доводят до объема 100 мл дистиллированной водой, добавляют 8 мл концентрированной H2SO4 и 1 мл 85%-ной ортофосфорной кислоты; раствор хранят в темной посуде). 2,5%-ный водный раствор диацетилмооксима, 0,25%-ный раствор тиосемикарбазида (хранят в темной посуде). Цветной реактив хлорида (готовят каждый раз перед употреблением): к 30 мл рабочего раствора хлорного железа добавляют 20 мл дистиллированной воды, 1 мл 2,5%-ного диацетилмооксима и 0,25 мл 0,25%-ного тиасемикарбазида).
Оборудование: пипетки, пробирки, ФЭК, кюветы с длиной оптического
ХОД РАБОТЫ. Мочу перед определением развести в 10 раз. В одну пробирку вносят 0,1 мл мочи, в другую – 0,1 мл сыворотки крови, в третью – стандартный раствор мочевины. Затем во все 3 пробирки добавляют по 2 мл рабочего раствора для определения мочевины, перемешивают и ставят на кипящую водяную баню на 10 мин. Затем пробирки охлаждают в струе холодной воды и колориметрируют на зеленом светофильтре в кювете с длиной оптического пути 5 мм против воды.
Расчет производят по формуле:
Клинико-диагностическое значение. Пониженное содержание мочевины в моче отмечается при нефрите, ацидозе, паренхиматозной желтухе, циррозе печени, уремии, повышенное – при недостатке белка в питании, злокачественной анемии, лихорадке, интенсивном распаде белков в организме, после приемов салицилатов, при отравлении фосфором.
Снижение содержания мочевины в сыворотке крови отмечается при паренхиматозном гепатите, циррозе (резкое снижение мочевинообразовательной функции печени), во время беременности, при эклампсии. Содержание мочевины в сыворотке может повышаться при нефритах, лихорадочных состояниях, сепсисе, туберкулезе почек.
Мочевинаявляется основной фракцией остаточного азота, определение которой используется в диагностических целях. Синтез ее происходит в печени из аммиака, который образуется при дезаминировании аминоктислот, распада пуриновых и пиримидиновых нуклеотидов.
Отклонения от нормального содержания мочевины в сыворотке крови зависит от скорости процессов синтеза мочевины и ее выделения. Увеличение содержания мочевины в сыворотке крови является одним из главных признаков нарушения почек. Из фракций остаточного азота раньше всего повышается уровень мочевины. При почечной недостаточности азот мочевины может составлять до 90% фракций остаточного азота.
Повышение уровня мочевины сыворотки крови может носить и внепеченочный характер: при потере жидкости, при усиленном распаде белков (острая атрофия печени, тяжелые печени) из-за нарушения синтеза мочевины в печени.
Принцип метода: Мочевина под действием уреазы разлагается с образованием аммиака и углекислого газа. Для уреазы мочевина является единственным субстратом, поэтому уреазные методы высокоспецифичны. Выделившийся аммиак образует с гипохлоритом натрия и фенолом окрашенный продукт – индофенол (синего цвета). Интенсивность окраски пропорциональна содержанию мочевины.
2. Этилендиамин-N (N-тетрауксусной кислоты динатриевая соль).
3 ЭДТА – буфер рН 6,5: 0,6 г трилона В растворяют в 30-40 мл воды, доводят до рН 6,5 раствором едкого натра и доливают водой до 50 мл.
4. Основной раствор уреазы в буфере: 20 мг уреазы растворяют в 10 мл буфера.
5. Рабочий раствор уреазы — перед началом определения берут необходимое количество основного раствора и разводят бидистиллированной водой в отношении 1:4.
7. Натрия нитропруссид 2-водный.
8. Цветной реактив: фенол – 0,11 моль/л, нитропруссид натрия – 0,18 моль/л: 0,0263 г нитропруссида натрия помещают в мерную колбу на 500 мл, приливают примерно 300 мл воды, растворяют при перемешивании. Затем добавляют 5,18 г фенола и доливают водой до метки.
9. Натр едкий 1 моль/л; 0,26 моль/л.
10. Гипохлорид натрия:10 г хлорной извести размешивают в течение 15 минут с 17 мл воды, затем добавляют раствор, состоящий из 17 мл воды и 7 г карбоната натрия. Масса сначала густеет, а затем разжижается. Надосадочную жидкость сливают и фильтруют через промытый водный фильтр. Как только раствор приобретает слабо желтую окраску, добавляют 10 капель 1%-ного раствора крахмала и титруют до обесцвечивания.
11. Основной раствор гипохлорита натрия разводят водой так, чтобы концентрация хлора составляла 0,78 г/л, смешивают с равным объемом 0,26 моль/л раствором едкого натрия (100мл+100мл).
13. Бензойная кислота, 2 г/л (кислоту растворяют при нагревании).
14. Калибровочный раствор мочевины, 0,5 ммоль/л: 15 мг мочевины растворяют в мерной колбе на 500 мл в 2 г/л растворе бензойной кислоты.
Ход определения: Перед определением сыворотку разводят 0,154 моль/л раствором хлорида натрия в отношении 1:9.
Опытная проба: 100 мкл рабочего раствор уреазы вносят в пробирку, добавляют 20 мкл разведенной сыворотки. Закрывают пробкой, перемешивают и инкубируют в течение 15 минут при 37 °С. После инкубации добавляют 300 мкл цветного реактива и 300 мкл рабочего раствора гипохлорита натрия. Перемешивают и инкубируют в течение 20-30 минут при 37 °С. Измеряют экстинкцию в кювете с толщиной слоя 1 см при длине волны 500-560 нм (зеленый светофильтр) против холостой пробы.
Холостую пробу обрабатывают так же, как опытную, но вместо сыворотки берут 0,154 моль/л раствор.
Калибровочную пробу обрабатывают так же, как опытную, но вместо сыворотки берут калибровочный раствор мочевины. Измеряют при тех же условиях против холостой пробы.
Количество мочевины, ммоль/л = ——— х 0,5 х 10
Где Еоо — экстинкция опытной пробы, Ек – экстинкция калибровочной пробьы: 0,5 — концентрация мочевины в калибровочном растворе ммоль/л, 10 – коэффициент разведения.
Нормальные величины. Сыворотка крови – 2, 5-8,3 ммоль/л , или 20-50 мг/100мл.
Количественное определение витамина С в сыворотке крови. стр11
Коагуляционная проба Вельтмана. стр12
Определение общего гемоглобина методом щелочной денатурации. стр12
Определение билирубина методом Иедрашека. стр13
Определение кальция, фосфора в сыворотке крови титрометрическим методом
с применением мурексида. стр14
Качественные реакции на неорганические и органические составные части мочи. стр14
Определение белка слюны биуретовым методом. стр15
Количественное определение активности амилазы слюны. стр16
Определение активности щелочной фосфатазы слюны. стр16
Определение трансаминазной активности слюны. стр17
Определение кальция в слюне титрометрическим методом с применением мурексида. стр18
1.Калориметр включить в сеть за 15 мин. до начала измерений. Во время прогрева кюветное отделение должно быть открыто (при этом шторка перед фотоприемниками перекрывает световой пучек).
2. Установить необходимый светофильтр. При переключении светофильтров ручка «чувствительность» должна находится в положении «1» (красный светофильтр 670- «1», зеленый светофильтр 540- «1»), а ручка «установка 100 Грубо» в крайнем левом положении (это предохраняет прибор от перегрузки и порчи).
3. В световой поток поместить кювету с контрольным раствором по отношению к которому производят измерения.
4. Во вторую ячейку кюветодержателя поместить кювету с исследуемым раствором.
5. Закрыть крышку кюветного отделения.
6. Ручка ЧУВСТВИТЕЛЬНОСТЬ и УСТАНОВКА 100 вначале ГРУБО, затем ТОЧНО установить отсчет 100 по шкале калориметра.
7. Поворотом ручки под кюветным отделением до упора, ввести в световой поток кювету с исследуемым раствором.
8. Снять отсчет по шкале Д в единицах оптической плотности.
ОБОСНОВАНИЕ ВЫПОЛНЕНИЯ РАБОТЫ. Мочевина — продукт, образующийся в печени при обезвреживании аммиака. Мочевина — основной конечный продукт обмена белков. Примерно 50 % небелкового, остаточного азота крови приходится на долю мочевины.
ПРИНЦИП МЕТОДА: мочевина образует с диацетилмонооксимом в сильнокислой среде в присутствии тиосемикарбазида и ионов трехвалентного железа комплексное соединение красного цвета, по интенсивности окраски которого определяют ее концентрацию.
ХОД РАБОТЫ: взять три пробирки: опыт, стандарт, контроль.
источник
(диацетилмонооксимный метод)
ОБОСНОВАНИЕ ВЫПОЛНЕНИЯ РАБОТЫ. Мочевина — продукт, образующийся в печени при обезвреживании аммиака. Мочевина – основной конечный продукт обмена белков. Примерно 50% небелкового, остаточного азота крови приходится на долю мочевины.
ПРИНЦИП МЕТОДА: мочевина образует с диацетилмонооксимом в сильнокислой среде в присутствии тиосемикарбазида и ионов трехвалентного железа комплексное соединение красного цвета, по интенсивности окраски которого определяют ее концентрацию.
ХОД РАБОТЫ: взять три пробирки: опыт, стандарт, контроль.
| ОТМЕРИТЬ | ОПЫТ | СТАНДАРТ | КОНТРОЛЬ |
| Рабочий раствор Сыворотка крови Дистилл. вода Стандартный раствор мочевины (16,65 ммоль/л) | 2,0 мл 0,1 мл — — | 2,0 мл — — 0,1 мл | 2,0 мл — 0,1 мл — |
Все пробирки поместить в водяную баню при температуре 100 о С в течение 5 минут.
Охладить и произвести измерение экстинкции против контроля при 500-560 нм; кювета 5 мм. Измерения проводят в пределах 15 минут.
КОНЕЧНЫЙ РЕЗУЛЬТАТ: рассчитывают по формуле:
Соп = —— ·16,65 = ммоль/л.
Нормальное содержание мочевины в сыворотке крови у взрослых 2,5 — 8,33 ммоль/л; в моче 333 — 582 ммоль/сут. У новорожденных в сыворотке крови нормальное содержание мочевины составляет 3,5 – 11 ммоль/л, у детей 2-14 лет 2,5 – 8,33 ммоль/л.
Незначительное повышение концентрации мочевины в сыворотке крови наблюдается при избыточном питании белковыми продуктами, при старении.
Значительное увеличение концентрации мочевины в сыворотке крови (уремия) наблюдается при почечной недостаточности, обезвоживании (рвота, понос), шоке, усиленном распаде белков, сепсисе.
Пониженное содержание мочевины в сыворотке крови отмечается при паренхиматозном гепатите, циррозе (резкое снижение мочевинообразовательной функции печени), эклампсии, во время беременности.
Пониженное содержание мочевины в моче отмечается при нефрите, ацидозе, паренхиматозной желтухе, циррозе печени
ЗАНЯТИЕ № 31
САМОСТОЯТЕЛЬНАЯ АУДИТОРНАЯ РАБОТА
ПО ТЕМЕ «ОБМЕН И ФУНКЦИИ АМИНОКИСЛОТ. ОБМЕН НУКЛЕОТИДОВ»
Задания для самостоятельной работы:
1. 1.Составить метаболическую карту аминокислотного обмена.
2.1. Источники аминокислот в тканях.
2.2. Пути превращения аминокислот в тканях.
2.3. Регуляторные ферменты гликолиза, метаболизма гликогена, глюконеогенеза, пентозофосфатного пути.
2.4. Витаминзависимые ферменты.
3. Решение и обсуждение ситуационных задач.
ЗАНЯТИЕ № 33
РАБОТА № 1. КАЧЕСТВЕННОЕ И КОЛИЧЕСТВЕННОЕ ОПРЕДЕЛЕНИЕ БИЛИРУБИНА
(ПО МЕТОДУ ЙЕНДРАШИКА)
ОБОСНОВАНИЕ ВЫПОЛНЕНИЯ РАБОТЫ. При разрушении эритроцитов (у человека через 100-120 дней) в клетках ретикулоэндотелиальной системы костного мозга, селезенки, печени происходит распад гемоглобина. Конечным продуктом распада гема является непрямой билирубин, который поступает в кровь и транспортируется альбуминами в печень, где происходит его обезвреживание с образованием прямого билирубина.
В сыворотке крови имеется два вида билирубина. Основная форма — это непрямой (свободный) билирубин, который не связан с глюкуроновой кислотой и дает непрямую диазореакцию. В крови содержится незначительное количество прямого (связанного) билирубина — этот билирубин связан с глюкуронатом и дает прямую диазореакцию. Сумма обоих пигментов дает общий билирубин.
Нарушение обмена билирубина сопровождается развитием желтухи. В связи с этим раздельное количественное определение общего, прямого и непрямого билирубина в сыворотке крови имеет значение для дифференциальной диагностики различных типов желтух.
ПРИНЦИП МЕТОДА: диазореактив дает с прямым билирубином розовое окрашивание. Непрямой билирубин переводят в растворимое состояние добавлением к сыворотке кофеинового реактива, после этого общий билирубин определяется диазореакцией. Интенсивность окраски прямо пропорциональна концентрации билирубина в пробе.
ХОД РАБОТЫ: взять три пробирки: опыт 1, 2 и контроль.
| ОТМЕРИТЬ | ОПЫТ1 | ОПЫТ2 | КОНТРОЛЬ |
| ПРЯМОЙ БИЛИРУБИН | ОБЩИЙ БИЛИРУБИН | ||
   СЫВОРОТКА КРОВИ NaCl 0,9% ДИАЗОРЕАКТИВ КОФЕИНОВЫЙ РЕАКТИВ СЫВОРОТКА КРОВИ NaCl 0,9% ДИАЗОРЕАКТИВ КОФЕИНОВЫЙ РЕАКТИВ | 0,5 мл 1,75 мл 0,25 мл | 0,5 мл 0,25 мл 1,75 мл | 0,5 мл 0,25 мл 1,75 мл |
Содержимое пробирок перемешать и инкубировать


ОПЫТ2 — фотометрия через 20 минут
Длина волны: 530-550 нм, кювета 5 мм.
КОНЕЧНЫЙ РЕЗУЛЬТАТ: находят по калибровочному графику. По разнице между количеством общего и прямого билирубина определяют уровень непрямого билирубина.
Нормальное содержание общего билирубина в сыворотке крови у взрослых 5,0 — 20,5 мкмоль/л; связанного билирубина (прямого) – 1,0 — 7,5 мкмоль/л; свободного билирубина (непрямого) – 1,7 — 17,1 мкмоль/л.
У новорожденных нормальное содержание общего билирубина в сыворотке крови составляет 12 – 20 мкмоль/л, у детей 2-14 лет 8,55 – 20,52 мкмоль/л.
Повышенное содержание общего билирубина в сыворотке крови отмечается при желтухе новорожденных, повреждении гепатоцитов (воспалительном, токсическом), закупорке желчных протоков, гемолитической болезни.
При паренхиматознойжелтухе:
— в крови повышается содержание прямого и непрямого билирубина;
— в моче появляется прямой билирубин и уробилиноген.
— уменьшается выделение стеркобилина с калом.
При обтурационной (механической) желтухе:
— в крови повышается содержание прямого билирубина;
— в моче появляется прямой билирубин (темная моча);
— отсутствует выделение стеркобилина (ахолический кал).
При гемолитической желтухе:
— в крови повышается содержание непрямого билирубина;
— в моче повышается содержание стеркобилиногена;
— увеличивается выделение стеркобилина (темный кал).
источник
Инструкция по применению набора реагентов для количественного определения содержания мочевины в сыворотке или плазме крови и моче человека, ферментативным УФ-кинетическим методом «Мочевина-УФ — UTS»
по применению набора реагентов для количественного определения содержания мочевины в сыворотке или плазме крови и моче человека ферментативным методом
Набор «МОЧЕВИНА – UTS» разрешен к производству, продаже и применению на территории РФ.
Регистрационное удостоверение № ФСР 2009/05467
Информация для заказа набора «МОЧЕВИНА – UTS»
Р1 (2 мл) + Р2 (50 мл) + Р3 (50 мл) +калибратор (1мл)
Р1 (2*4 мл) + (2*100 мл)+ Р3 (2*100 мл) + калибратор (2*2мл)
*v – объем фотометрической ячейки анализатора.
ВНИМАНИЕ! Изменено соотношение компонентов набора. Рабочий реагент готовить смешиванием Реагента 1 (Р1) и Реагента 2 (Р2) в соотношении 1 : 24.
1.1. Набор реагентов «МОЧЕВИНА — UTS» предназначен для определения активности мочевины в сыворотке или плазме крови и моче человека в клинико-диагностических и биохимических лабораториях для целей диагностики заболеваний и контроля проводимого лечения пациентов.
1.2. Мочевина является конечным продуктом метаболизма белков в организме. Она синтезируется в печени из аммиака, который образуется при дезаминировании аминокислот. Определение мочевины в сыворотке или моче является важным показателем функции почек. Повышение уровня мочевины в сыворотке (азотомия) может быть связано с ухудшением ренальной функции или при диетах с потреблением большого количества белковой пищи, снижение уровня мочевины наблюдается при низкобелковой или высокоуглеводной диетах, при беременности [1,4,5]. На этом основано клиническое значение анализа.
1.3. Потенциальный риск применения набора – класс 2а. Основной риск косвенный и связан с возможностью получения ложного результата анализа, что может привести к неправильно поставленному диагнозу и назначению неэффективного лечения пациента. Для снижения указанного риска необходимо в каждой аналитической серии наборов реагентов контролировать качество результатов анализов с применением контрольных сывороток в соответствии с ОСТ 91500.13..
2.1. МОЧЕВИНА (NH2CONH2) в анализируемом образце ферментативно под действием уреазы гидролизуется в ион аммония (NH4+) и углекислый газ (CO2) (1). Образовавшиеся ионы аммиака вступают в реакцию с салицилатом и гипохлоритом в присутствии катализатора нитропруссида Na c образованием окрашенного соединения индофенола зеленого цвета (2) – метод Бертло.


2.2. Фотометрическое измерение основано на наличии пика поглощения молекулами индофенола [1,2,3]. Таким образом, увеличение оптической плотности реакционной смеси пропорционально интенсивности окраски индофенола при (580-630) нм и, следовательно, прямо пропорционально содержанию мочевины в анализируемом образце.
3.1. Поскольку рабочий реагент, содержащий все компоненты для обеспечения химических реакций (1 и 2) не стабилен, набор реагентов «МОЧЕВИНА-UTS» поставляется в виде трех реагентов Р1, Р2, Р3 и раствора калибратора.
источник
Принцип метода. Диацетилмонооксим в кислой среде и в присутствии тиосемикарбазида и ионов трехвалентного железа образует с мочевиной красный комплекс.
Смешать реактивы, на 10 минут поместить в кипящую водяную баню все три пробирки, предварительно закрыв их отверстие фольгой. Затем быстро охлаждают все пробирки водой и колориметрируют при длине волны 490-540 нм опытную и калибровочную пробы против контроля в кюветах толщиной 0,5 см. Формула для расчета:
Норма содержания мочевины в крови: 2,5-8,3 ммоль/л. Уровень мочевины в крови характеризует выделительную функцию почек.
Аммиак выделяется в моче в виде солей серной и фосфорной кислот. За счет аммиака у детей выделяется относительно больше азота, чем у взрослых.
Избыток аммиака в детской моче зависит от неполного превращения его в мочевину. Аммиак входит в состав солей серной и фосфорной кислот, образующихся при расщеплении белка и фосфорсодержащих органических соединений. У взрослого это осуществляется отчасти за счет щелочных земель (Na, К, Са, Mg), поступающих в достаточном количестве с пищей. Детский организм эти соли использует для пластических целей; кроме того, всасывание их в кишечнике несколько затруднено образованием мыл вследствие относительно большого содержания жира в пище ребенка.
Повышенное содержание аммиака в моче не говорит об ацидозе и ацидурии, а скорее об алкалопении, указывая на некоторый недостаток щелочей. У старших детей количество аммиака в моче зависит от характера пищи, главным образом от характера ее зольного остатка; при большом количестве овощей поступает много щелочей и, следовательно, меньше выделяется аммиака с мочой; при мясной пище, наоборот, больше образуется кислых продуктов межуточного обмена, нейтрализуемых аммиаком и выделяющихся с мочой в виде соответствующих соединений.
3. Роль липопротеинов низкой и высокой плотности (ЛПНП и ЛПВП) в обмене холестерина. Биохимические основы развития атеросклероза Количественное определение общего холестерина в сыворотке крови. Клиническое значение определения.
Липиды являются в основе своей гидрофобными молекулами, они транспортируются в водной фазе крови в составе особых частиц – липопротеинов. Такие транспортные липопротеины можно сравнить с орехом, который имеет скорлупу и ядро. Поверхность липопротеиновой частицы («скорлупа») гидрофильна и сформирована белками, фосфолипидами и свободным холестеролом. Триацилглицеролы и эфиры холестерола составляют гидрофобное ядро. Белки в липопротеинах обычно называются апобелками, выделяют несколько их типов – А, В, С, D, Е. В каждом классе липопротеинов находятся соответствующие ему апобелки, выполняющие структурную, ферментативную и кофакторную функции.
ЛП различаются по соотношению триацилглицеролов, холестерола и его эфиров, фосфолипидов и как сложные белки состоят из четырех классов.
липопротеины очень низкой плотности (ЛПОНП, пре-β-липопротеины, пре-β-ЛП),
липопротеины низкой плотности (ЛПНП, β-липопротеины, β-ЛП),
липопротеины высокой плотности (ЛПВП, α-липопротеины, α-ЛП).
Хиломикроны и ЛПОНП ответственны, в первую очередь, за транспорт жирных кислот в составе ТАГ. ЛП высокой и низкой плотности – за транспорт холестерола и жирных кислот в составе эфиров ХС.
Транспорт триацилглицеролов от кишечника к тканям (экзогенные ТАГ) осуществляется в виде хиломикронов (ХМ), от печени к тканям (эндогенные ТАГ) – в виде липопротеинов очень низкой плотности.В транспорте ТАГ к тканям можно выделить последовательность следующих событий:
1.Образование незрелых первичных ХМ в кишечнике. 2.Движение первичных ХМ через лимфатические протоки в кровь.
3.Созревание ХМ в плазме крови – получение белков апоС-II и апоЕ от ЛПВП. 4.Взаимодействие с липопротеинлипазой (ЛПЛ) эндотелия, которая отщепляет жирные кислоты от ТАГ. Жирные кислоты переходят непосредственно в данную ткань или, связываясь с альбумином, разносятся по организму. В результате количество ТАГ в хиломикроне резко снижается и образуются остаточные ХМ. 5.Переход остаточных ХМ в гепатоциты и полный распад их структуры. 6.Синтез ТАГ в печени из пищевой глюкозы. Использование ТАГ, пришедших в составе остаточных ХМ. 7.Образование первичных ЛПОНП в печени.
8.Созревание ЛПОНП в плазме крови – получение белков апоС-II и апоЕ от ЛПВП. 9.Взаимодействие с липопротеинлипазой эндотелия и потеря большей части ТАГ. Образование остаточных ЛПОНП (по-другому липопротеины промежуточной плотности, ЛППП). 10.Остаточные ЛПОНП переходят в гепатоциты и полностью распадаются, либо остаются в плазме крови. После воздействия на них печеночной ТАГ-липазы в синусоидах печени ЛПОНП превращаются в ЛПНП.
ЛП очень низкой плотности (пребеталипопротеиды): -синтезируются в печени из эндогенных и экзогенных липидов,
-в их составе преобладают ТАГ, около 40% от массы составляют белок, фосфолипиды и холестерол (8% белка, 60% ТАГ, 6% ХС, 12% эфиров ХС, 14% фосфолипидов), -основным белком является апоВ-100, выполняющий структурную функцию,
-в норме концентрация 1,3-2,0 г/л, -слабо атерогенны.
Функция: Транспорт эндогенных и экзогенных ТАГ от печени в ткани, запасающие и использующие жиры, т.е. в те же ткани, что и хиломикроны (в сутки в печни обр-ся от 20 до 50 г жира на экспорт)
Метаболизм: 1. Первичные ЛПОНП образуются в печени из пищевых жиров, достигающих гепатоцитов с остаточными хиломикронами, и новосинтезированных из глюкозы жиров, содержат только апоВ-100; 2. В крови первичные ЛПОНП взаимодействуют с ЛПВП и приобретают от них апоС-II и апоЕ, образуя зрелые формы. 3. Аналогично хиломикронам, на эндотелии капилляров ряда тканей зрелые ЛПОНП подвергаются воздействию липопротеинлипазы, которая находится на поверхности кл эндотелия сосудов с образованием свободных жирных кислот и глицерина. Жирные кислоты перемещаются в клетки органов и используются как Е материал, либо остаются в плазме крови и в комплексе с альбумином разносятся с кровью в другие ткани. 4. Остаточные ЛПОНП (также называемые липопротеины промежуточной плотности, ЛППП)
либо эвакуируются в гепатоциты посредством эндоцитоза, связанного с рецепторами к апоЕ и апоВ-100-белкам, либо после воздействия на них печеночной ТАГ-липазы (только в сосудах печени) превращаются в следующий класс липопротеинов – липопротеины низкой плотности (ЛПНП).
ЛП низкой плотности (ЛПНП или beta-липопротеипы): Образуются в крови. Состоят из 25% белка и 75% липидов. Главным компонентом является холестерин (примерно50%) в виде эфиров с линолевой кислотой и фосфолипиды. У здоровых людей до 2/3 всего холестерина плазмы находится в составе ЛПНП. Они являются главным поставщиком холестерина в ткани. ЛПНП регулируют синтез холестерина de novo. Большинство ЛПНП являются продуктами расщепления ЛПОНП липопротеидлипазой. На клеточных мембранах имеются рецепторы для ЛПНП, они взаимодействуют с апопротеинами ЛПНП. После узнавания проникают в клетки путем эндоцитоза, там распадаются под действием ферментов гидролаз в лизосомах. Освободившийся холистерин идёт на построение мембран и метаболические нужды клеток. Функция: транспорт холестерина в ткани, в том числе в печени.
ЛП высокой плотности (ЛПВП или а-липопротеины): Состав: 50% белков, 25% фосфолипидов, 20% эфиров холестерина и очень мало триацилглицеринов. Образуются главным образом в печени. В поверхностном слое ЛПВПобразуют комплексы с ферментом лецитинхолестеролацилтрансферазой (ЛХАТ). С помощью этого фермента остаток ж к-ты переносится с лицитина на свободный холестерин ЛПВП, превращая его в эфир (холестерид) и лизофосфотидилхолин. Холестерид является гидрофобным соединением, поэтому перемещается в ядро ЛПВП. Т.о. он нагружается эфирами холестерина, увел-ся в размерах и из дисковидного превращается в частицу сферической формы – зрелый ЛПВП. Далее он транспортируется в печень, где холестерин исп-ся на синтез желчных к-т. ЛПВП, благодаря ЛХАТ, забирают холестерин от других липопротеидов и транспортируют его в печень, предотвращая накопление его в клетках. Концентрация ЛПВП меняется в зависимости от ритма питания. Их мах кол-во ч/з 4-5 часов после еды. Ч/з 10-12 часов хиломикронов 0%, ЛПОНП 15%, ЛПНП 60%, ЛПВП 25%.
ЛПОНП и ЛПНП считают атерогенными, то есть вызывающими атеросклероз. ЛПВП — антитиатерогенными.
Нарушения липидного обмена могут быть как первичными, так и вторичными, т.е. вызванными патологией эндокринной системы или компенсаторные при различных заболеваниях.
Нарушения переваривания и всасывания липидов сопровождаются развитием стеатореи (повышенное содержание липидов и жирных кислот в кале) и обусловливаются одной из следующих причин:
1.Дефицит панкреатической липазы, связанный с заболеваниями поджелудочной железы.
2.Дефицит желчи в кишечнике, обсуловленный заболеваниями печени или желчевыводящих путей.
3.Угнетение ферментных систем ресинтеза триглицеридов в стенке кишечника при его заболеваниях.
Повышение липопротеидов называется гиперлипопротеидемией. Главная опасность этого состояния связана с тем, что повыш-ся вер-ть возникновения атеросклероза. Вер-ть заболевания тем выше, чем больше отношение ЛПНП к ЛПВП в крови.
Атеросклероз -это патология, которая характеризуется отложением, главным образом, холестерина в стенке крупных сосудов (аорта, коронарные сосуды, сосуды мозга и т.д.) с образованием вначале пятен, полосок. Затем на их месте образуются утолщения (атеросклеротические бляшки). Эти липидные бляшки являются своеобразным инородным телом, вокруг которого развивается соединительная ткань, затем наступает кальцификация пораженного участка сосуда. Сосуды становятся неэластичными, плотными, ухудшается кровоснабжение ткани, а на месте бляшек могут возникать тромбы. В стенке сосудов есть два защитных механизма от избыточного отложения холестерина: Работа липопротеидлипазы, которая расщепляет жир липопротеидов, делает их меньше по размеру;ЛПВП, которые уносят холестерин.Ожирение: У нормально упитанного человека жиры составляют около 15% массы тела. При сбалансированном питании количество жира в организме не изменяется. При этом жиры жировой ткани все время обновляются, то есть одновременно идут липолиз и липогенез с равными скоростями. В результате жиры жировой ткани за несколько дней обновляются полностью. При длительном голодании и физических нагрузках липолиз идет с большей скоростью, чем липогенез. В результате количество депонированного жира уменьшается. Если липогенез опережает липолиз, наступает ожирение. Наиболее частой причиной ожирения является несоответствие между количеством потребляемой пищи и энергетическими тратами организма. Такое несоответствие возникает при переедании (особенно углеводов, так как они легко переходят в жиры), при гиподинамии (при этом мобилизация жира идет с более низкой скоростью) и, особенно, при сочетании этих факторов. Кроме того, ожирение является характерным признаком многих эндокринных заболеваний. Генетические заболевания, при которых происходит неполное расщепление полимерных веществ и их накопление, получили название лизосомные болезни накопления, так как они обусловлены дефектами специфических лизосомальных гидролаз. В случае накопления липидов такие болезни называются липидозы. При липидозах нарушается нормальный катаболизм липидов до соответствующих мономеров. Болезнь Вольмана – редкое аутосомно-рецессивное заболевание из-за дефекта кислой эстеразы лизосом, что обусловливает накопление эфиров холестерола в лизосомах печени, селезенки, надпочечников, костного мозга и тонкого кишечника. Проявляется в первые недели жизни рвотой, диареей и стеатореей, гепатоспленомегалией и двусторонним кальцинозом надпочечников. Больные умирают в возрасте до 6 мес. Болезнь Шюллера-Кристиана аутосомно-рецессивное заболевание характеризуется отложением в плоских костях, твердой мозговой оболочке и коже холестерола и его эфиров. Характерными являются деструктивные изменения в костях, остеопороз, мозжечковые расстройства. Заболевание обычно начинается в возрасте до 10 лет, реже позднее. Мужчины болеют в 2 раза чаще, чем женщины. Течение заболевания прогрессирующее. Дефектный фермент неизвестен. Болезнь Гоше – отложение цереброзидов в макрофагальных клетках селезенки, печени, лимфатических узлов и костного мозга. Возникает в связи с аутосомно-рецессивным отсутствием гликоцереброзидазы (β-глюкозидазы). Основными симптомами заболевания являются спленомегалия, увеличение печени и селезенки, а также изменения в костях, проявляющиеся в виде остеопороза. При болезни Нимана-Пика наблюдается отложение сфингомиелина в клетках различных органов из-за дефицита сфингомиелиназы. Болезнь наследуется аутосомно-рецессивно, проявляется резким увеличением печени и селезенки, замедлением психического развития ребенка, появлением слепоты и глухоты. Чаще всего дети погибают в возрасте до 2 лет. Болезнь Тея-Сакса (амавротическая семейная идиотия) является результатом дефекта N-ацетилгексозаминидазы, при котором происходит отложение ганглиозидов в клетках головного мозга, что сопровождается атрофией зрительных нервов, слепотой, слабоумием и смертью в младенческом возрасте.
Содержание липидных фракций новорожденных отличается от спектра этих веществ у более старших детей и взрослых тем, что у них значительно увеличено содержание альфа-липопротеинов и понижено количество.
Опора деревянной одностоечной и способы укрепление угловых опор: Опоры ВЛ — конструкции, предназначенные для поддерживания проводов на необходимой высоте над землей, водой.
источник
Основные группы методов определения содержания мочевины подразделяют на:
- Ксантгидроловые : гетероциклический спирт ксантгидрол вступает в реакцию с мочевиной и образует нерастворимую диксантилмочевину, которую в дальнейшем определяют гравиметрически, нефелометрически, колориметрически или титрометрически. Методы точны, но трудоемки.
- Гипохлоритные – метод Б.А.Рашкована, состоящий в появлении характерной окраски при взаимодействии мочевины с гипохлоритом натрия и фенолом, практически не применяется из‑за разного оттенка опытных и контрольной проб, частого появления мути при добавлении HCl.
- Диацетилмонооксимные методы основаны на реакции Фирона – взаимодействии мочевины и диацетилмонооксима с образованием окрашенных продуктов, отличаются хорошей воспроизводимостью, высокой чувствительностью, большой специфичностью.
- Полуколичественные методы с использованием индикаторной бумаги.
- Методы с использованием ионоселективных электродов .
- Ферментативные методы базируются на гидролизе мочевины уреазой (оптимум pH 6,0‑8,0). Образовавшийся аммиак определяют с помощью различных реакций (фенолгипохлоритная, с помощью глутаматдегидрогеназы, салицилатно‑гипохлоритная).
- Газометрические (гипобромитные), основаны на окислении и разложении мочевины гипобромитом натрия в щелочной среде:
Выделяющуюся углекислоту поглощает раствор, свободным остается только азот, объем которого измеряют. Метод неспецифичен (так как гипобромит реагирует не только с мочевиной, но и другими веществами, содержащими аминогруппы), неточен, плохо воспроизводим и трудоемок.
В качестве унифицированных методов определения мочевины утверждены фенолгипохлоритный, диацетилмонооксимный и уреазный методы, экспресс‑метод с использованием индикаторной бумаги «Уреатест».
Методы этой группы основаны на реакции Фирона, протекающей в два этапа. Первый этап заключается в гидролизе диацетилмонооксима с образованием диацетила и гидроксиламина. На втором этапе гидроксиламин взаимодействует с мочевиной с образованием окрашенного диазинового производного. Для окисления гидроксиламина могут применяться: персульфат натрия, мышьяковая кислота, хлорная кислота, феназон, катионы. Для интенсификации окраски и ее стабильности применяются: тиосемикарбазид, фенилантраниловая кислота, глюкуронолактон, катионы, триптофан, нитриты.
Ферментативные методы базируются на гидролизе мочевины уреазой в инкубационной среде с pH=6,0‑6,5 (ЭДТА‑буфер) или pH=6,9‑7,0 (фосфатный буфер) на углекислый газ и аммиак. Образовавшийся аммиак можно определить по высокочувствительной и специфичной реакции с фенолгипохлоритом и катализатором нитропруссидом, по салицилатно‑гипохлоритной реакции, по реакции с реактивом Несслера (является в 10 раз менее чувствительной по сравнению с фенолгипохлоритной, малоспецифична), по дихлоризоциануратной реакции (наличие белка мешает определению).
| Сыворотка | (по реакции с диацетилмонооксимом) | |
| новорожденные | 1,4‑4,3 ммоль/л | |
| дети | 1,8‑6,4 ммоль/л | |
| взрослые | 2,5‑8,3 ммоль/л | |
| (по реакции с реактивом Несслера) | 2,5-8,3 ммоль/л | |
| (по реакции с фенолгипохлоритом) | 3,3-8,3 ммоль/л | |
| Моча (по реакции с диацетилмонооксимом) | 330‑580 ммоль/сут | |
| Моча (по реакции с реактивом Несслера) | 430‑710 ммоль/сут | |
| Слюна | около 1,83 ммоль | |
При необходимости сопоставления концентрации остаточного азота с содержанием азота мочевины концентрацию последней следует разделить на 2,14.
- in vivo: увеличение — нефротоксичные препараты, кортикостероиды, избыток тироксина; снижение – увеличение концентрации соматотропного гормона,
- in vitro: снижение (метод с уреазой) – цитрат натрия.
Уровень мочевины зависит от скорости ее синтеза в печени и выделения через почки, а также от величины белкового катаболизма.
Повышение уровня мочевины может наблюдаться при нарушении функции почек (острые и хронические заболевания, обтурация мочевых путей), нарушении почечной перфузии (застойная сердечная недостаточность), истощении запасов воды в организме (рвота, понос, повышенный диурез или потоотделение), повышенном катаболизме белка (острый инфаркт миокарда, стресс, ожоги, желтая атрофия печени, желудочно‑кишечные кровотечения), при диете с высоким содержанием белка. В тяжелых случаях острой почечной недостаточности выявлено 10‑кратное возрастание уровня мочевины. Так как водовыделительная функция почек восстанавливается быстрее, чем концентрационная способность, то нормальное выделение мочевины с мочой наступает значительно позднее, чем восстановление диуреза.
Снижение отмечается при диете с низким содержанием белка, при повышенной утилизации белка в тканях (поздние сроки беременности), тяжелых заболеваниях печени, сопровождающихся нарушением синтеза мочевины (паренхиматозная желтуха, цирроз печени).
Повышение количества мочевины в моче связано с гипертиреозом, злокачественной анемией, лихорадкой, при отравлении фосфором, отмечается при диете с высоким содержанием белка, в послеоперационном периоде.
Снижение наблюдается у больных с нефритом и другими заболеваниями почек, уремией, паренхиматозной желтухой, циррозом или дистрофией печени, также у здоровых растущих детей и при низкобелковой диете.
источник
Распад белков в организме сопровождается выделением мочевины. При этом, концентрирующийся в мочевине азот, вместе с ней выводится из организма. Повышенное содержание мочевины в крови — признак почечной недостаточности, выливающийся, например в уремию. Вот почему, важное значение приобретает определение мочевины в сыворотке крови.
Специальные исследовательские мероприятия на сыворотке крови проводятся с целью установления возможной почечной патологии, а также степени её развития. Вовремя проведенный анализ — это возможность сокращения сроков лечения.
Анализ возможен в специализированных медицинских лабораториях, имеющих соответствующую лицензию на право проведения подобных работ, а также техническое оснащение и химические реактивы.
- Газометрические.
- Уреазные.
- Фотометрические прямые.
Для определённых методик определения мочевины в кровяной сыворотке могут использоваться готовые специальные наборы с необходимым составом лабораторных реактивов.
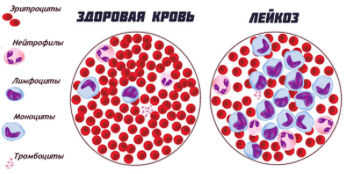
- Лейкоз.
- Дизентерия.
- Желтуха паренхиматозная.
- Пиелонефрит.
- Почечная недостаточность (хроническая форма).
- Гломерулонефрит.
Перечисленные недуги — распространенные показания, ввиду чего может понадобиться анализ концентрации мочевины в крови.
Вне зависимости от метода проведения анализа, определение мочевой кислоты имеет следующие важные особенности:
- Время забора крови с 8 до 11 часов дня.
- Пациент, не должен быть голодным более 14 часов.
- Кровь берётся из вены больного.
- Достаточный объём крови в пределах 8 мл.
Посмотрите видео про мочевину
Анна Поняева. Закончила нижегородскую медицинскую академию (2007-2014) и Ординатуру по клинико-лабораторной диагностике (2014-2016).Задать вопрос>>
Чтобы определить точную концентрацию мочевой кислоты в сыворотке крови, больному могут быть предложены следующие возможные варианты:
- Ксантгидроловые.
- Гипохлоритные.
- Диацетилмонооксимные.
- Полуколичественные методы с использованием индикаторной бумаги.
- Методы с использованием ионоселективных электродов.
- Ферментативные.
- Газометрические.
Базовый компонент, задействуемый при исследованиях — ксантгидрол (гетероциклический спирт).
Принцип метода — получение соединения ксантгидрола с мочевиной и последующее определение весовой доли каждого вещества.
Данные методы определения мочевой кислоты используются нечасто, ввиду высокой мутности соединения мочевины с лабораторными реагентами. В исследованиях задействуется гипохлорит натрия, фенол.
В результате получается характерное окрашивание используемых элементов.

В среднем на анализ затрачивается не более 10 минут.
Распространены тестовые бумаги с нанесенными реактивами под маркой «Уреатест», «Уранал».
Принцип проведения анализа практически схож, как если бы использовался глюкометр замера холестерина и сахара (данный портативный прибор с успехом устанавливает холестериновые превышения в организме человека).
При использовании метода селективный и ещё один вспомогательный электроды помещаются в исследуемую среду. Сигнал от пары электродов, направляется на измерительный прибор.
Диагностика посредством ферментативных исследований подразумевает гидролиз определённого объёма мочевины посредством уреазы.
Нормальный показатель pH при этом в пределах 6,0-8,0.
Другое название исследований гипобромитный анализ концентрации мочевины. Идея методов — использование окислительной реакции и разложения мочевины посредством гипобромита. При реакции выделяется азот и углекислота. Последний компонент устраняется специальным раствором, после чего подсчитывается количество азота.

- При приеме таких фармацевтических препаратов, как «Цисплатин», «Тетрациклин», «Аспирин», а также при ряде определённых диуретиков.
- В период беременности.
- Постоянное потребление большого количества белка.
При диацетилмонооксимном варианте определения концентрации мочевины в крови проводятся следующие шаги:
- В пробирку вносят 1 мл кислоты трихлоруксусной, 0,8 мл воды, 0,2 мл сыворотки.
- Перемешивание компонентов в центрифуге в течение 15 минут.
- В чистую пробирку вводится 0,5 мл центрифужной смеси, а также 5 мл специализированного лабораторного реактива.
- Пробирка выдерживается в течение трети часа над закипевшей водяной бане.
- После водяной бани содержимому пробирки дают остыть в течение 2-3 минут.
- Дальнейшие работы над содержимым исследуемой пробирки ведутся посредством фотометра и калибровочной пробирки.
Количественное суточное присутствие мочевины в моче проводится посредством следующей формулы:
Mсут=Cк*Eоп*a*K/Eк*b.
Mсут — концентрация мочевины в суточном объёме мочи (ед. изм. — ммоль);
- Cк — концентрация мочевины в калибровочном образце (ммоль);
- Eоп — экстинкция исследуемой пробы;
- a — суточный объём мочи (мл);
- b — объём мочи для исследования (мл);
- Eк — экстинкция калибровочной пробы;
- K — коэффициент разведения мочи.
Указанный алгоритм расчета позволяет точно определить количество мочевины.
У каждой возрастной группы концентрация мочевины своя определённая
- С рождения до 4 лет — в пределах от 1,8 до 6 ммоль, на литр.
- Дети с 4 лет до 14 лет — в пределах от 2,5 до 6 ммоль на литр.
- С 14 до 20 лет — в пределах от 2,9 до 7,5 ммоль на литр.
- Мужчины в возрасте от 20 до 50 лет — в пределах от 3,2 до 7,3 ммоль на литр.
- Женщины в возрасте от 20 до 50 лет — в пределах от 2,6 до 6,7 ммоль на литр.
- Мужчины в возрасте от 50 лет и старше — в пределах от 3,0 до 9,2 ммоль на литр.
- Женщины в возрасте от 50 лет и старше — в пределах от 3,5 до 7,2 ммоль на литр.
- В период беременности — от 1,9 до 6,0 ммоль на литр.
Показатели, находящиеся выше или ниже обозначенных пределов, указывают на ту или иную патологию, что позволяет более точно поставить диагноз.
Проводя исследования на карбамид, существуют свои тонкости:
- Замеры проводятся оперативно, в пределах четверти часа. Это обусловлено неустойчивостью окраски смешиваемых элементов.
- Калибровочная проба определяется попутно при каждой новой серии исследований. Это обусловлено неустойчивой окраской соединения мочевины с диацетилмонооксимом.
- Если концентрация мочевины в кровяной сыворотке находится выше 17 ммоль на литр, используется хлорид натрия изотонический для разведения сыворотки. Конечный результат корректируется путём умножения на коэффициент разведения.
- Для подсчёта содержания азота, конечный результат делят на 2,14.
Для определения возможного недуга, поставить точный диагноз помогает изучение мочевины в сыворотке крови. Анализ может быть назначен, как терапевтом, так и более узкими специалистами (уролог, кардиолог, нефролог, гинеколог).
источник
