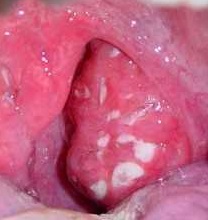
Причиной развития данного заболевания у взрослых является в большинстве случаев бета-гемолитический стрептококк группы А, реже условно-патогенная флора (стафилококки, гемофильная палочка) или вирусы (аденовирусы, цитомегаловирусы).
Заражение происходит при контакте с больным человеком или бактерионосителем. Путь передачи инфекции – воздушно-капельный, алиментарный или контактно-бытовой (при использовании предметов быта, обсеменённых патогенной флорой).
Возбудитель проникает в организм ребёнка воздушно-капельным путём, когда тому приходится общаться с уже заражённым человеком или пользоваться его вещами (игрушками, посудой, предметами личной гигиены и т. д.). Обычно это происходит в детском саду, школе или общественном транспорте. Инфицированию при этом способствует ряд определённых факторов.
Внешние факторы
- Местное переохлаждение: самая частая причина фолликулярной ангины, когда ребёнок съедает слишком много мороженого или выпивает ледяную воду.
- Общее переохлаждение организма: промокли ноги, перекупался, ходил зимой в лёгкой одежде и без шапки, длительное время оставался на морозе или на ветру и т. д.
- Частые стрессы и нервное напряжение.
- Неудачное хирургическое вмешательство: причиной нагноения фолликул может стать непрофессиональное удаление зуба с последующим занесением инфекции.
- Плохое питание.
- Переутомление.
- Недостаток витаминов.
Внутренние факторы
- Снижение иммунитета.
- Некоторые заболевания: кариес, воспаление носовых пазух, проблемы с ушами.
- Травмирование глотки и ротовой полости: царапины, ранки, ссадины.
- Инфекции: ОРВИ, дифтерия, скарлатина, грипп.
- Аллергия, туберкулёз, сбой в работе нервной системы, красная волчанка, проблемы с кровообращением, сахарный диабет.
Все эти факторы подвергают здоровье ребёнка опасности и способствуют заражению вредными микроорганизмами. Поэтому нужно снизить их влияние, особенно в период эпидемии, которая обычно начинается в осенне-зимнее время.
В отличие от других форм детской ангины, фолликулярная развивается очень стремительно. Инкубационный период может составлять 2-3 дня, но бывает, что он занимает всего несколько часов. Поэтому действовать нужно так же быстро, как и болезнь. Первая задача родителей — распознать недуг по соответствующим симптомам.
Ангина называется фолликулярной, так как гной преимущественно скапливается в фолликулах — это лимфоидные образования глотки. Слово восходит к латинскому «folliculus», что означает «мешочек, пузырь».
Фолликулярная ангина является одной из форм воспаления, поражающего миндалины и слизистую горла. К остальным типам относят:
- Катаральную. Боли в горле сопутствуют незначительное повышение температуры, слабость и вялость, небольшое воспаление лимфатических узлов
- Лакунарную. По симптомам похожа на фолликулярную, но гной накапливается в лакунах (углублениях) миндалин.
- Грибковую. Вызывают дрожжеподобные грибки. Протекание аналогично лакунарной ангине с образованием на миндалинах беловатого налета.
- Дифтерийную. Развивается вследствие попадания в организм дифтерийной палочки и представляет наибольшую опасность. Сопровождается приступами удушья.
В педиатрической практике фолликулярная ангина занимает лидирующие позиции среди всех встречающихся нозологических форм, особенно в младшей возрастной группе. В большинстве ситуаций фолликулярная ангина у детей носит вторичный характер и рассматривается как осложнение течения вирусной инфекции. Первично-бактериальная природа встречается лишь в 25% случаев.
Среди возможных возбудителей фолликулярной ангины у детей, лидирующие позиции занимает β-гемолитический стрептококк группы А. Дети новорожденного возраста не склонны к развитию фолликулярной ангины, так как в этой возрастной группе преобладают острые назофарингиты.
Фолликулярная ангина без температуры у детей является исключением из правил, так как в большинстве случаев у ребенка развивается выраженная интоксикация организма. Появление клинических признаков фолликулярной ангины у ребенка новорожденного или грудного возраста является основанием для незамедлительной госпитализации в инфекционный стационар, так как лечение данной группы пациентов должно проводиться под постоянным контролем медицинских работников.
Стрептококковый генез фолликулярной ангины у детей является опасной патологией ввиду молниеносного распространения возбудителя и склонности к развитию осложнений. Среди детской категории пациентов превалируют местные осложненные формы фолликулярной ангины в виде абсцесса и гнойного лимфаденита, которые должны подлежать незамедлительной хирургической коррекции. В отношении генерализованных последствий данного заболевания у детей следует отметить острую ревматическую лихорадку, дебют которой приходится на конец второй недели заболевания, гломерулонефрит и бактериальный эндокардит.
При ведении пациента, страдающего фолликулярной ангиной стрептококкового генеза, следует учитывать, что он представляет эпидемиологическую опасность для окружающих людей с первых суток заболевания. Антибиотики при фолликулярной ангине стрептококкового генеза должны назначаться с начала клинической картины, что позволяет сократить продолжительность симптоматики и предотвратить возможность развития осложнений.
Для всех этиопатогенетических форм фолликулярной ангины у детей характерно острое начало клинической симптоматики в виде гектической лихорадки, выраженного озноба, болевого синдрома в горле и задней стенки глотки, усиливающегося при движениях головы и глотании, отечности миндалин и появления налетов на миндалинах.
Для идентификации возбудителя фолликулярной ангины у детей основополагающей диагностической методикой является проведение посева мазка зева. И вместе с тем, четкий анализ имеющихся у ребенка клинических проявлений позволяет опытному специалисту определить вирусную или бактериальную форму болезни. При вирусной природе фолликулярной ангины превалируют такие проявления как кашель, затруднение носового дыхания, конъюнктивит. При стрептококковом генезе фолликулярной ангины катаральные симптомы, как правило, отсутствуют.
После установления бактериальной природы фолликулярной ангины у ребенка необходимо в кратчайшие сроки назначать этиотропную антибактериальную терапию. Препаратами выбора в этой ситуации являются антибиотики группы пенициллинов, цефалоспоринов или макролидов. Основной целью использования антибактериальных препаратов при фолликулярной ангине является полная эрадикация стрептококка из организма для профилактики возможного рецидива заболевания, предотвращения появления антибиотикоустойчивых штаммов возбудителя. При фолликулярной ангине у ребенка вирусного происхождения медикаментозное лечение состоит из препаратов симптоматического действия и соблюдения рекомендаций по питанию и режиму. При вирусоносительстве стрептококка у ребенка фолликулярная ангина не развивается и данная ситуация не требует проведения лечебных мероприятий.
При фолликулярном типе заболевания наблюдаются следующие признаки:
- появляется озноб;
- температура повышается до 39-40 градусов;
- сильная слабость, чувство ломоты в пояснице и суставах;
- чувствуется потеря аппетита;
- лимфатические узлы увеличены и болезненны при пальпации;
- небные миндалины и участи вокруг них опухают, воспаляются и краснеют;
- наблюдаются нагноившиеся фолликулы – белые или желтые бляшки на миндалинах;
- из-за очень сильной и острой боли больному сложно глотать;
- при сильном насморке сложно дышать ртом и носом.
На первых этапах развития болезни ее можно принять за кандидоз полости рта, герпетическую ангину или мононуклеоз.
У детей и взрослых характерным является острое начало фолликулярной ангины (см. фото), в первые дни наиболее выражены общие симптомы: повышенная до 38-40 °C температура тела, лихорадка, потливость, боли во всем теле, плохой сон и аппетит, слабость. Вскоре пациента начинает беспокоить боль в горле, которая становится более интенсивной при глотании слюны и пищи, нередко иррадиирует в ухо. Нарастает болезненность регионарных лимфоузлов (углочелюстных, шейных). Осматривая глотку, можно заметить увеличенные в объеме, гиперемированные миндалины с просвечивающими сквозь эпителиальную ткань фолликулами, наполненными гнойным содержимым.
У детей в возрасте 5-10 лет фолликулярная ангина протекает особенно тяжело – с выраженной интоксикацией, поражением мозговых оболочек (сильные боли в голове, тошнота и рвота, судорожные припадки, обморочное состояние). Могут быть диспепсические проявления (боли в эпигастральной области и по ходу кишечника, метеоризм, жидкий стул). Нередко наблюдается отказ ребенка от приема пищи, раздражительность, капризность, нарушение качества сна, снижение объема выделяемой мочи. При этом болевые ощущения в горле при глотании могут появиться только через 2-3 дня после начала болезни. Продолжительность течения ангины составляет от 1 до 3 недель.
Диагностические мероприятия в отношении фолликулярной ангины включают в себя:
- Сбор жалоб больного (типичные симптомы фолликулярной ангины характеризуются выраженными явлениями интоксикации и резкими болями в горле);
- Сбор анамнеза заболевание (выяснение причины, то есть с кем, когда и как контактировал больной);
- Сбор анамнеза жизни (наличие у больного хронических заболеваний, его условия труда и быта, экологическая обстановка места проживания);
- Объективное исследование (исключение патологии других систем и органов);
- Фарингоскопия (осмотр ротоглотки) – обращает на себя внимание наличие гнойных фолликулов на поверхности нёбных миндалин;
- Общий анализ крови (позволяет выявить лейкоцитоз со сдвигом лейкоформулы влево, повышенные значения СОЭ);
- Биохимия крови (позволяет определить маркеры воспалительной реакции в крови – С-реактивный белок, гаммаглобулины);
- Бактериологическое исследование мазка со слизистой ротоглотки (с целью дифференциальной диагностики с другими заболеваниями бактериальной или вирусной природы);
Обязательно проводится дифференциальная диагностика с такими заболеваниями, как дифтерия и инфекционный мононуклеоз. От природы возбудителя будет зависеть дальнейшая тактика лечения пациента, поэтому лечащий врач должен провести полный спектр обследования для исключения диагностической ошибки.
Осложнения при фолликулярной ангине бывают довольно часто, если лечение не начато вовремя.
- Когда боль в горле слишком сильная и острая, и больной не может глотать, то чаще всего возникает обезвоживание организма, приводит к проблемам с почками.
- При несвоевременном лечении на одной из миндалин может возникнуть перитонзиллярный абсцесс — скопление гноя в тканях горла. Боль становится невыносимой, принимая пульсирующий характер. Может возникнуть спазм жевательных мышц. Больному сложно глотать даже жидкую пищу, она выливается через нос из-за сильного отека. В этом случае нужна срочная госпитализация.
- Инфекция может распространиться на внутреннюю яремную вену (парная вена, по которой кровь идет от шеи к голове). Возле миндалевидной железы образовывается гнойный карман, и может произойти септицемия, или другими словами – заражение крови.
У людей перенесших ангину, может развиться гломерулонефрит, который приводит к отекам, повышению давления, появлению крови в моче. Невылеченная ангина в дальнейшем может привести к ревматическому поражению сердца: на первой стадии может быть поражение мышц, что в дальнейшем может привести к формированию порока сердца.
Отоларинголог – специалист по диагностике, терапевтическому или хирургическому лечению и профилактике заболевания полости носа, гортани, глотки, ушей.
За консультацией к отоларингологу, при подозрении заболевания горла, необходимо обращаться если имеются ощущения:
- боли (першения) в горле;
- отечности горла и затрудненного дыхание;
- повышения местной (в области горла) и общей температуры;
Диагноз ставится на основании опроса, осмотра глотки (фарингоскопии) и гортани (ларингоскопии). Клиническая картина тонзиллитов характерна, процент диагностических ошибок не велик. Для определения возбудителя ангины (тонзиллита) часто применяют лабораторные методы исследования (бактериологический посев, ПЦР метод, тест на бета гемолитический стрептококк группы А — БГСА, экспресс-метод и другие).
Дифференциальная лабораторная диагностика бактериальных и вирусных тонзиллитов необходима для определения стратегии лечения. При вирусной этиологии заболевания антибактериальное лечение не эффективно. Одним из вне лабораторных критериев диагностики бактериального и вирусного тонзиллита является оценка лечебного эффекта на использование антибиотиков в первые 48 часов, антибиотики на вирусы не действуют.
Следующим шагом, предваряющим лечение бактериальных тонзиллитов, является определение чувствительности микрофлоры к антибиотикам и выбор эффективного препарата. Нет принципиального отличия в лечении различных видов ангин.
При лечении ангины имеются два основных метода лечения:
Медикаментозные препараты используют в подавляющем числе клинических случаев лечения ангин.
В первые сутки после начала фолликулярной ангины у больного необходимо взять мазки из носа и зева на палочку Лефлера (возбудитель дифтерии) для проведения дифференциации этих двух патологий. После этого переходят к подбору терапии. Основа быстрого лечения фолликулярной ангины заключается в назначении антибиотиков. В первую очередь необходимо подавить бактериальную флору, а также в случае развития стрептококковой ангины провести профилактику такого серьезного осложнения патологии, как ревматизм:
Если острая ревматическая лихорадка лишь дает температуру с интоксикацией и провоцирует воспаления суставов, поражения нервной системы, стенок и клапанов сердца, то хроническая ревматическая болезнь — это тяжелые клапанные пороки сердца с прогрессирующей сердечной недостаточностью и инвалидизацией больных. Также при ангине стрептококкового генеза мы боимся вторичных гломерулонефритов, приводящих к хронической почечной недостаточности.
В связи с этим всегда при отсутствии аллергии на данный вид антибиотиков назначаются:
- Препараты первого ряда, которыми являются пенициллины (ингибиторозащищенные или полусинтетические). Это лекарственные препараты широкого спектра действия, которые весьма эффективны в борьбе со стрептококками и стафилококками. Курс пенициллина должен составлять не менее 10 дней. К препаратам данной группы относят Экоклав, Амоксиклав, Аугментин, Амоксициллин.
- Вторичный ряд антибиотиков – это макролиды. Джозамицин, Клацид (кларитромицин, Азитромицин (Хемомицин, Азитрокс, Сумамед). Курсовой прием данных препаратов должен быть ограничен 5 сутками, поскольку препараты имеют свойство накапливаться в крови, поэтому такой курс обеспечит 10 дней воздействия на бактерии в организме.
Эффективность антибактериальной терапии оцениваем в течение 72 часов по снижению температуры и улучшению общего самочувствия. Для этого больного в течение первых трех суток посещает врач. При неэффективности антибиотика его заменяют на препарат из другой группы.
При таком серьезном заболевании как фолликулярная ангина, лечение антибиотиками нельзя прекращать после того, как только станет легче. При досрочном окончании курса возможно возникновение лекарственной устойчивости бактерий к данному антибиотику и при возникновении рецидива ангины он окажется бессильным, а также развитии серьезных осложнений.
Больной должен соблюдать режим покоя, ослабленным больным запрещено выходить на улицу, поскольку может возникнуть ухудшение состояния.
Чтобы избежать сильного обезвоживания организма от лихорадки и выраженной интоксикации, для скорейшего вывода токсинов, показано обильное теплое питье, лучше всего это теплое молоко с содой или минеральной водой без газов, также хорошо помогают фиточаи — с ромашкой аптечной, шалфеем, шиповником. Температура жидкости должна быть оптимально комфортной, не горячей и не холодной, чтобы не вызывать лишнее травмирование воспаленной слизистой.
- Антигистаминные и жаропонижающие средства.
Для того чтобы уменьшить проявления ангины, применяют нестероидные противовоспалительные средства, которые снижают температуру и боль (ибуклин, парацетамол, нурофен). Также для снижения симптомов аллергического компонента воспаления используют антигистаминные средства (Цетрин, Кларисенс, Лоратадин).
Питание должно быть однородным, поскольку при осуществлении глотания твердая пища значительно усиливает болевые ощущения, рацион должен формироваться из жидких бульонов, супчиков, каш. Также важно часто выполнять проветривание помещения и регулярно выполнять уборку в комнате (ежедневно).
Кроме антибиотика дополнять лечение необходимо местными процедурами. Процесс развития этого заболевания заключается сначала в формировании гнойного фолликула, затем его созревание, рост в размерах, и наконец, процесс вскрытия фолликула. Именно по причине постоянного нахождения гнойного отделяемого в ротовой полости важнейшим условием правильного лечения фолликулярной ангины считается частое полоскание горла.
Полоскать горло при ангине нужно как можно чаще до 6-10 раз в день. Использовать при процедуре можно специальные антисептические средства, такие как Йодинол, Долфин, Люголь, Хлорофиллипт, Мирамистин, фурацилин (2 табл. на стакан воды), травяные настои, раствор соды и соли. Фармацевтическая промышленность предлагает также великое множество различных аэрозолей, которыми удобно пользоваться – Ингалипт, Тантум Верде, Гексорал. Также можно смягчать боли в горле и отек с помощью рассасывающих таблеток и леденцов — Фарингосепт, Гексорал табс и пр. Помимо дезинфицирующего действия, полоскание горла способствует смыванию гнойных выделений, которые образуются после вскрытия фолликулов.
Существует один широкодоступный метод народного лечения фолликулярной ангины – полоскание горла следующим раствором: натереть на мелкой терке 1 свеклу, из расчета 1 столовая ложка 6% яблочного уксуса на 1 стакан свекольной массы, соединить свекольную массу с уксусом и положить полученную смесь в темное место на 4 часа, после чего сок отжать с помощью плотной ткани и полученным соком проводить полоскание горла каждые 3 часа. Свекольный сок в комплексе с яблочным уксусом оказывает уникальные антибактериальные свойства.
Если фолликулярная ангина повторяется с неприятной регулярностью, с каждым разом протекает все интенсивнее и болезненнее, приносит много страданий больному и оставляет после себя осложнения, единственным остающимся выходом становится оперативное вмешательство.
Врачи считают миндалины своеобразным естественным фильтром, которые не пропускают разнообразные болезнетворные микроорганизмы дальше горла. Именно поэтому в наши дни миндалины удаляют только в крайних случаях, когда польза от их отсутствия будет намного больше, чем при их наличии. Раньше же считалось, что единственным вариантом лечения ангины с серьезными проявлениями является операция.
Сейчас миндалины далеко не всегда оперируют. Чаще всего на них оказывается местное воздействие типа замораживания, при котором соседние, здоровые ткани совершенно не страдают и не повреждаются. В результате такой манипуляции пациент быстрее выздоравливает и намного легче переносит хирургическое вмешательство.
Специфических мер профилактики фолликулярной ангины не существует. Для предупреждения развития данного заболевания необходимо придерживаться ряда правил:
- Отказаться от вредных привычек (табакокурения, употребления спиртных напитков);
- Оптимизировать условия труда и отдыха (здоровый и крепкий сон, оптимальные физические нагрузки, исключение стрессовых ситуаций);
- Ограничить контакт с вредными и токсичными веществами;
- Закаливать организм;
- Заниматься физкультурой (легкие пешие прогулки, плавание);
- Санировать очаги хронической инфекции в ротоглотке (кариес, гингивиты, синуситы);
Таким образом, фолликулярная ангина является опасным в плане развития осложнений инфекционно-воспалительным заболеванием, требующим своевременной диагностики и лечения. Для достижения положительных результатов в лечении фолликулярной ангины у взрослых и детей необходимо при появлении первых симптомов заболевания обращаться к врачу для определения верной тактики лечения и исключения диагностических ошибок.
Прогноз благоприятный при своевременной диагностике и рациональной антибиотикотерапии. Ухудшение прогноза в отношении осложнений характерно для тяжелого течения, невосприимчивости к проводимой терапии, некорректном лечении, наличии тяжелых сопутствующих заболеваний, у иммунокомпрометированных пациентов.
источник
Лечение повышенного белка в моче зависит от причины, которая помешала почкам полностью вернуть в кровь белок, поступивший в ее канальцы, и он оказался там, где ему быть не положено — в моче.
Присутствие белка в моче – в соответствии с физиологическими нормами – практически нулевое (менее 0,03 г в литре урины за сутки). Если этот показатель выше, то это уже можно считать протеинурией. Именно так в клинической медицине называется повышенный белок в моче. Данная патология подразделяется на протеинурию преренальную (при усиленном распаде белка в тканях), ренальную (при почечных патологиях), постренальную (при заболеваниях мочевыводящей системы) и инфраренальную (секреторную). В свою очередь — по характеру ключевого патофизиологического механизма — каждый из этих видов имеет массу подвидов.
Следует отметить, что повышенный белок в моче не всегда является признаком какой-либо болезни. Так называемая физиологическая протеинурия проявляется при избытке в рационе белковой пищи, при длительном мышечном напряжении, пребывании на холоде или на солнце, при стрессах. Как только исчезает негативный фактор, все приходит в норму. И в подобных случаях лечение повышенного белка в моче не требуется.
А вот постоянно или длительно повышенный белок в моче является свидетельством весьма серьезных проблем со здоровьем. Чем выше содержание белка в моче (более 0,5 г/л в день), тем реальнее развитие почечной недостаточности.
В первую очередь, лечение повышенного белка в моче требуется при гломерулярных болезнях – остром и хроническом гломерулонефрите (нефрите) и нефротическом синдроме. Повышение содержания протеинов в моче также числится в списках симптомов таких заболеваний, как пиелонефрит, цистит, уретрит, туберкулез почек, киста почки, простатит, амилоидоз, сахарный диабет, ревматоидный артрит, системная склеродермия, подагра, артериальная гипертензия, сердечная недостаточность, малярия, лейкемия, гемолитическая анемия.
Кроме того, повышенный белок в моче отмечается при негативном воздействии некоторых лекарственных препаратов, отравлениях токсическими веществами и тяжелыми металлами, при хроническом дефиците калия в организме. А когда белок в моче выявлен у беременной женщины в последнем триместре гестации, то налицо явный симптом нефропатии — дисфункции плаценты, которая чревата преждевременными родами.
Совершенно очевидно, что лечение повышенного белка в моче может быть либо этиологическим — направленным на устранение причины основной болезни, либо патогенетическим, когда целью терапии является механизм развития заболевания.

За концентрацию белков в моче отвечает почечная базальная мембрана – гломерулярный барьер, который фильтрует протеины плазмы крови и не допускает их выхода в мочу. Когда нарушается проницаемость этого барьера, уровень белка в моче возрастает.
При остром гломерулонефрите это происходит вследствие стрептококковой, стафилококковой или пневмококковой инфекции (фарингита, ангины, синусита, пневмонии и др.), токсины которой повреждают почечную мембрану и проводят к образованию антител к М-протеину стрептококка и иммунному воспалению клубочков почки.
Нефротический синдром считается аутоиммунным заболеванием, которое может развиваться при красной волчанке или системном нарушении белкового обмена (амилоидозе), а также при сахарном диабете (диабетическая нефропатия) и злокачественных новообразованиях. Обострения и рецидивы нефротического синдрома могут провоцироваться инфекциями. У пациентов с такими диагнозами отмечаются отеки, повышенное артериальное давление, повышенный белок в моче (3-3,5 г/л в сутки), а также наличие крови в моче (макрогематурия) и сокращение суточного диуреза (выделения мочи).
При данных заболеваниях — после уточнения диагноза и антибактериальной терапии имеющихся инфекций — урологи назначают следующие основные препараты для лечения повышенного белка в моче: кортикостероиды (преднизолон или метилпреднизолон); цитостатики (циклофосфамид); антиагреганты (дипиридамол).
Метилпреднизолон является аналогом преднизолона (синтетического гормона надпочечника кортизона), но у него меньше побочных действий и лучшая переносимость больными как при внутримышечном введении (суспензия для инъекций метилпреднизолона натрия сукцинат), так и при пероральном применении (в таблетках по 0,004 г). Дозировку лекарственного средства определяет врач в зависимости от степени тяжести заболевания: средняя суточная доза составляет 0,004-0,048 г (в форме таблеток); внутримышечно — 4-60 мг в сутки. Курс лечения – от одной недели до месяца.
Побочные действия данного препарата: задержка натрия и воды в тканях, потеря калия, повышение АД, мышечная слабость, ломкость костей (остеопороз), повреждение слизистой желудка, снижение функции надпочечников. Применение метилпреднизолона в период беременности (как и всех кортикостероидов, поскольку они проникают через плаценту) возможно, если ожидаемый эффект лечения для женщины превышает потенциальный риск для плода.

Лекарственное средство циклофосфамид (синонимы – цитофорсфан, цитоксан, эндоксан, геноксол, митоксан, процитоке, сендоксан, клафен) препятствует делению клеток на уровне ДНК и обладает противоопухолевым действием. Циклофосфан используется в качестве иммунодепрессивного средства, так как подавляет деление В-лимфоцитов, участвующих в иммунном ответе. Именно это действие используется в лечении повышенного белка в моче при гломерулонефритах и нефротическом синдроме.
Препарат (в ампулах по 0,1 и 0,2 г) вводят внутривенно и внутримышечно — согласно назначенной врачом схеме лечения из расчета 1,0-1,5 мг на килограмм массы тела (50-100 мг в сутки). Внутрь принимают таблетки по 0,05 г, дозировка: по 0,05-0,1 г дважды в день.
В числе противопоказаний данного лекарственного средства: повышенная чувствительность, тяжелые нарушения функции почек, гипоплазия костного мозга, лейкопения, анемия, онкологические заболевания, беременность и лактация, наличие активных воспалительных процессов. Возможные побочные эффекты циклофосфамида: тошнота, рвота, боли в области живота, нарушение менструального цикла, алопеция (выпадение волос), потеря аппетита, снижение уровня лейкоцитов крови, изменение цвета ногтевых пластин.

Для терапии данной патологии врачи используют дипиридамол (синонимы — курантил, персантин, пенселин, ангинал, кардиофлукс, корозан, диринол, тромбонин и др.). Этот препарат тормозит склеивание (агрегацию) тромбоцитов и препятствует образованию тромбов в кровеносных сосудах, поэтому его применяют в целях предупреждения образования тромбов после операций, при инфаркте миокарда и проблемах с мозговым кровообращением. При хронических заболеваниях почек, связанных с нарушением функций гломерулярного барьера, данное лекарственное средство способствует улучшению фильтрации крови.
Таблетки-драже по 0,025 г рекомендуется принимать по 1 шт. три раза в день. В отдельных случаях дипиридамол может иметь побочные эффекты в виде кратковременной гиперемии лица, учащения пульса и кожных высыпаний. Противопоказание к применению данного лекарства — распространенный склерозирующий атеросклероз коронарных артерий.
Для симптоматического лечения повышенного белка в моче применяются гипотензивные, мочегонные и спазмолитические средства.
Например, среди диуретиков рекомендуется мочегонный препарат растительного происхождения канефрон, в составе которого содержатся золототысячник, кожура шиповника, любисток и розмарин. Он уменьшает проницаемость капилляров почек и способствует нормализации их функций. Кроме того, канефрон работает как уросептик и спазмолитик.
Канефрон выпускается в форме каплей и драже. Дозировка для взрослых — по 2 драже или по 50 капель трижды вдень; детям в возрасте 1-5 лет — по 15 капель 3 раза в сутки, старше 5 лет — по 25 капель или по одному драже трижды в течение суток.

Применение антибактериальных препаратов в комплексном лечении повышенного содержания белка в моче направлено на ликвидацию очага инфекции в начальной стадии заболевания и подавления инфекции в дальнейшем течении болезни.
Из антибиотиков пенициллинового ряда во многих случаях — при воспалении легких (в том числе с абсцессами), ангинах, холецистите, инфекциях желче- и мочевыводящих путей и кишечника — назначается ампициллин.
Таблетки и капсулы по 0,25 г назначают принимать внутрь: взрослым – по 0,5 г 4-5 раз в день, независимо от приема пиши; детям доза рассчитывается в зависимости от веса — 100 мг/кг. Длительность курса терапии составляет минимум 5 дней.
Применение ампициллина может вызывать нежелательные побочные реакции в виде кожной сыпи, крапивницы, отека Квинке; при продолжительном лечении возможно развитие суперинфекции. Во избежание этого необходимо одновременно принимать витамины С и группы В. К противопоказаниям данного антибиотика относятся повышенная чувствительность к пенициллину и склонность к аллергии.
Лечение повышенного белка в моче антибиотиками не обходится без олеандомицин (аналог — олететрин) — антибиотик группы макролидов — активен в отношении многих грамположительных, грамотрицательных и анаэробных бактерий, устойчивых к пенициллину. Его прописывают (таблетки по 125 тыс. ЕД и по 250 тыс. ЕД) при ангине, отите, синусите, ларингите, пневмонии, скарлатине, дифтерии, коклюше, гнойном холецистите, флегмонах, а также при сепсисе стафилококкового, стрептококкового и пневмококкового происхождения.
Доза для взрослых — по 250-500 мг (в 4-6 приемов, суточная доза не более 2 г); для детей до 3 лет — 20 мг на килограмм массы, 3-6 лет — 250-500 мг в сутки, 6-14 лет — 500 мг-1 г, после 14 лет — 1-1,5 г в сутки. Курс лечения длится от 5 до 7 дней.
Возможные побочные эффекты: кожный зуд, крапивница, нарушения функции печени (редко). В период беременности и лактации олеандомицин применяют с большой осторожностью и только по строгим показаниям лечащего врача.
О том, что белок в моче значительно повышен, говорят такие признаки, как быстрая утомляемость и головокружение, головная боль и боль в области поясницы, отеки, снижение аппетита, озноб, рвота или тошнота, повышение артериального давления, одышка и учащенное сердцебиение. Самолечение в данном случае недопустимо и невозможно!
Адекватное и эффективное лечение повышенного белка в моче может назначить только врач – уролог или нефролог – после лабораторного исследования мочи, обследования пациента и всестороннего анализа клинической картины заболевания.
источник
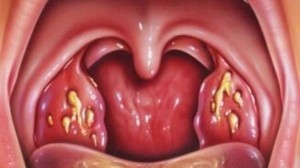
Типичные проявления заболевания сразу же заставляют задуматься о том, что это ангина. Для неё характерны боли в горле, а на миндалинах образуются белые налёты. Но этим клиника не ограничивается. Сопровождается ангина интоксикацией, достаточно сильной.
При ангине интоксикация организма проявляется следующими симптомами.
-
Лихорадка. Продолжается не больше недели. Сопровождается ознобом.
- Болевой синдром: боли в мышцах, в области поясницы, головные боли.
- Слабость, быстрая утомляемость.
- Аппетит снижается или отсутствует совсем.
- Нарушение сна.
- У детей возможна рвота, признаки воспаления мозговых оболочек.
- Увеличение регионарных лимфоузлов (в подчелюстной области).
- Дискомфорт в области сердца, боли, выраженная тахикардия. Частый пульс отмечается при высокой температуре, но может быть результатом токсического влияния на сердце (при отсутствии лихорадки). Могут выявляться изменения на ЭКГ.
- Редко, но бывает, что увеличиваются печень и селезёнка.
- Возможно, появление эритроцитов в моче.

Могут страдать почки, базальные мембраны клубочков которых также подвержены негативному влиянию продуктов жизнедеятельности стрептококка. Токсины не только сами способны вызывать интоксикацию при тонзиллите, но и способствуют образованию иммунных комплексов, которые циркулируют по кровеносным сосудам, осаждаются в почечных клубочках, повреждают их стенку и нарушают кровоток. Эти комплексы способствуют развитию тромбозов и нарушению кровообращения в почках.
Некоторые симптомы интоксикации проявляются в первые дни болезни. Но самые тяжёлые осложнения развиваются тогда, когда человек считает себя абсолютно здоровым. Чаще такие осложнения наблюдаются у людей, столкнувшихся с ангиной не в первый раз. Способен вызвать тяжёлую интоксикацию тонзиллит, имеющий хроническое течение с частыми обострениями. Не последнюю роль играют особенности генетики.

- паратонзиллита (вовлечение в воспалительный процесс тканей вокруг миндалин);
- отита (воспаление уха);
- синусита (воспалительный процесс в околоносовых пазухах);
- эндокардита (инфекционное воспаление клапанов сердца);
- заглоточного абсцесса (гнойное расплавление лимфоузлов и клетчатки заглоточного пространства);
- отёка гортани;
- флегмоны шеи (разлитое воспаление подкожной клетчатки);
- сепсиса (генерализованная инфекция);
- менингита (воспаление мозговых оболочек);
- инфекционно-токсического шока.
Чаще всего такие осложнения возникают у детей, ослабленных больных, при снижении иммунной защиты организма.
- Острая ревматическая лихорадка. Проявляется через две, иногда три недели после выздоровления. Характерно поражение сердца, суставов, наличие кожных изменений, повышение температуры тела. При поражении клапанного аппарата сердца — развиваются его пороки.
- Острый гломерулонефрит может проявляться спустя восемь, а то и десять дней от начала заболевания. Первые изменения наблюдаются при исследовании общего анализа мочи, где обнаруживается много лейкоцитов, эритроцитов, появляется белок и цилиндры.
При хроническом тонзиллите отравление токсинами стрептококка, который постоянно находится в миндалинах, в полости рта и носа (в том числе в кариозных зубах, околоносовых пазухах) может приводить к развитию: миокардиодистрофии, кардиосклерозу, порокам сердца на фоне эндокардита. Могут появляться воспалительные изменения в сосудах и тромбоэмболические осложнения.
При обычном течении ангины госпитализация не требуется. Но необходима консультация врача, который поставит диагноз, даст основные рекомендации по лечению и объяснит, как снять интоксикацию при ангине.
Лечебные мероприятия включают:
-
Режим — постельный.
- Антибактериальная терапия: препараты из группы пенициллинов, макролиды или цефалоспорины.
- Обильное питье: щелочная минеральная вода, соки, отвары трав.
- Обезболивающие и противовоспалительные препараты помогают справиться с лихорадкой, уменьшают болевой синдром. Для этого подойдут: Парацетамол, Нимесулид, Ибупрофен.
- Местное лечение: полоскание настоем ромашки, календулы, Хлоргексидином, раствором фурацилина, перекисью водорода 3% (1 чайная ложка на половину стакана воды). Можно использовать аэрозоли и спреи: Гексорал, Гексаспрей, Стопангин и другие.
- Антигистаминные средства могут облегчить состояние (Супрастин, Зодак, Цетрин и др.).
Если на фоне лечения состояние ухудшается: сохраняется лихорадка, боли в горле становятся интенсивнее, появляется выраженная болезненность в области шеи, увеличиваются лимфоузлы, появляется слюнотечение и становится тяжело открывать рот, нарастает слабость, беспокоят боли за грудиной или в прекардиальной области, аритмии, сильные головные боли, падает артериальное давление – необходима срочная госпитализация.
В условиях стационара проводится инфузионная терапия, внутривенное или внутримышечное введение антибиотиков. При необходимости проводится оперативное лечение (вскрытие абсцесса). Если потребуется – весь комплекс реанимационных мероприятий.

- избавление от хронических инфекционных очагов (кариозные зубы, синуситы, фарингиты, хронический тонзиллит);
- наблюдение у врача на протяжении трёх месяцев после клинического выздоровления, с обязательным контролем ЭКГ, анализа крови и мочи;
- полноценное питание;
- при частых ангинах, возможно, удаление миндалин;
- повышение общего и местного иммунитета: Имудон, Тонзилгон, Иммунал;
- физиотерапевтические процедуры с использованием аппарата Тонзиллор;
- бициллинопрофилактика – введение длительно действующего антибиотика пенициллинового ряда для профилактики ангины.
Не стоит считать ангину безобидным заболеванием. К лечению нужно подходить основательно и грамотно, чтобы избежать тяжёлых осложнений в будущем.
источник

Типичные проявления заболевания сразу же заставляют задуматься о том, что это ангина. Для неё характерны боли в горле, а на миндалинах образуются белые налёты. Но этим клиника не ограничивается. Сопровождается ангина интоксикацией, достаточно сильной.
При ангине интоксикация организма проявляется следующими симптомами.
-
Лихорадка. Продолжается не больше недели. Сопровождается ознобом.
- Болевой синдром: боли в мышцах, в области поясницы, головные боли.
- Слабость, быстрая утомляемость.
- Аппетит снижается или отсутствует совсем.
- Нарушение сна.
- У детей возможна рвота, признаки воспаления мозговых оболочек.
- Увеличение регионарных лимфоузлов (в подчелюстной области).
- Дискомфорт в области сердца, боли, выраженная тахикардия. Частый пульс отмечается при высокой температуре, но может быть результатом токсического влияния на сердце (при отсутствии лихорадки). Могут выявляться изменения на ЭКГ.
- Редко, но бывает, что увеличиваются печень и селезёнка.
- Возможно, появление эритроцитов в моче.

Могут страдать почки, базальные мембраны клубочков которых также подвержены негативному влиянию продуктов жизнедеятельности стрептококка. Токсины не только сами способны вызывать интоксикацию при тонзиллите, но и способствуют образованию иммунных комплексов, которые циркулируют по кровеносным сосудам, осаждаются в почечных клубочках, повреждают их стенку и нарушают кровоток. Эти комплексы способствуют развитию тромбозов и нарушению кровообращения в почках.
Некоторые симптомы интоксикации проявляются в первые дни болезни. Но самые тяжёлые осложнения развиваются тогда, когда человек считает себя абсолютно здоровым. Чаще такие осложнения наблюдаются у людей, столкнувшихся с ангиной не в первый раз. Способен вызвать тяжёлую интоксикацию тонзиллит, имеющий хроническое течение с частыми обострениями. Не последнюю роль играют особенности генетики.

- паратонзиллита (вовлечение в воспалительный процесс тканей вокруг миндалин);
- отита (воспаление уха);
- синусита (воспалительный процесс в околоносовых пазухах);
- эндокардита (инфекционное воспаление клапанов сердца);
- заглоточного абсцесса (гнойное расплавление лимфоузлов и клетчатки заглоточного пространства);
- отёка гортани;
- флегмоны шеи (разлитое воспаление подкожной клетчатки);
- сепсиса (генерализованная инфекция);
- менингита (воспаление мозговых оболочек);
- инфекционно-токсического шока.
Чаще всего такие осложнения возникают у детей, ослабленных больных, при снижении иммунной защиты организма.

- Острая ревматическая лихорадка. Проявляется через две, иногда три недели после выздоровления. Характерно поражение сердца, суставов, наличие кожных изменений, повышение температуры тела. При поражении клапанного аппарата сердца — развиваются его пороки.
- Острый гломерулонефрит может проявляться спустя восемь, а то и десять дней от начала заболевания. Первые изменения наблюдаются при исследовании общего анализа мочи, где обнаруживается много лейкоцитов, эритроцитов, появляется белок и цилиндры.
При хроническом тонзиллите отравление токсинами стрептококка, который постоянно находится в миндалинах, в полости рта и носа (в том числе в кариозных зубах, околоносовых пазухах) может приводить к развитию: миокардиодистрофии, кардиосклерозу, порокам сердца на фоне эндокардита. Могут появляться воспалительные изменения в сосудах и тромбоэмболические осложнения.
При обычном течении ангины госпитализация не требуется. Но необходима консультация врача, который поставит диагноз, даст основные рекомендации по лечению и объяснит, как снять интоксикацию при ангине.
Лечебные мероприятия включают:
-
Режим — постельный.
- Антибактериальная терапия: препараты из группы пенициллинов, макролиды или цефалоспорины.
- Обильное питье: щелочная минеральная вода, соки, отвары трав.
- Обезболивающие и противовоспалительные препараты помогают справиться с лихорадкой, уменьшают болевой синдром. Для этого подойдут: Парацетамол, Нимесулид, Ибупрофен.
- Местное лечение: полоскание настоем ромашки, календулы, Хлоргексидином, раствором фурацилина, перекисью водорода 3% (1 чайная ложка на половину стакана воды). Можно использовать аэрозоли и спреи: Гексорал, Гексаспрей, Стопангин и другие.
- Антигистаминные средства могут облегчить состояние (Супрастин, Зодак, Цетрин и др.).
Если на фоне лечения состояние ухудшается: сохраняется лихорадка, боли в горле становятся интенсивнее, появляется выраженная болезненность в области шеи, увеличиваются лимфоузлы, появляется слюнотечение и становится тяжело открывать рот, нарастает слабость, беспокоят боли за грудиной или в прекардиальной области, аритмии, сильные головные боли, падает артериальное давление – необходима срочная госпитализация.
В условиях стационара проводится инфузионная терапия, внутривенное или внутримышечное введение антибиотиков. При необходимости проводится оперативное лечение (вскрытие абсцесса). Если потребуется – весь комплекс реанимационных мероприятий.

- избавление от хронических инфекционных очагов (кариозные зубы, синуситы, фарингиты, хронический тонзиллит);
- наблюдение у врача на протяжении трёх месяцев после клинического выздоровления, с обязательным контролем ЭКГ, анализа крови и мочи;
- полноценное питание;
- при частых ангинах, возможно, удаление миндалин;
- повышение общего и местного иммунитета: Имудон, Тонзилгон, Иммунал;
- физиотерапевтические процедуры с использованием аппарата Тонзиллор;
- бициллинопрофилактика – введение длительно действующего антибиотика пенициллинового ряда для профилактики ангины.
Не стоит считать ангину безобидным заболеванием. К лечению нужно подходить основательно и грамотно, чтобы избежать тяжёлых осложнений в будущем.
источник
Роль ангины и хронического тонзиллита в происхождении заболеваний почек издавна обсуждается в литературе, и нет возможности (да и надобности) привести все это огромное количество публикаций. Заинтересованного читателя мы отсылаем к монографии М. Г. Григ, где достаточно полно изложена соответствующая литература. Здесь же постараемся представить в основном клинический материал и лишь коротко коснуться вопросов патогенеза тонзиллогенных поражений почек.
Нам кажется целесообразным разделить почечную патологию при ангине и хроническом тонзиллите на две группы: 1) проявление заболевания и 2) осложнение его. Под первым мы понимаем те изменения почечной функции, которые обязаны в основном острой или хронической инфекционной интоксикации, недостаточны для диагностики нефрита и исчезают вскоре после выздоровления от основного заболевания, осложнение же нам представляется уже самостоятельным заболеванием почек и мочевыводящей системы, которое может продолжаться и после ликвидации тонзиллогенной интоксикации. Грань между ними часто бывает нечеткой, а иногда даже условной, но такое деление позволяет практическому врачу правильно ориентироваться в диагностике и лечении почечных осложнений у больных ангиной и хроническим тонзиллитом.
Ангина — стрептококковое заболевание (в большинстве случаев), а значительное поражение почек при стрептококковой (особенно тонзиллярной) инфекции подмечено не только клинически, но доказано и в эксперименте. Поэтому легко понять, почему так часто обнаруживаем у больных ангиной микрогематурию и умеренную альбуминурию. В наших наблюдениях эти проявления инфекционной интоксикации у больных ангиной отмечены в 54% случаев, притом практически одинаково часто при тяжелой, среднетяжелой и легкой ангине. А. И. Батурин в работе, проведенной под нашим руководством, нашел, что в остром периоде болезни олигурия наблюдается у половины обследованных, никтурия — почти у всех (у 40 из 44), фиксированный на высоких цифрах удельный вес мочи у 17 из 44 и монотонный удельный вес — у 23 из 44. После клинического выздоровления (перед выпиской из клиники) описанные изменения обнаруживаются еще довольно часто (олигурия — у 11, никтурия — у 30, монотонный удельный вес — у 8), и только через 2 недели после выписки из стационара (после пятидневной пенициллинотерапии и клинического выздоровления) проба Зимницкого в основном нормализуется, хотя никтурия и фиксированный высокий удельный вес мочи у части реконвалесцентов еще выявлялись (соответственно у 5 и 4 переболевших).
Автор согласен с И. И. Зарецким, что фиксацию удельного веса мочи на высоких цифрах и монотонность его нужно связывать не только с экстраренальными факторами, но и с понижением функциональной гибкости почек. Он изучил также состояние почечных мембран при помощи пробы Амбурже. У здоровых лиц (обследовано 30 человек) в минутном объеме мочи максимальное количество эритроцитов не превышало 100, а лейкоцитов — 500 (что совпадает с данными Амбурже). Из больных же ангиной в первом периоде проба оказалась нормальной всего у 8, во втором — у 23, а через 2 недели после выписки из стационара — у 33 из 44 обследованных. Количество форменных элементов в моче увеличивалось в прямой зависимости от тяжести ангины и достигало до 2000-6000 в минутном объеме мочи. Важно подчеркнуть, что при обычном анализе мочи патология не всегда выявлялась даже при таком большом количестве форменных элементов. Параллельное изучение ломкости капилляров, по А. И. Нестерову, показало, что повышенная ломкость сосудов (II и III степени) в остром периоде имелась у 16, перед выпиской — у 9, а через 2 недели — у 5.
Таким образом, изученные функции почек нарушены практически у всех больных ангиной, у части из них они не нормализуются даже через 2 недели после клинического выздоровления (особенно проницаемость для форменных элементов крови).
Что же касается осложнений — острого нефрита и пиелонефрита, то частоту их трудно установить по литературным данным, так как обычно обследуют уже заболевших нефритом и сообщают о частоте связи нефрита с ангиной. А. И. Гнатюк отметил ангину в ближайшем анамнезе у 166 из 224 больных острым нефритом. М. Г. Григ нашла, что в 80% случаев причиной острого нефрита явились ангина и обострение хронического тонзиллита (т. е. первичная и рецидивирующая ангины). Е. М. Тареев главное значение в генезе острого нефрита также придает назофаренгеальной инфекции.
Однако нас больше интересует вопрос несколько в ином освещении: как часто возникают почечные осложнения у больных ангиной и каковы причины, способствующие их возникновению?
Изменения, которые не могли быть уже расценены как проявления болезни со стороны почек и должны были быть признаны осложнениями, из 325 больных ангиной мы могли отметить у 19 (5,8%). У троих диагностировался острый цистоуретрит, у 15 — пиелонефрит и лишь у одного — острый гломерулонефрит.
Важно проследить за обстоятельствами, приведшими к почечным осложнениям у этих больных. По тяжести основного заболевания и по частоте перенесенных ранее ангин они распределялись следующим образом: легкой ангиной болели 4 человека, среднетяжелой -7 и тяжелой — 8; впервые болели ангиной 7 человек, повторно, но редко — 4, повторно и часто — 8 больных. Таким образом, по этим двум признакам они существенно не отличались от всей массы обследованных больных. Можно лишь заметить некоторое преобладание тяжелых и среднетяжелых форм. Тогда рассмотрим время возникновения этих осложнений. Только у 3 больных осложнение возникло на 2-3-й день болезни (у одного острый цистит, у двоих — острый пиелонефрит), т. е. одновременно с разгаром ангины. У всех же остальных 15 человек возникновение осложнения было связано с очень поздним поступлением (позже 5-го дня болезни) или ранним рецидивом болезни, вернее — обострением ангины, когда вскоре после нормализации или снижения температуры до субфебрильных цифр вновь наступало обострение ангины, часто в связи с поступ-лением свежих больных или при раннем прекращении лечения на дому.
К сказанному надо добавить, что пиелонефрит, возникающий в разгаре болезни, несмотря на свою выраженность, легко поддавался обычно проводимой пенициллинотерапии и не требовал удлинения курса, в то время как это же осложнение, возникающее во время обострения ангины, было более упорным.
Учитывая огромное значение, которое в последнее время придается пиелонефритам, нам хотелось подчеркнуть некоторые клинические особенности упомянутого осложнения у наших больных.
Жалобы, могущие навести на мысль о патологии почек или моче-выводящей системы, из 19 больных предъявляли всего четверо. Притом у 2 из них наступило осложнение острым уретритом, у одного — гломерулонефритом и только у одного — пиелонефритом. Таким образом, 14 из 15 больных с лабораторно-несомненным, выраженным пиелонефритом субъективных ощущений, говорящих в пользу этого осложнения, не имели. Ясно, что вне условий клиники (или, во всяком случае, стационара) эти больные не были бы повторно обследованы в связи с появлением обострения ангины (иногда очень кратковременного!), и у части из них мог развиться хронический пиелонефрит.
Таким образом, выделяются две особенности пиелонефритов, осложняющих ангину : 1) их наиболее частое возникновение при ранних обострениях ангины и 2) бессимптомное (в смысле субъективных ощущений) их течение.
Роль хронического тонзиллита в возникновении почечной патологии также не является спорной. Однако нас интересовало, насколько связана частота почечных поражений с клинической формой хронического тонзиллита, т. е. с выраженностью хронической тонзиллогенной интоксикации. Это могло бы пролить свет и на патогенез поражения почек и мочевыводящей системы у больных хроническим тонзиллитом.
Следы белка (реже до 0,033%) и микрогематурия у 1-й группы больных выявлялись в 11,3% случаев, во 2-й группе — в 15, а в 3-й 21% анализов. Кроме того, у 8 больных субкомпенсированным и 8 больных декомпенсированным хроническим тонзиллитом при обследовании был выявлен скрыто протекавший пиелонефрит.
Из больных компенсированным тонзиллитом пиелонефрит не был диагностирован ни у одного, но у 2 обнаружен цистоуретрит.
Приведенные данные показывают, что при амбулаторном обследовании больных хроническим тонзиллитом, особенно при токсико-аллергической ее форме (субкомпенсированной и декомпенсированной), необходимо проводить анализ мочи, что в практике далеко не всегда делается. Известно, насколько трудна бывает диагностика пиелонефритов. Это заставляет исследователей предлагать более усовершенствованные, сложные методы исследования больных, и если не будут применяться даже такие простые методы, как анализ мочи, то, безусловно, упущений будет еще больше.
Г. П. Шульцев пишет, что в настоящее время преобладают больные с хроническим нефритом, которые попадают к врачу нередко уже с явлениями почечной недостаточности, и что явно увеличилось число больных хроническим пиелонефритом.
Это указание, подтвержденное в наблюдениях многих авторов, нас должно настораживать. Одним из важных способов раннего выявления таких больных, безусловно, является тщательное терапевтическое обследование больных хроническим тонзиллитом, особенно токсико-аллергической ее формой. Это тем более важно, что роль (по-видимому, решающая) стрептококковой инфекции в развитии не только острого, но и хронического нефрита сегодня надо считать доказанной.
Источником стрептококковой инфекции при нефрите могут быть не только тонзиллы — описаны единичные случаи развития нефрита и вслед за мезотимпанитом, вызванным бета-гемолитическим стрептококком, но казуистичность таких наблюдений подчеркивает их второстепенную роль.
Частота возникновения нефрита у больных ангиной, даже при не леченой ангине, в значительной мере может варьировать в зависимости от серотипа стрептококка, вызвавшего ангину. В настоящее время можно считать доказанным, что особенной «нефритогенностью» обладает 12-й серотип стрептококка группы A, за ним идут 4-й и 25-й серотипы. Этим объясняется то обстоятельство, что еще до антибиотикотерапии частота осложнения скарлатины нефритом колебалась в различных эпидемиях от 1 до 80%.
Что же касается патогенеза осложнений со стороны почек и мочевыводящих путей у больных ангиной и хроническим тонзиллитом, то ограниченный объем монографии не позволяет обсудить их подробно. Укажем лишь, что гломерулонефрит сегодня также представляется инфекционно-аллергическим заболеванием стрептококковой этиологии. Большой процент выздоровления (до 90% по некоторым авторам) и редкость повторных заболеваний в случае полного выздоровления от острого гломерулонефрита объясняются стойкостью антистрептококкового иммунитета у перенесших острый диффузный гломерулонефрит, что, в свою очередь, как думают, обязано ограниченности числа «нефритогенных» серотипов стрептококка группы А и, следовательно, меньшей вероятности суперинфекции другим «нефритогенными» серотипом стрептококка.
Все это мы говорим потому, что большое внимание, которое совершенно оправданно уделяется сегодня нефриту, должно быть обязательно дополнено пристальным вниманием к тем больным, которые являются «поставщиками» нефритов острых и хронических, явных и скрытых. И речь идет здесь не столько о внимании к таким больным в научно-исследовательском плане (литературы по данному вопросу много!), сколько в плане практическом, организационном. О том, что ни один больной с активным хроническим тонзиллитом не должен оставаться без квалифицированного и тщательного терапевтического обследования; что терапевт должен стать, наряду с ларингологом, одной из ведущих фигур в лечении хронического тонзиллита. А в процессе терапевтического обследования лабораторно-инструментальные методы исследования мочевыводящей системы и почек должны занять видное (а порой и главное) место, ибо почечная патология длительное время протекает у таких больных латентно, без клинических проявлений. Ясно, что большим комплексом лабораторных исследований трудно охватить всех больных хроническим тонзиллитом, а потому подчеркиваем, что должны быть выделены из этой группы больные с токсико-аллергическими (субкомпенсированный и декомпенсированный) формами заболевания. Но и само разделение на эти формы не может быть проведено с успехом без участия терапевта.
Коротко о значении лечения ангины и хронического тонзиллита в профилактике и лечении почечных осложнений у них.
Как уже было показано, своевременное эффективное антимикробное лечение больных ангиной практически гарантирует от почечных осложнений, а в случае их раннего возникновения (первый-второй дни болезни) обеспечивает успешное лечение данного осложнения. Что же касается значения радикального лечения хронического тонзиллита, то профилактическое его значение не вызывает сомнения, лечебное же не является абсолютным. М. Г. Григ сообщает, что после тонзиллэктомии у 102 (81,6%) больных возникло кратковременное обострение нефрита, но затем у 64,6% наступило выздоровление, у 16,7% — улучшение, и только у 14,7% течение нефрита не изменилось. Отсюда можно было бы сделать вывод, что тонзиллэктомия оказывает не только профилактический, но и довольно высокий терапевтический эффект при наличии у больного хронического тонзиллита и нефрита. Однако это не совсем так. Автор пишет, что выздоровление чаще наблюдалось при остром диффузном и очаговом нефрите, чем при хроническом. А ведь острый нефрит излечивается и без дополнительного вмешательства в 80-90% случаев.
Автор приходит к справедливому заключению, что тонзиллэктомия не является средством лечения нефрита, но она способствует эффективности медикаментозного, диетического и климатического лечения.
источник
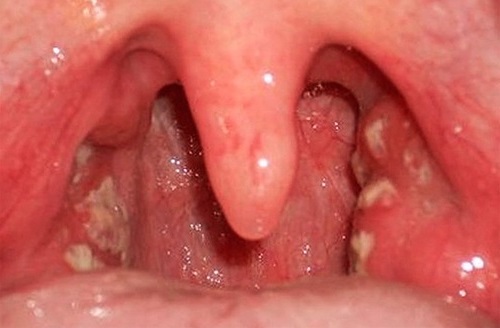

 Лихорадка. Продолжается не больше недели. Сопровождается ознобом.
Лихорадка. Продолжается не больше недели. Сопровождается ознобом. Режим — постельный.
Режим — постельный.