Развитие большинства почечных патологий отличается тем, что они могут иметь довольно продолжительный латентный (скрытый) период. Поэтому такой анализ как определение белка в моче несомненно является важнейшим для врачей многих специальностей.
При ультрафильтрации в состав первичной мочи попадает большое количество различных белковых молекул и аминокислот. Оно и не удивительно, для большинства белок средний размер превышает порог прохождения через мембраны. А молекулы аминокислот являются полярно заряженными. Это также играет роль при их «задержании» на поверхности мембран. Однако в процессе прохождения первичной мочи по канальцам нефрона практически все белки и аминокислоты реабсорбируются (подвергаются обратному всасыванию) в кровь. Из-за чего, вторичная моча может содержать не более сотых доле грамма протеинов.
Нормальные цифры, при определении белка в моче стандартными методами не должны превышать 0,033 грамма на один литр. За сутки же взрослый здоровый человек может выделять до 0,15 грамм. Причем около 1−2% из них являются альбуминами. Остальные же 90% приходятся на белки плазмы (их насчитывает около 30-ти видов) и гликопротеины — основные белки мембран. Последние появляются в моче за счет деятельности подоцитов. Так как, что при работе любой клетки неизбежно постоянное повреждение мембраны. Но это повреждений, во-первых не существенны, а во-вторых они быстро «затягиваются» благодаря постоянным процессам ее регенерации. Так же в эти 90% входят мукопротеиды — белковые молекулы, попадающие в просвет канальцев при работе эпителия петли Генле.
Различают несколько видов протеинурии. Они строятся только на основании анализа мочи на суточный белок.
- Нормальная протеинурия. Выделение белка не превышаетуже известных 0,15 грамм за сутки.
- Умеренная протеинурия. Выставляется при выделении более 0,15, но менее 3,5 грамм за сутки.
- Массивная протеинурия означает, что почками выделяется более 3,5 грамм белковых молекул за 24 часа.
Согласно основным механизмам ультрафильтрации и реабсорбции, превышений количества белка, выделяемого мочой, может явиться результатом поражения канальцев, клубочков и мочевыводящих путей.
- Поражение клубочков. Приводит к так называемой клубочковой протеинурии. При нормальных условиях, белки задерживаются мембраной. Только небольшое количество может проходить через ее поры. Поэтому у канальцев не предусмотрено наличие специальных механизмов реабсорбции белков, которые туда практически не попадают. Здесь речь идет об альбуминах. Они хотя и задерживаются мембранами подоцитов, но в состав первичной мочи попадает не более 2%, так как благодаря своему отрицательному заряду они задерживаются у базальных мембран и не попадают в Полость капсулы нефрона. Однако при разрушении мембраны, альбумины устремляются в полость капсулы и из канальцев уже не реабсорбируются. Именно поэтому при клубочковой патологии отмечается небольшая степень протеинурии: удельный вес альбуминов не позволяет сильнее реагировать индикаторам, которые используются для определения белка в моче.
- Патология канальцев. Здесь ультрафильтрация не нарушена. На так как страдает реабсорбция абсолютная степень протеинурии будет значительно за счет того, что в состав вторичной мочи входит большое количество грубодисперсных белков. Но и здесь необходимо оговориться, что для ее определения необходимы более чувствительные индикаторы. Так как действие большинства из них направлено на определение количества заряженных белковых частиц. Коими являются в первую очередь альбумины и которые при данных ситуациях повышаются не значительно, или во все находятся в пределах нормы. В связи с чем анализ мочи на общий белок может давать ложные результаты о реальных размерах протеинурии.
Это важно! Основным способом для регистрации протеинурии является тест на белок в моче. Для чего используются специальные индикаторы. Минимальным порогом для чувствительности большинства таких индикаторных палочек является значение в 30 миллиграмм на литр.
Однако и здесь необходимо помнить, что тест-полоск чувствительна к концентрации белка в пределах сотых долей миллиметра от ее поверхности. Поэтому при очень разбавленной моче полоска покажет отрицательный результат, даже если протеинурия составит больше 50 или даже 70 мг.
Для того чтобы избежать подобных «недочетов» лабораторных методов диагностики, исследование мочи лучше всего проводить утром, когда ее концентрация является наибольшей. Если же при общем анализе выявлена протеинурия более 0,033 г/л, для ее подтверждения проводиться исследование на суточное содержание белка.
источник
В последнее время в отечественной литературе достаточно часто обсуждается вопрос: что считать протеинурией? Если раньше протеинурией называли просто обнаружение белка в моче обычными качественными или количественными методами, чувствительность и специфичность которых была не очень высока, то сейчас, учитывая все большее внедрением в практику более чувствительных и специфичных методов, о протеинурии говорят, когда уровень белка в моче превышает норму. Варьирует и понятие нормы белка в моче – что связано с использованием как старых, так и новых методов определения белка в моче, которые отличаются чувствительностью и специфичностью. Некоторые авторы, учитывая наличие белка в моче и у здорового человека, понимают под термином протеинурия вообще выделение белка с мочой и для простоты делят протеинурию на физиологическую и патологическую, что сейчас также дискутируется. Обычно под термином протеинурия понимается увеличение содержания белка в моче.
В большинстве лабораторий при исследовании мочи «на белок» сначала пользуются качественными реакциями, которые не обнаруживают белок в моче здорового человека. Если же белок в моче обнаружен качественными реакциями, проводят количественное (или полуколичественное) его определение. При этом имеют значение особенности используемых методов, охватывающих различный спектр уропротеинов. Так, при определении белка с помощью 3% сульфосалициловой кислоты, нормальным считается количество белка до 0,03 г/л, при использовании же пирогаллолового метода, граница нормальных значений белка повышается до 0,1 г/л. В связи с этим в бланке анализа необходимо указывать нормальное значение белка для того метода, которым пользуется лаборатория.
При определении минимальных количеств белка рекомендуется повторить анализ, в сомнительных случаях следует определять суточную потерю белка с мочой. В норме суточная моча содержит белок в незначительных количествах. В физиологических условиях профильтровавшийся белок практически полностью реабсорбируется эпителием проксимальных канальцев и содержание его в суточном количестве мочи колеблется по разным авторам от следов до 20 – 50, 80 – 100 мг и даже до 150 – 200 мг. Некоторые авторы считают, что суточная экскреция белка в количестве 30 – 50 мг/сут является физиологической нормой для взрослого человека. Другие полагают, что выделение белка с мочой не должно превышать 60 мг/м2 поверхности тела в сутки, исключая первый месяц жизни, когда величина физиологической протеинурии может в четыре раза превышать указанные значения.
Общим условием появления белков в моче здорового человека являются достаточно высокая их концентрация в крови и молекулярная масса не более 100 – 200 кДа.
У практически здоровых людей под воздействием различных факторов может появляться преходящая протеинурия. Такую протеинурию называют также физиологической, функциональной или доброкачественной, так как она, в отличие от патологической, не требует лечения.
Преходящее выделение белка с мочой у здоровых людей может появляться после тяжелой физической нагрузки (длительные походы, марафонский бег, игровые виды спорта). Это так называемая рабочая (маршевая) протеинурия или протеинурия напряжения, наблюдавшаяся и описанная многими исследователями. Работы этих авторов, иллюстрирующие возможность развития протеинурии под влиянием физической нагрузки, свидетельствуют о высокой степени ее выраженности, а также ее обратимости. Генез такой протеинурии объясняют гемолизом с гемоглобинурией и стрессовой секрецией катехоламинов с преходящим нарушением гломерулярного кровотока. При этом протеинурия выявляется в первой после физической нагрузки порции мочи.
Значение фактора охлаждения в генезе скоропреходящей протеинурии было отмечено у здоровых людей под влиянием холодных ванн.
Известна albuminuria solaris, возникающая при выраженной реакции кожи на инсоляцию, а также при раздражении кожи некоторыми веществами, например, при смазывании ее йодом.
Установлена возможность появления протеинурии при повышении уровня адреналина и норадреналина в крови, чем объясняют выделение белка с мочой при феохромоцитоме и гипертонических кризах.
Выделяют алиментарную протеинурию, появляющуюся иногда после употребления обильной белковой пищи.
Доказана возможность появления центрогенной протеинурии – при эпилепсии, сотрясении мозга.
Описана эмоциональная протеинурия во время экзаменов.
К протеинурии функционального происхождения относят и описываемое некоторыми авторами выделение белка с мочой при энергичной и продолжительной пальпации живота и области почек (пальпаторная протеинурия).
Лихорадочная протеинурия наблюдается при острых лихорадочных состояниях, чаще у детей и стариков. Механизм ее малоизучен. Этот вид протеинурии сохраняется в период повышения температуры тела и исчезает при ее снижении и нормализации. Если протеинурия сохраняется в течение многих дней и недель после нормализации температуры тела, то следует исключить возможное органическое заболевание почек — либо вновь возникшее, либо уже существующее.
При заболеваниях сердца часто выявляют застойную, или сердечную протеинурию. С исчезновением сердечной недостаточности она обычно исчезает.
У новорождённых в первые недели жизни также наблюдается физиологическая протеинурия.
Ортостатическая (постуральная, лордотическая) протеинурия наблюдается у 12 – 40% детей и подростков, характеризуется выявлением белка в моче при длительном стоянии или ходьбе с быстрым исчезновением (преходящий вариант ортостатической протеинурии) или уменьшением его (персистирующий вариант) в горизонтальном положении. Генез ее связывают с нарушениями почечной гемодинамики, развивающимися за счет лордоза, сдавливающего нижнюю полую вену в положении стоя, или выброса ренина (ангиотензина II) в ответ на изменения объема циркулирующей плазмы при ортостатизме.
Физиологическая протеинурия, как правило, незначительная – не более 1,0 г/сут.
Современные методы исследования позволяют выявить ряд изменений в микроструктуре почек, следствием которых и является так называемая физиологическая протеинурия. Исходя из таких соображений, многие авторы сомневаются в правомочности выделения «функциональной» протеинурии.
Патологическая протеинурия бывает почечного и внепочечного происхождения.
Почечная протеинурия является одним из наиболее важных и постоянных признаков заболеваний почек и может быть гломерулярной, или клубочковой, и тубулярной, или канальцевой. При сочетании этих двух типов развивается смешанный тип протеинурии.
Клубочковая протеинурия обусловлена повреждением гломерулярного фильтра, возникает при гломерулонефритах и при нефропатиях, связанных с обменными или сосудистыми заболеваниями. При этом из крови в мочу в большом количестве фильтруются плазматические белки.
В основе нарушения работы клубочкового фильтра лежат различные патогенетические механизмы:
- токсические или воспалительные изменения гломерулярной базальной мембраны (отложение иммунных комплексов, фибрина, клеточная инфильтрация), вызывающие структурную дезорганизацию фильтра;
- изменения гломерулярного кровотока (вазоактивные агенты – ренин, ангиотензин II, катехоламины), влияющие на гломерулярное транскапиллярное давление, процессы конвекции и диффузии;
- недостаток (дефицит) специфических гломерулярных гликопротеидов и протеогликанов, ведущий к потере фильтром отрицательного заряда.
Клубочковая протеинурия наблюдается при остром и хроническом гломерулонефрите, амилоидозе, диабетическом гломерулосклерозе, тромбозе почечных вен, застойной почке, гипертонической болезни, нефросклерозе.
Клубочковая протеинурия может быть селективной и неселективной в зависимости от тяжести повреждения гломерулярного фильтра.
Селективная протеинурия встречается при минимальном (нередко обратимом) повреждении гломерулярного фильтра (нефротический синдром с минимальными изменениями), представлена белками с молекулярной массой не выше 68000 – альбумином и трансферрином.
Неселективная протеинурия чаще встречается при более тяжелом повреждении фильтра, отличается повышением клиренса средне- и высокомолекулярных плазматических белков (в составе белков мочи присутствуют также альфа2-глобулины и гамма-глобулины). Неселективная протеинурия наблюдается при нефротической и смешанной формах гломерулонефрита, вторичном гломерулонефрите.
Канальцевая протеинурия связана либо с неспособностью канальцев реабсорбировать белки, прошедшие через неизмененный гломерулярный фильтр, либо обусловлена выделением белка эпителием самих канальцев.
Канальцевая протеинурия наблюдается при остром и хроническом пиелонефрите, отравлении тяжелыми металлами, остром канальцевом некрозе, интерстициальном нефрите, хроническом отторжении почечного трансплантата, калийпенической нефропатии, генетических тубулопатиях.
Внепочечная протеинурия возникает при отсутствии патологического процесса в самих почках и делится на преренальную и постренальную.
Преренальная протеинурия развивается при наличии необычно высокой плазматической концентрации низкомолекулярного белка, который фильтруется нормальными клубочками в количестве, превышающем физиологическую способность канальцев к реабсорбции. Подобный тип протеинурии наблюдается при миеломной болезни (в крови появляется низкомолекулярный белок Бенс-Джонса и другие парапротеины), при выраженном гемолизе (за счет гемоглобина), рабдомиолизе, миопатии (за счет миоглобина), моноцитарном лейкозе (за счет лизоцима).
Постренальная протеинурия обусловлена выделением с мочой слизи и белкового экссудата при воспалении мочевых путей или кровотечением. Заболевания, которые могут сопровождаться внепочечной протеинурией — мочекаменная болезнь, туберкулез почки, опухоли почки или мочевых путей, циститы, пиелиты, простатиты, уретриты, вульвовагиниты. Постренальная протеинурия чаще весьма незначительна и практически менее важна.
В зависимости от степени выраженности выделяют легкую, умеренную и тяжелую протеинурию.
Легкая протеинурия (от 300 мг до 1 г/сут) может наблюдаться при острой инфекции мочевыводящих путей, обструктивной уропатии и пузырно-мочеточниковом рефлюксе, тубулопатиях, мочекаменной болезни, хроническом интерстициальном нефрите, опухоли почки, поликистозе.
Умеренная протеинурия (от 1 до 3 г/сут) отмечается при остром канальцевом некрозе, гепаторенальном синдроме, первичном и вторичном гломерулонефрите (без нефротического синдрома), протеинурической стадии амилоидоза.
Под тяжелой, или выраженной протеинурией понимают потерю белка с мочой, превышающую 3,0 г в сутки или 0,1 г и более на килограмм массы тела за 24 часа. Такая протеинурия почти всегда связана с нарушением функции клубочкового фильтрационного барьера в отношении размера или заряда белков и наблюдается при нефротическом синдроме.
Выявление и количественная оценка протеинурии важны как для диагностики, так и для оценки течения патологического процесса, эффективности проводимого лечения. В заключении необходимо отметить, что диагностическая значимость протеинурии оценивается в совокупности с другими изменениями в моче.
- Л. В. Козловская, А. Ю. Николаев. Учебное пособие по клиническим лабораторным методам исследования. Москва, Медицина, 1985 г.
- А. В. Папаян, Н. Д. Савенкова «Клиническая нефрология детского возраста», Санкт-Петербург, СОТИС, 1997 г.
- Куриляк О.А. «Белок в моче – методы определения и границы нормы (современное состояние проблемы)»
- А. В. Козлов, «Протеинурия: методы ее выявления», лекция, Санкт-Петербург, СПбМАПО, 2000 г.
- В. Л. Эмануэль, «Лабораторная диагностика заболеваний почек. Мочевой синдром», — Справочник заведующего КДЛ, № 12, декабрь 2006 г.
- О. В. Новоселова, М. Б. Пятигорская, Ю. Е. Михайлов, «Клинические аспекты выявления и оценки протеинурии», Справочник заведующего КДЛ, № 1, январь 2007 г.
Патологическая протеинурия является одним из наиболее важных и постоянных признаков заболеваний почек и мочевых путей. Определение концентрации белка в моче является обязательным и важным элементом исследования мочи.
Раздел: Анализ мочи
Для количественного определения белка пригоден любой образец мочи. Большинство исследователей для выяснения величины суточной потери белка предпочитают определять содержание белка в моче, собранной за сутки.
Раздел: Анализ мочи
Все качественные пробы на белок в моче основаны на способности белков к денатурации под влиянием различных физических и химических факторов. При наличии белка в исследуемом образце мочи появляется либо помутнение, либо выпадение хлопьевидного осадка.
Раздел: Анализ мочи
В настоящее время для определения белка в моче все чаще используются диагностические полоски. Для полуколичественного определения белка в моче на полоске в качестве индикатора чаще всего используется краситель бромфеноловый синий в цитратном буфере. О содержании белка в моче судят по интенсивности сине-зеленой окраски, развивающейся после контакта реакционной зоны с мочой.
Раздел: Анализ мочи
Определение концентрации мочевины в моче проводится значительно реже, чем определение уровня мочевины в крови и используется обычно при при обнаружении повышенного уровня мочевины в крови и решении вопроса о состоянии выделительной функции почек. При этом определяют суточную экскрецию мочевины с мочой. Повышенное содержание мочевины крови при снижении суточной экскреции с мочой чаще свидетельствует о нарушении азотовыделительной функции почек.
Раздел: Клиническая биохимия
источник
В моче исследуют рН, осмотическую концентрацию или относительную плотность, белки, глюкозу, осадок мочи и проводят микробиологические и биохимические исследования. Это – достаточно простые и информативные методы. Также следует знать современные дорогостоящие методы с высокими диагностическими возможностями, используемые в последние годы в развитых странах (протеомика мочи).
Общий анализ мочи (ОАМ) – наиболее часто используемый метод. В настоящее время количественные (Аддиса-Каковского, Амбурже) и полуколичественные (Нечипоренко) пробы признаны неудобными и не имеют преимуществ перед ОАМ. Суточный сбор мочи показан только для оценки суточной протеинурии при невозможности определения протеин/креатининового коэффициента. Для проведения анализа необходимо исследование утренней свежевыпущенной мочи со средней порции без применения стабилизаторов с целью уменьшения вероятности ошибок, связанных с бактериальным разложением и другими факторами. Можно исследовать вторую и последующие порции мочи, полученные в течение дня.
Экономичным и точным методом скринингового исследования мочи является применение тест-полосок (качественный анализ). В случае отсутствия гематурии/ гемоглобинурии или лейкоцитурии, протеинурии, глюкозурии, необходимость в микроскопическом исследовании мочи отпадает. При обнаружении хотя бы одной из вышеуказанных патологических находок необходимы дальнейшие количественные биохимические и микроскопические исследования.
Глюкозурия обычно свидетельствует о гипергликемии, однако может носить и изолированный характер (почечная глюкозурия) или сочетаться с нарушениями других функций проксимальных почечных канальцев (синдром Фанкони). Глюкозурия иногда встречается при нефротическом синдроме и на фоне стероидной терапии.
Протеинурия– один из главных признаков заболевания почек, маркер локализации и тяжести почечного повреждения. Однако, следует помнить, что при таких состояниях, как лихорадка, значительная физическая нагрузка, хроническая сердечная недостаточность и инфекция мочевой системы, может иметь место транзиторное (преходящее) повышение альбумина в моче.
В норме с мочой выделяются различные белки (альбумин, глобулин и др.), количество которых незначительно. Суточная протеинурия в норме не превышает 150мг/сут. Рутинные методы исследования (тест-полоски, проба с сульфосалициловой кислотой) не выявляют выделяющиеся в норме белки. При патологии уровень протеинурии растет. Поэтому диагностическое значение имеет определение суточного количества белка в моче, а также электрофоретическая дифференциация видов белка (альбумин, α1, α2 -микроглобулин, β2-микроглобулин, белок Тамма-Хорсфаля и др.). При качественной пробе (тест-полоски) используется шкала:
Таким образом, диагностические полоски на протеинурию позволяют выявить содержание белка 300 мг/л и выше. При этом преимущественно определяется альбумин. При положительном результате (желательно повторить анализ) следует перейти на количественное определение белка.
Для нивелирования различной концентрации веществ в моче используют определение суточной протеинурии. Для этого собирают суточную мочу и производят пересчет концентрации белка в моче (г/л) на суточный диурез (г/сут). Более удобен новый метод вычисления протеин/креатининового коэффициента, который позволяет определить суточную экскрецию белка без сбора 24-часовой мочи. Принцип основан на том, что креатинин выделяется путем клубочковой фильтрации и экскреция его постоянна в течение суток. С помощью вычисления отношения концентрации любого вещества (включая белок) в моче к уровню креатинина в моче, можно определить суточную экскрецию этих веществ (Na, K, Ca и др., табл.5). концентрация веществ и креатинина может выражаться в ммоль, мг или г/л.
При расчете суточной протеинурии чаще белок определяют в мг или г, а креатинин в ммоль. Оба вещества могут определяться в г/л. В зависимости от этого протеин/креатининовый коэффициент в норме равен:
у взрослых 2 лет
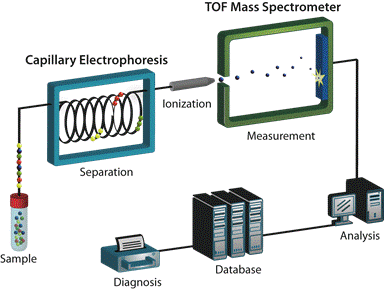 | Рисунок 2.Капиллярный электрофорез on-line с масс-спектрометром (CE-MS) |
Внедрение этого дорогостоящего метода в будущем позволит дифференцировать такие болезни, как Ig A нефропатия, фокально-сегментарный гломерулосклероз без биопсии почек.
При заболеваниях почек, связанных с гематологическими, онкологическими болезнями, увеличивается экскреция парапротеинов с мочой. Парапротеины появляются в избыточном количестве при множественной миеломе, амилоидозе, макроглобулинемии Вальденстрема (протеинурия переполнения). Одним из них является белок Бенс-Джонса. Он не определяется обычными тест-полосками и требует специального исследования легких цепей иммуноглобулинов. Свойством белка Бенс-Джонса является осаждение при термической обработке сульфосалициловой кислотой.
Экскреция химических веществ в моче.Также определяется с использованием креатининового коэффициента (КК). Уровень экскреции химических веществ с мочой зависит от возраста детей и для правильной оценки рекомендуется руководствоваться нормативами (табл.5).
Таблица 5:Экскреция веществ с мочой по креатининовому коэффициенту в возрастном аспекте (95-й перцентиль) [по данным Matos V. с соавт., J. Pediatr. (1997)131:252–257].
| Вещество/ Креатинин, ммоль/ммоль | Возраст, г | |||||||
| 1/12 -1 | 1 – 2 | 2 – 3 | 3 – 5 | 5 – 7 | 7 – 10 | 10 – 14 | 14 – 17 | |
| Натрий / креатинин | ||||||||
| Калий / креатинин | ||||||||
| Кальций/ креатинин | 2,2 | 1,5 | 1,4 | 1,1 | 0,8 | 0,7 | 0,7 | 0,7 |
| Магний / креатинин | 2,2 | 1,7 | 1,6 | 1,3 | 1,0 | 0,9 | 0,7 | 0,6 |
| Фосфат / креатинин | 3,6 | 3,2 | 2,7 | |||||
| Оксалат / креатинин | 0,17 | 0,13 | 0,1 | 0,08 | 0,07 | 0,06 | 0,06 | 0,06 |
| Мочевая кислота/ креатинин | 1,5 | 1,4 | 1,3 | 1,1 | 0,8 | 0,56 | 0,44 | 0,4 |
Большинство детей старше 2-х лет при нормальном питьевом режиме имеют уровень креатинина мочи 5±4 ммоль/л. Может быть ошибка «разведения мочи», когда креатинин мочи составляет около 2 ммоль/л или «концентрирования мочи» при концентрации около 12 ммоль/л. При концентрации альбумина в моче 1 г/л, то есть при 50-кратном его повышении, расчет КК не требуется. КК всех веществ у грудных детей выше, чем у старших детей. Это связано не с повышенной их экскрецией, а со сниженной экскрецией креатинина из-за малой мышечной массы. Норма КК у новорожденных детей в 4 раза выше, чем у старших детей. При определении КК необходимость в определении суточной экскреции веществ отпадает.
Для правильной интерпретации экскреции электролитов (Na, K, Ca, Mg, Cl, P) с мочой важно знать их уровни в сыворотке крови и суточный прием. Учесть последний фактор удается редко, за исключением случаев парентерального введения электролитов. Например, при гипокалиемии 3.0 ммоль/л калийурия — 20 ммоль/л свидетельствует о почечной потере калия. При гиперкалиемии 6.5 ммоль/л калийурия — 20 ммоль/л – признак почечной недостаточности с задержкой калия, так как здоровые почки должны экскретировать калий в повышенных количествах – около 80 ммоль/л и выше. Особое внимание необходимо обращать на экскрецию кальция, так как ее повышение сопряжено с высоким риском нефрокальциноза и нефролитиаза. Определение экскреции органических кислот (цитраты, оксалаты, ураты) проводится при подозрении на гипероксалурию, гипо- или гиперцитратурию, гипоурикозурию. Это исследование выполняется в специальных лабораториях (дорогостоящий метод).
Для определения рН и относительной плотности мочи используются рутинные методы. Точное определение рН (рН-метрия) имеет значение при нарушении экскреции водородных ионов (первичные и вторичные тубулопатии), процессах камнеобразования и инфекциях мочевых путей.
Дата добавления: 2015-07-14 ; просмотров: 1032 ; ЗАКАЗАТЬ НАПИСАНИЕ РАБОТЫ
источник

В процессе выполнения своей основной функции почки отфильтровывают из кровотока небольшое количество белка. Так он оказывает в первичной моче.
Далее запускается механизм обратного всасывания белка в почечных канальцах. Результатом функционирования здоровых почек и отсутствия избытка белков в плазме крови становится наличие во вторичной моче (жидкости, которая выводится из организма) небольшого количества белка.
Лабораторное исследование мочи не определяет протеины в такой концентрации, либо дает результат 0,033 г/л.
Превышение этого значения и называется протеинурией – содержанием в урине белка в большом количестве. Это состояние является поводом для дальнейшей диагностики с целью выявления причин нарушения.
В зависимости от источника появления белка в урине можно выделить следующие типы нарушения:
- Ренальную (почечную) – при которой избыток протеина образуется при дефектах клубочковой фильтрации (клубочковая или гломерулярная протеинурия), либо при нарушении обратного всасывания в канальцах (канальцевая или тубулярная).
- Преренальную – возникающую при неадекватно высоком формировании в плазме крови белковых соединений. Здоровые почечные канальцы не в состоянии осуществить всасывание такого количества белков. Также может возникать при искусственном введении альбумина на фоне нефротического синдрома.
- Постренальную – обусловленную воспалением органов нижнего отдела мочеполовой системы. Белок попадает в мочу, вышедшую из почечного фильтра (отсюда и название – дословно «после почек»).
- Секреторную – характеризующуюся выделения ряда специфических белков и антигенов на фоне некоторых заболеваний.
Все перечисленные механизмы попадания протеина в мочу характерны для протекания в организме патологического процесса, поэтому такие протеинурии называют патологическими.
Функциональные протеинурии – это чаще всего эпизодическое явление, не сопровождаемое заболеваниями почек или мочеполовой системы. К ним относят следующие формы нарушения:
- Ортостатическая (лордотическая, постуральная) – появление белка в моче у детей, подростков или молодых людей астенического телосложения (часто на фоне поясничного лордоза) после длительной ходьбы или нахождения в статичном вертикальном положении.
- Алиментарная – после употребления белковой пищи.
- Протеинурия напряжения (рабочая, маршевая) – имеет место при условии обширных физических нагрузок (например, у спортсменов или военнослужащих).
- Лихорадочная – возникает в результате усиления процессов распада в организме или повреждения почечного фильтра при повышении температуры тела выше 38 градусов.
- Пальпаторная – может появляться на фоне длительной и интенсивной пальпации области живота.
- Эмоциональная – диагностируется во время сильного стресса или выступает его последствием. Сюда можно включить транзиторную форму, также связанную с шоковыми изменениями в организме при переохлаждении или тепловом ударе.
- Застойная – явление, сопровождающее аномально медленный кровоток в почках или кислородное голодание организма при сердечной недостаточности.
- Центрогенная – имеющая место при сотрясениях мозга или эпилепсии.
Появление протеинов в моче при функциональных формах может объясняться механизмами, сходными с патологическими формами. Разница лишь в преходящем характере и количественных показателях.
Стоит отметить, что две последних функциональные формы часто объединяют под название экстраренальной протеинурии, которую при этом включают в список патологических форм.
Исходя из обилия только основных видов функциональных форм, можно предположить, что разовое превышение количества белка в моче – не всегда необходимо и явно недостаточно для выявления устойчивой тенденции. Поэтому правильнее воспользоваться результатами анализа суточного диуреза.
При наличии ряда физиологических причин суточная норма также может быть превышена и у здоровых людей, для постановки диагноза нужно учесть жалобы пациента, а также другие количественные показатели анализа урины (эритроциты, лейкоциты, цилиндры).
Общая норма суточного белка для взрослых – 0,15 г/сутки, а согласно иным справочным данным – 0,2 г/сутки (200 мг/сутки) либо меньшее значение – 0,1 г/сутки.
Эти цифры, впрочем, справедливы только для 10-15 % населения, у подавляющего большинства с уриной выделяется всего 40-50 мг протеина.
При беременности возрастает объем кровотока в почках, соответственно увеличивается и количество отфильтрованной крови. Это учитывается при расчете нормы протеина. Непатологический показатель у беременных женщин – менее 0,3 г/сутки (150-300 мг/сутки).
Нормы у детей можно представить в форме таблицы:
| Возраст | Потеря белка с мочой в сутки |
|---|---|
| Новорожденные | 14-60 мг/сутки |
| 2-12 месяцев | 17-86 мг/сутки |
| 2-4 года | 20-120 мг/сутки |
| 4-10 лет | 26-195 мг/сутки |
| 11-16 лет | 29-240 мг/сутки |
Некоторое отклонение от нормы (в стороны повышения) может наблюдаться у детей в первую неделю жизни.
При любых видах функциональной протеинурии количественный показатель редко превышает 2 г/сутки, а чаще – 1 г/сутки. Аналогичные значения могут наблюдаться и при некоторых патологиях, здесь важно провести дополнительные исследования и осмотр пациента. Исключение – беременные женщины, у которых суточный показатель более 0,3 г/сутки уже позволяет с высокой вероятностью заподозрить наличие осложнений протекания беременности.
Общий список заболеваний, признаком которых является наличие протеина в моче удобно рассматривать в соответствии с патологическими формами. Преренальная форма протеинурии может возникать на фоне:
- некоторых видов системных и регионарных гемобластозов – злокачественных изменений кроветворной и лимфатической ткани (в том числе миеломной болезни);
- заболеваний соединительной ткани – нарушений аллергической природы, при которых происходит поражение различных (от 2-х) систем организма;
- рабдомиолиза – состояния, характеризующегося разрушением мышечной ткани и резким повышением концентрации в крови белка миоглобина;
- макроглобулинемии – заболевания, при котором злокачественно измененные клетки плазмы начинают выделять вязкий белок – макроглобулин;
- гемолитической анемии – сопровождающейся распадом эритроцитов и выходом в кровь большого количества белка гемоглобина (может происходить в связи с отравлением специфичными ядами);
- переливания несовместимой крови или приема медикаментов (сульфаниламидов);
- наличия в организме метастаз или опухолей, локализующихся в брюшной полости;
- отравления;
- эпилептического припадка или черепно-мозговой травмы, в том числе сопровождающейся кровоизлиянием в мозг.
Причинами возникновения ренальной формы являются непосредственно почечные патологии:
- гломерулонефрит – характеризующийся поражением клубочкового аппарата почек, а в некоторых случаях и отмиранием тканей канальцев;
- диабетическая нефропатия – нарушение работы почек, возникающее на фоне изменений метаболизма жиров и углеводов при повышенном давлении;
- гипертонический нефросклероз – «сморщивание» почечной ткани как результат поражения сосудов на фоне высокого давления;
- почечные новообразования;
- амилоидоз – отложение в почках белковых комплексов – амилоидов;
- мочекаменная болезнь;
- воспалительные заболевания почек, в частности интерстициональный нефрит – воспаление соединительной ткани канальцев.
Постренальная протеинурия может быть симптомом:
- воспалительных заболеваний нижнего отдела мочеполовой системы – мочевого пузыря, уретры, половых органов;
- кровотечений из уретры;
- туберкулеза почек;
- доброкачественных новообразований мочевого пузыря (полипы) и мочевыводящих путей.
Во всех перечисленных (постренальных) случаях повреждаются клетки эпителия слизистой оболочки. Их разрушение высвобождает протеины, которые и обнаруживаются в урине.
Протеинурия у детей также может развиваться при наличии ряда перечисленных причин. При этом специфичным для малышей будет возникновение избытка протеина на фоне:
- гемолитической болезни новорожденных – разновидности гемобластоза, спецификой которой является несовместимость крови матери и плода. Патология может начать развиваться еще во внутриутробном периоде жизни эмбриона;
- голодании или нарушении режима питания;
- переизбытке витамина D;
- аллергии.
Повышение количества белка в урине при беременности также может иметь ряд дополнительных причин:
- нефропатия беременных;
- токсикоз (в первом триместре) – нарушение водно-солевого баланса на фоне обезвоживания, приводящее к изменению общего метаболизма;
- гестоз (преэклампсия) – осложненно протекающая беременность, сопровождающаяся гипертензией, судорогами, отеками, протеинурией. Обычно состояние диагностируют во 2 и 3 триместре.
Общие признаки того, что имеет место потеря белка с мочой, следующие:
- отечные проявления, в частности утренний отек век;
- появление на поверхности урины белесой пены либо грязно-белых хлопьев.
Дифференцированные признаки могут включать как симптомы потери определенного типа протеиновых соединений, так и симптомы заболевания-первопричины протеинурии. В числе первых:
- общее снижение иммунитета;
- анемические проявления;
- склонность к кровотечениям;
- слабость, снижение мышечного тонуса;
- гипотиреоз.
Ко вторым можно отнести, главным образом, признаки, указывающие на наличие почечных патологий:
- боль в почках, в том числе колики;
- дискомфорт при мочеиспускании;
- повышение давления;
- высокая температура, озноб, мышечные боли;
- слабость, сухость кожных покровов;
- изменение цвета, консистенции или запаха урины;
- расстройства диуреза.
Однако основным источником информации для постановки диагноза и определения причины избытка протеина служат лабораторные исследования.
После разового выявления протеинурии в результате общего анализа мочи следует дифференцировать функциональную и патологическую формы. Для этого могут потребоваться:
- сбор жалоб пациента, выяснение наличия факторов, могущих спровоцировать эпизодическое повышение уровня белка;
- ортостатическая проба – проводится у детей и подростков.
Если есть подозрение на сопутствующую патологию, то назначаются:
- анализ на суточный белок;
- пробы на специфичные белки (Бенс-Джонса);
- осмотр уролога или гинеколога;
- УЗИ почек, мочевого пузыря, органов половой сферы (при наличии показаний).
Далее проводятся более узконаправленные тесты:
Естественно, комплекс дополнительных обследований может значительно расширяться, соответственно тому, что вызывать протеинурию могут самые различные заболевания, выступая в качестве первичной/вторичной причины повышения уровня протеина.
Особых мер не потребуется, однако некоторые нюансы стоит учесть:
- о приеме на постоянной основе любых медикаментов нужно предупредить врача, при необходимости согласовать с ним целесообразность их применения в день сдачи анализа;
- не менять питьевой режим, как до сбора мочи, так и во время него;
- не употреблять в пищу непривычных продуктов, следовать своему обычному рациону;
- исключить алкогольные напитки;
- за день до сдачи следует прекратить прием мочегонных средств, витамина С;
- избегать физических и нервных перегрузок;
- по возможности обеспечить организм полноценным сном.
Для получения адекватного результата анализа пациенту потребуется соблюсти такой алгоритм:
- Заранее подготовить (приобрести) стерильную емкость для сбора суточного объема урины.
- Первую порцию утренней мочи собирать не нужно.
- Теперь при каждом мочеиспускании урину следует добавлять в емкость, записывая время каждого диуреза. Хранить собранный объем только в холодильнике.
- Собирать нужно всю мочу, включая первую утреннюю порцию на следующий день после начала сбора (чтобы получить диурез за сутки).
- После окончания сбора зафиксировать полученный объем жидкости;
- Перемешать урину и перелить от 30 до 200 мл в отдельную стерильную емкость.
- Представить емкость в лабораторию, добавив зафиксированный график диуреза, а также указав итоговый объем полученной жидкости, свой рост и вес.
Незначительная протеинурия может корректироваться в домашних условиях с участием следующих мер:
- сведение к минимуму физических и эмоциональных стрессов;
- внесение изменений в рацион питания – потреблять меньше тяжелых протеинов (жирного мяса и рыбы, грибов, бобовых) и соли, при этом увеличить количество клетчатки – овощей, приготовленных на пару, фруктов, круп, хлеба и кисломолочных продуктов, молочных и овощных супов.
Диета при повышенном содержании белка предполагает также отказ от алкогольных напитков и приготовление пищи с малым количеством жира – варке или обработке на пару.
Известно множество народных средств, помогающих уменьшить количество протеина в моче, вот некоторое из них:
- настои из семян или корней петрушки, листьев брусники, березовых почек, толокнянки;
- отвары овса (зерен, а не хлопьев), зерен кукурузы либо коры пихты;
- отвар из тыквенных семян вместо чая;
- чаи и настои из клюквы;
- настои из липы и цедры лимона.
Рецепты отваров трав, коры деревьев и зерновых для питья:
- Чайную ложку измельченных семян петрушки заварить кипятком и настоять несколько часов. Принимать по несколько глотков в течение дня.
- Две столовые ложки березовых почек залить кипятком и настоять 1-2 часа. Принимать по 50 мл 3 раза в день.
- 4 столовые ложки кукурузных зерен отваривать в воде (около 0,5 литра) до размягчения. После процедить и пить в течение дня. Отвар не следует хранить дольше суток.
- 5 столовых ложек зерен овса варить в литре воды до размягчения, отвар принимать аналогично кукурузному.
При беременности диета не теряет своей актуальности, как и применение народных средств. А вот прием химических лекарственных средств должен происходить строго по назначению врача (хотя этой рекомендацией не стоит пренебрегать и в отсутствии беременности).
Важно понимать, что в домашних условиях можно бороться лишь с функциональным либо только начинающим развиваться расстройством. При массивных отклонениях от нормы в результате анализа мочи и выраженных симптомах перечисленные меры могут выступать как дополнение к основной медикаментозной терапии.
А вот последняя может быть представлена препаратами самых различных групп:
- статины последнего поколения – для лечения сахарного диабета и атеросклероза сосудов (некоторые статины, однако, могут сами способствовать протеинурии);
- ингибиторы АПФ и блокаторы ангиотензина – применяются при патологиях сердца, в частности, артериальной гипертензии;
- блокаторы кальциевых каналов – часто используются для лечения сочетания гипертензии с сахарным диабетом;
- противоопухолевые препараты – применяются при наличии доброкачественных или злокачественных новообразований;
- антибиотики и уросептики – назначаются при наличии воспалительного процесса и/или наличии инфекций;
- антикоагулянты – оказывают комплексное воздействие при остром гломерулонефрите и почечной недостаточности;
- негормональные иммунодепрессанты (цитостатики) – подавляют воспалительный аутоиммунный процесс при гломерулонефрите или нефротическом синдроме на фоне высокого давления;
- комплексные или узконаправленные средства для снижения отечности;
- гормональные препараты (кортикостероиды) – оказывают антиаллергическое и противовоспалительное действие, однако могут повышать артериальное давление.
Лечение тяжелой протеинурии, к тому же осложненной серьезным заболеванием, может потребовать сил и значительных временных затрат. Поэтому даже при эпизодическом появлении белка в моче не стоит пренебрегать диагностикой и применением «домашних» лечебных мер с целью профилактики развития патологий почек и организма в целом.
источник
Нормальные показатели: белок в норме в моче содержится в минимальных количествах, которые не обнаруживаются обычными качественными реакциями. Верхняя граница нормы белка в моче – 0,033 г/л. Если содержание белка выше этого значения, то качественные пробы на белок становятся положительными.
Клиническое значение определения:
Появление белка в моче называется протеинурия. Протеинурии могут быть ложными и почечными. Экстраренальные протеинурии могут быть при наличии примесей белкового происхождения из половых органов (вагинитах, уретритах и др.), количество белка при этом незначительно – до 0,01 г/л. Почечные протеинурии могут быть функциональными (при переохлаждении, физических нагрузках, лихорадке) и органическими — при гломерулонефрите, пиелонефрите, нефрите, нефрозах, почечной недостаточности. При почечных протеинуриях содержание белка может быть от 0,033 до 10 – 15 г/л, иногда выше.
Принцип метода: основан на том, что белок под действием неорганических кислот коагулирует (становится видимым). Степень помутнения зависит от количества белка.
Обнаружение белка в моче с 20% сульфосалициловой кислотой.
Реактивы: 20% р-р сульфосалициловой кислоты. Оборудование: темный фон.
1. Требования к моче: моча должна быть кислой (или слабокислой) рН, должна быть прозрачной, для этого мочу центрифугируют. Щелочную мочу подкисляют до слабокислой реакции среды, используя для контроля индикаторную бумагу.
2. В 2 пробирки одинакового диаметра наливают по 2 мл подготовленной мочи. 1 пробирка – контроль, 2 – опыт. В опытную пробирку добавляют 4 капли 20% сульфосалициловой кислоты.
3. Результат отмечают на темном фоне.
4. При наличии белка, моча в опытной пробирке мутнеет.
Качественное определение белка в моче тест – полосками.
Для выявления протеинурий используют различные монотест – полоски: Альбуфан, Альбустикс, Биофан Е и политесты: Трискан, Нонафан и др.
Обнаружение белка в моче по методу Робертса – Стольникова.
Принцип метода: основан на том, что белок под действием неорганических кислот коагулирует (становится видимым). Степень помутнения зависит от количества белка (т.е. кольцевая проба Геллера). При концентрации белка в моче 0,033 г/л к концу 3 минуты после наслаивания мочи появляется тонкое нитевидное белое кольцо.
Реактивы: 50% р-р азотной кислоты или реактив Робертса (98 частей насыщенного раствора поваренной соли и 2 части концентрированной соляной кислоты) или реактив Ларионовой (98 частей насыщенного р-ра поваренной соли и 2 части концентрированной азотной кислоты).
1. 
2. В пробирку наливают 2 мл 50% р-ра азотной кислоты или один из реактивов, затем осторожно по стенке пробирки с помощью пипетки наслаивают такой же объем подготовленной мочи
3. Пробу оставляют на 3 минуты
4. Через 3 минуты отчитывают результат. Результат отмечают на темном фоне в проходящем свете. Если кольцо широкое, компактное, то мочу разводят дистиллированной водой и вновь наслаивают на реактив.
5. Мочу разводят до тех пор, пока через 3 минуты не образуется тонкое нитевидное кольцо.
6. Расчет содержания белка в моче производят по формуле:
С = 0,033г/л х степень разведения.
Не нашли то, что искали? Воспользуйтесь поиском:
Лучшие изречения: Увлечёшься девушкой-вырастут хвосты, займёшься учебой-вырастут рога 9679 — 

195.133.146.119 © studopedia.ru Не является автором материалов, которые размещены. Но предоставляет возможность бесплатного использования. Есть нарушение авторского права? Напишите нам | Обратная связь.
Отключите adBlock!
и обновите страницу (F5)
очень нужно
источник
Мищерина Д.А., Насырова Ж.С., 3 курс
Научный руководитель – к.м.н., доц. М.А.Белова
Кафедра клинической лабораторной диагностики
Анализ содержания белков в моче – одно из наиболее массовых исследований, выполняемых в клинико-диагностических лабораториях.
Актуальность проблемы: Определения количества белка в моче позволяют оценить функциональное состояние почек, прогнозировать осложнения, контролировать ход лечения патологии.
Повышение экскреции белка с мочой — протеинурия, сопровождает патологию почек, в то же время белок в моче может иметь преренальное и постренальное происхождение.
Белок Бенс−Джонса – это лёгкие цепи Ig, которые осаждаются при нагревании мочи до температуры 45− 55 °C. Протеины Бенс-Джонса обладают крайне низкой массой молекул, а сам белок вырабатывается плазматическими клетками при формировании злокачественного образования. Присутствуют при миеломной болезни, макроглобулинемии Вальденстрема, лимфолейкозе, болезни Ходжкина.
Микроальбуминурия — это выделение почками (путем клубочковой фильтрации) альбумина в количествах, определить которые с помощью рутинных лабораторных методов (клинический анализ мочи, например, путем осаждения сульфосалициловой кислотой) не удается — от 30 до 300 мг/сутки или от 20 до 200 мкг/минуту. При отсутствии инфекции мочевыводящих путей и острого заболевания повышенная экскреция альбуминов с мочой, как правило, отражает патологию клубочкового аппарата почек.
Альфа-2-макроглобулин – это белок острой фазы воспаления, непрямой показатель повреждения почек. Анализ альфа-2-макроглобулина в моче применяется для диагностики тяжелых гломерулопатий и отторжения трансплантата почки. Чем выше значения белка — тем больше поврежден почечный клубочек и хуже прогноз. Норма: содержание в крови — 1,3-3,0 мг/л, в моче — 0,4-1,6 мг/л.
ß-2-микроглобулин – маркер, свидетельствующий о поражении канальцев почек. Его исследование применяется при злокачественных заболеваниях крови для контроля эффективности лечения, дифференциации тубулярных и клубочковых почечных поражений.
Вывод: Количественное и качественное определение уровня протеинурии имеет важное диагностическое значение, поскольку оно является не только наиболее ранним маркёром заболевания почек, но и важным показателем прогрессирования нефропатий как гломерулярного, так и тубулоинтерстициального ряда.
1. Чернов, А. Н.Основы клинической биохимии [Текст] : учеб. лит. для врачей и студентов мед. вузов / А. Н. Чернов, А. М. Белова, Ю. Н. Копылов ; ОрГМА;. — Оренбург : РИО ОГИМ, 2003. — 247 с
2. Кишкун, А. А.Клиническая лабораторная диагностика [Текст] : учеб. пособие / А. А. Кишкун . — М. : ГЭОТАР-Медиа, 2015. — 720 с.
4. Руководство по лабораторным методам диагностики [Текст] : руководство / А. А. Кишкун. — М. : ГЭОТАР-Медиа, 2007. — 800 с.
КАРДИОРЕНАЛЬНЫЙ СИНДРОМ. ТИПЫ И ПАТОГЕНЕЗ
Нафиков А.В., Астафьев Б.В., Баймешов Ж.С., 4 курс
Научный руководитель – к.м.н., доц. В.А. Шевель
Кафедра факультетской терапии и эндокринологии
Функции сердца и почек тесно связаны. Циркуляция крови определяется тонусом сосудов и объёмом плазмы, регулируемыми почками, на работу которых в свою очередь влияет гемодинамика, формируемая сердцем. Частое сочетание заболеваний сердца и почек связано с общностью их патогенеза и взаимным отягощением. Такое взаимодействие получило название кардиоренального синдрома (КРС). Экспертная группа AcuteDialysisQualityInitiative (ADQI) определяет КРС как патологическое состояние сердца и почек, при котором острое или хроническое нарушение функций одного из этих органов вызывает острое или хроническое нарушение функций другого. [2, c. 256]
Предложено рассматривать пять типов КРС.
I тип — остро развившееся нарушение функций сердца, приводящее к острой почечной дисфункции, например кардиогенный шок при инфаркте миокарда и острая декомпенсация ХСН. При острой кардиальной дисфункции острое повреждение почек развивается не всегда, но в целом оно пропорционально тяжести поражения сердца. КРС возникает в первые дни заболевания и ведёт к повышению летальности вследствие как сердечной, так и почечной дисфункций. Если острая сердечная недостаточность возникла на фоне хронической болезни почек, то почечная дисфункция усиливается. При этом риск неблагоприятного исхода индивидуален и тем выше, чем сильнее снижены почечные функции и чем более стойко нарушены функции сердца. Ингибиторы ангиотензин-превращающего фермента и антагонисты альдостерона, часто используемые в данном случае, могут усугубить почечную дисфункцию и спровоцировать гиперкалиемию. Интенсивная диуретическая терапия также способна оказать отрицательный эффект. Альтернативным лечением служит гемодиализ [1, c. 11-17].
II тип — хроническая кардиальная патология приводит к хронической почечной дисфункции в виде ХБП. Обычно это больные с ХСН, у которых нарушение почечных функций выявляется в половине случаев. Хронические заболевания сердца предрасполагают к почечной дисфункции, а сочетание любых двух факторов сердечно-сосудистого риска повышает вероятность развития ХБП почти в 4 раза. Ведущим механизмом считают снижение почечного кровотока, хотя прямой корреляции между насосной функцией сердца и состоянием почек не выявлено. Снижение почечной функции при ХСН указывает на неблагоприятный прогноз и повышение летальности. При артериальной гипертензии почки являются органом-мишенью, а поражение их сосудистого русла становится фактором прогрессирования ХБП. Стойкая АГ приводит к нефросклерозу, почка уменьшается в объёме, деформируется чашечнолоханочная система.
III тип — острое нарушение почечных функций вызывает острое нарушение деятельности сердца, например гломерулонефрит или острая ишемия почек, механизм генеза значения не имеет. Гиперкалиемия нарушает электрическую активность клеток миокарда и проводящей системы и может приводить к угрожающим жизни аритмиям; при полиорганной недостаточности гиперкалиемия развивается быстрее. Уремия вызывает накопление токсических веществ в полости перикарда, что приводит к перикардиту, когда избыток жидкости, отложение фибрина и сращение листков перикарда серьёзно нарушают гемодинамику. Перикардит развивается на стадии терминальной почечной недостаточности в 20% случаев и требует начала или оптимизации гемодиализа, но может возникнуть и на фоне диализного лечения[5, c.285-295].
IV тип — хроническая почечная дисфункция вызывает долговременные нарушения в работе сердца и сердечно-сосудистой системы. Высокий риск сердечно-сосудистой смертности при хронической почечной недостаточности подтверждён и особенно актуален для пациентов, находящихся на гемодиализе. КРС может возникать со стадии ХБП 3а и выше, когда риск сердечно-сосудистых осложнений выше риска нарастания хронической почечной недостаточности [4, c. 103-106]. Причинами ХБП могут быть сахарный диабет и ангиопатия, атеросклероз почечных артерий, АГ и ХСН, при которой до 20% больных имеют почечную патологию. Поражения сердца имеют хронический характер, формируются длительно, нарастают при падении почечной функции и могут не быть нозологическими формами. Почечная дисфункция приводит к нарастанию ХСН, АГ и нарушениям ритма, но для замедления её прогрессирования необходимы контроль АГ, нормальное кровоснабжение почек и эффективная работа сердца. Общим для хронических заболеваний сердца и почек является нарастающий фиброз, который сам по себе, помимо нейрогуморальных механизмов, приводит к нарушениям их функций. Наличие и прогрессирование почечной дисфункции отягощает течение ХСН и повышает смертность пациентов с АГ. Сочетание ХСН и ХБП приводит к повышению риска развития КРС и росту летальности [3, c. 7-37].
V тип — нарушения функций других органов и систем приводят к развитию сочетанной кардиоренальной патологии. Первичные нарушения могут быть острыми или хроническими, преимущественно влиять на сердце или почки, но их нарастание сопровождается взаимным отягощением сердечной и почечной дисфункции. Сюда относятся коллагенозы, сахарный диабет, сепсис. В половине случаев сепсис сочетается с острым повреждением почек, в 75% — с повышением содержания миокардиальных маркёров. Сочетанная патология ведёт к росту летальных осложнений, а взаимное отягощение двух дисфункций протекает по I или III типу КРС.
Список литературы
1. Авдошина С.В., Ефремовцева М.А., Виллевальде С.В., Кобалава Ж.Д. Острый кардиоренальный синдром: эпидемиология, патогенез, диагностика и лечение. Клин. фармакол. и терап. 2013 (4);
2. Кобалава Ж.Д., Виллевальде С.В., Ефремовцева М.А. Основы кардиоренальной медицины. Под ред. Ж.Д. Кобалава, В.С. Моисеева. М.: ГЭОТАР-Медиа. 2014;
3. Моисеев В.С., Мухин Н.А., Смирнов А.В. и др. Сердечно-сосудистый риск и хроническая болезнь почек: стратегии кардио-нефропротекции. Рос. кардиол. ж. 2014 (8);
4. Сигитова О.Н., Архипов Е.В. Хроническая болезнь почек: новое в классификации, диагностике, нефропротекции. Вестн. соврем. клин. мед. 2014; 7 (1);
5. Boerrigter G., Hocher B., Lapp H. Changes in renal function in congestive heart failure. Curr. Heart Fail. Rep. 2013; 10 (4);
Дата добавления: 2019-03-09 ; просмотров: 78 ; ЗАКАЗАТЬ РАБОТУ
источник
Почечная (истинная) протеинурия бывает функциональной и органической. Среди функциональной почечной протеинурии наиболее часто наблюдаются следующие ее виды:
— физиологическая протеинурия новорожденных, которая исчезает на 4— 10-й день после рождения, а у недоношенных несколько позже;
— ортостатическая альбуминурия, которая характерна для детей в возрасте 7—18 лет и появляется только в вертикальном положении тела;
— транзиторная (инсультная) альбуминурия, причиной которой могут быть различные заболевания органов пищеварения, тяжелая анемия, ожоги, травмы или физиологические факторы: тяжелая физическая нагрузка, переохлаждение, сильные эмоции, обильная, богатая белком пища и др.
Органическая (почечная) протеинурия наблюдается вследствие прохождения белка из крови через поврежденные участки эндотелия почечных клубочков при заболеваниях почек (гломерулонефрит, нефроз, нефросклероз, амилоидоз, нефропатия беременных), расстройствах почечной гемодинамики (почечная венная гипертензия, гипоксия), трофических и токсических (в том числе лекарственных) воздействиях на стенки капилляров клубочков.
Большинство качественных и количественных методов определения белка в моче основаны на его коагуляции в объеме мочи или на границе сред (мочи и кислоты).
Среди качественных методов определения бедка в моче наибольшее распространение получили унифицированная проба с сульфосалициловой кислотой и кольцевая проба Геллера.
Унифицированная проба с сульфасалициловой кислотой проводится следующим образом. В 2 пробирки наливают по 3 мл профильтрованной мочи. В одну из них прибавляют 6—8 капель 20 % раствора сульфасалициловой кислоты. На темном фоне сравнивают обе пробирки. Помутнение мочи в пробирке с сульфасалициловой кислотой указывает на наличие белка. Перед исследованием необходимо определить реакцию мочи, и если она щелочная, то подкислить 2—3 каплями 10 % раствора уксусной кислоты.
Проба Геллера основана на том, что при наличии белка в моче на границе азотной кислоты и мочи происходит его коагуляция и появляется белое кольцо. В пробирку наливают 1—2 мл 30 % раствора азотной кислоты и осторожно по стенке пробирки наслаивают точно такое же количество профильтрованной мочи. Появление белого кольца на границе двух жидкостей указывает на наличие белка в моче. Следует помнить, что иногда белое кольцо образуется при наличии большого количества уратов, но в отличие от белкового кольца оно появляется несколько выше границы между двумя жидкостями и растворяется при нагревании [Плетнева Н.Г., 1987].
Из количественных методов наиболее часто применяются:
1) унифицированный метод Брандберга—Робертса—Стольникова, в основу которого положена кольцевая проба Геллера;
2) фотоэлектроколориметрический метод количественного определения белка в моче по помутнению, образующемуся при добавлении сульфасалициловой кислоты;
3) биуретовый метод.
Выявление белка в моче упрощенным ускоренным методом проводят колориметрическим методом с помощью индикаторной бумаги, которую выпускают фирмы «Lachema» (Словакия), «Albuphan», «Ames» (Англия), «Albustix», «Boehringer» (Германия), «Comburtest» и др. Метод заключается в погружении в мочу специальной бумажной полоски, пропитанной тетрабромфеноловым синим и цитратным буфером, которая меняет свой цвет от желтого до синего в зависимости от содержания белка в моче. Ориентировочно концентрацию белка в исследуемой моче определяют с помощью стандартной шкалы. Для получения правильных результатов необходимо соблюдать следующие условия. рН мочи должна быть в пределах 3,0—3,5; при слишком щелочной моче (рН 6,5) будет получен ложноположительный результат, а при слишком кислой моче (рН 3,0) — ложноотрицательный.
Бумага должна находиться в контакте с исследуемой мочой не дольше, чем указано в инструкции, в противном случае тест даст ложноположительную реакцию. Последнюю также наблюдают и при содержании в моче большого количества слизи. Чувствительность различных видов и серий бумаги может быть различной, поэтому к количественной оценке белка в моче этим методом следует относиться осторожно. Определение его количества в суточной моче при помощи индикаторной бумаги невозможно [Плетнева Н.Г., 1987]
Существует несколько способов определения количества белка, выделившегося с мочой за сутки. Наиболее простым является метод Брандберга —Робертса—Стольникова.
Методика. 5-10 мл тщательно перемешанной суточной мочи наливают в пробирку и осторожно по стенкам ее добавляют 30 % раствор азотной кислоты. При наличии белка в моче в количестве 0,033 % (т.е. 33 мг на 1 л мочи) через 2-3 мин появляется тонкое, но четко видимое белое кольцо. При меньшей его концентрации проба отрицательная. При большем содержании белка в моче его количество определяют путем многократных разведений мочи дистиллированной водой до тех пор, пока не перестанет образовываться кольцо. В последней пробирке, в которой еще видно кольцо, концентрация белка будет составлять 0,033 %. Умножив 0,033 на степень разведения мочи, определяют содержание белка в 1 л неразведенной мочи в граммах. Затем рассчитывают содержание белка в суточной моче по формуле:
где К — количество белка в суточной моче (г); х — количество белка в 1 л мочи (г); V — количество мочи, выделенное за сутки (мл).
В норме в течение суток с мочой выделяется от 27 до 150 мг (в среднем 40—80 мг) белка.
Указанная проба позволяет определить в моче только мелкодисперсные белки (альбумины). Более точные количественные методы (колориметрический метод Кьельдаля и др.) довольно сложны и требуют специальной аппаратуры.
При почечной протеинурии с мочой выделяются не только альбумины, но и другие виды белка. Нормальная протеинограмма (по Зейцу и соавт., 1953) имеет следующее процентное содержание: альбуминов — 20 %, α1-глобулинов — 12 %, α2-глобулинов — 17 %, γ-глобулинов — 43 % и β-глобулинов — 8 %. Отношение альбуминов к глобулинам изменяется при различных заболеваниях почек, т.е. нарушается количественное соотношение между белковыми фракциями.
Наиболее распространенными методами фракционирования уропротеинов являются следующие: высаливание нейтральными солями, электрофоретическое фракционирование, иммунологические методы (реакция радиальной иммунодиффузии по Манчини, иммуноэлектрофоретический анализ, преципитационный иммуноэлектрофорез), хроматография, гель-фильтрация, а также ультрацентрифугирование.
В связи с внедрением методов фракционирования уропротеинов, основанных на изучении электрофоретической подвижности, вариабильности молекулярной массы, размеров и формы молекул уропротеинов, появилась возможность выделять характерные для того или иного заболевания типы протеинурии, изучать клиренсы индивидуальных плазменных белков. К настоящему времени в моче идентифицировано свыше 40 плазменных белков, В том числе в нормальной моче 31 плазменный белок [Berggard, 1970].
В последние годы появилось понятие селективности протеинурии. В 1955 г. Hardwicke и Squire сформулировали понятие «селективная» и «неселективная» протеинурия, определив, что фильтрация плазменных белков в мочу подчиняется определенной закономерности: чем больше молекулярная масса белка, экскретируемого в мочу, тем меньше его клиренс и тем ниже концентрация его в окончательной моче. Протеинурия, соответствующая этой закономерности, является селективной в отличие от неселективной, для которой характерным является извращение выведенной закономерности.
Обнаружение в моче белков с относительно большой молекулярной массой свидетельствует об отсутствии избирательности почечного фильтра и выраженном его поражении. В этих случаях говорят о низкой селективности протеинурии. Поэтому в настоящее время широкое распространение получило определение белковых фракций мочи с использованием методов электрофореза в крахмальном и полиакриламидном геле. По результатам этих методов исследования можно судить о селективности протеинурии.
По данным В.С.Махлиной (1975), наиболее оправданным является определение селективности протеинурии путем сравнения клиренсов 6—7 индивидуальных белков плазмы крови (альбумина, транеферрина, α2 — макроглобулина, IgA, IgG, IgM) с использованием точных и специфичных количественных иммунологических методов реакции радиальной иммунодиффузии по Манчини, иммуноэлектрофоретического анализа и преципитального иммуноэлектрофореза. Степень селективности протеинурии определяют по индексу селективности, представляющего собой отношение сравниваемого и эталонного белков (альбумина).
Изучение клиренсов индивидуальных плазменных белков позволяет получить достоверные сведения о состоянии фильтрационных базальных мембран клубочков почки. Связь между характером экскретируемых в мочу белков и изменениями базальных мембран клубочков настолько выражена и постоянна, что по уропротеинограмме можно косвенно судить о патофизиологических изменениях в клубочках почек. В норме средний размер пор гломерулярной базальной мембраны составляет 2,9—4 А° НМ, которые могут пропускать белки, имеющие молекулярную массу до 10 4 (миоглобулин, кислый α1 — гликопротеин, легкие цепи иммуноглобулинов, Fc и Fab — фрагменты IgG, альбумин и трансферрин).
При гломерулонефрите, нефротическом синдроме размеры пор в базальных мембранах клубочков увеличиваются, в связи с чем базальная мембрана становится проницаемой для белковых молекул большого размера и массы (церулоплазмин, гаптоглобин, IgG, IgA и др.). При крайней степени повреждения клубочков почек в моче появляются гигантские молекулы белков плазмы крови (α2-макроглобулин, IgM и β2-липопротеин).
Определяя белковый спектр мочи, можно сделать заключение о преимущественном поражении тех или иных участков нефрона. Для гломерулонефрита с преимущественным поражением гломерулярных базальных мембран характерно наличие в моче крупно- и среднемолекулярных белков. Для пиелонефрита с преимущественным поражением базальных мембран канальцев характерны отсутствие крупномолекулярных и наличие повышенных количеств средне- и низкомолекулярных белков.
Концентрацию этого белка в плазме крови и моче определяют радиоиммунологическим методом с помощью стандартного набора «Phade-bas β2-mikroiest» (фирма «Pharmaсia», Швеция). В сыворотке крови здоровых людей содержится в среднем 1,7 мг/л (колебания от 0,6 до 3 мг/л), в моче — в среднем 81 мкг/л (максимально 250 мкг/л) β2-микроглобулина. Превышение его в моче свыше 1000 мкг/л — явление патологическое. Содержание β2-микроглобулина в крови увеличивается при заболеваниях, сопровождающихся нарушением клубочковой фильтрации, в частности при остром и хроническом гломерулонефрите, поликистозе почек, нефросклерозе, диабетической нефропатии, острой почечной недостаточности.
Концентрация β2-микроглобулина в моче повышается при заболеваниях, сопровождающихся нарушением реабсорбционной функции канальцев, что приводит к увеличению экскреции его с мочой в 10—50 раз, в частности, при пиелонефрите, ХПН, гнойной интоксикации и др. Характерно, что при цистите в отличие от пиелонефрита не наблюдается увеличения концентрации β2-микроглобулина в моче, что может быть использовано для дифференциальной диагностики этих заболеваний. Однако при интерпретации результатов исследования надо учитывать, что любое повышение температуры всегда сопровождается увеличением экскреции β2-микроглобулина с мочой.
Средние молекулы (СМ), иначе называемые белковыми токсинами, представляют собой вещества с молекулярной массой 500—5000 дальтон. Физическая структура их неизвестна. В состав СМ входят по меньшей мере 30 пептидов: окситоцин, вазопрессин, ангиотензин, глюкагон, адренокортикотропный гормон (АКТГ) и др. Избыточное накопление СМ наблюдается при снижении функции почек и содержании в крови большого количества деформированных белков и их метаболитов. Они обладают разнообразным биологическим действием и нейротоксичны, вызывают вторичную иммунодепрессию, вторичную анемию, угнетают биосинтез белка и эритропоэз, тормозят активность многих ферментов, нарушают течение фаз воспалительного процесса.
Уровень СМ в крови и моче определяют скрининговым тестом, а также путем спектрофотометрии в ультрафиолетовой зоне по длине волны 254 и 280 мм на спектрофотометре ДИ-8Б, а также динамической спектрофотометрии с компьютерной обработкой в диапазоне волн 220—335 нм на том же спектрометре фирмы Beckman. За норму принимают содержание СМ в крови, равное 0,24 ± 0,02 усл. ед., а в моче — 0,312 ± 0,09 усл. ед.
Будучи нормальными продуктами жизнедеятельности организма, они удаляются из него в норме ночками путем гломерулярной фильтрации на 0,5 %; 5 % их утилизируется другим путем. Все фракции СМ подвергаются канальцевой реабсорбции.
Кроме белков плазмы крови, в моче могут быть неплазменные (тканевые) протеины. По данным Buxbaum и Franklin (1970), неплазменные белки составляют приблизительно 2/3 всех биоколлоидов мочи и значительную часть уропротеинов при патологической протеинурии. Тканевые белки попадают в мочу непосредственно из почек или органов, анатомически связанных с мочевыми путями, или попадают из других органов и тканей в кровь, а из нее через базальные мембраны клубочков почки — в мочу. В последнем случае экскреция в мочу тканевых протеинов происходит аналогично выведению плазменных белков различной молекулярной массы. Состав неплазменных уропротеинов чрезвычайно разнообразен. Среди них гликопротеины, гормоны, антигены, ферменты (энзимы).
Тканевые протеины в моче выявляют с помощью обычных методов белковой химии (ультрацентрифугирование, гель-хроматография, различные варианты электрофореза), специфических реакций на ферменты и гормоны и иммунологических методов. Последние позволяют также определить концентрацию неплазменного уропротеина в моче и в ряде случаев определить тканевые структуры, ставшие источником его появления. Основным методом выявления в моче неплазменного белка является иммунодиффузионный анализ с антисывороткой, полученной иммунизацией экспериментальных животных мочой человека и истощенной (адсорбированной) в последующем белками плазмы крови.
При патологическом процессе наблюдаются глубокие нарушения жизнедеятельности клеток, сопровождающиеся выходом внутриклеточных ферментов в жидкостные среды организма. Энзимодиагностика базируется на определении ряда ферментов, выделившихся из клеток пораженных органов и не свойственных сыворотке крови.
Исследования нефрона человека и животных показали, что в отдельных его частях имеется высокая ферментативная дифференциация, тесно связанная с функциями, которые выполняет каждый отдел. В клубочках почки содержится относительно небольшое количество различных энзимов.
Клетки почечных канальцев, особенно проксимальных отделов, содержат максимальное количество энзимов. Высокая их активность наблюдается в петле Генле, прямых канальцах и собирательных трубочках. Изменения активности отдельных энзимов при различных заболеваниях почек зависят от характера, остроты и локализации процесса. Они наблюдаются до появления морфологических изменений в почках. Поскольку содержание различных ферментов четко локализовано в нефроне, определение того или иного фермента в моче может способствовать топической диагностике патологического процесса в почках (клубочки, канальцы, корковый или мозговой слой), дифференциальной диагностике почечных заболеваний и определению динамики (затухание и обострение) процесса в почечной паренхиме.
Дли дифференциальной диагностики заболеваний органов мочеполовой системы применяют определение активности в крови и моче следующих ферментов: лактатдегидрогеназы (ЛДГ), лейцинаминопептидазы (ЛАП), кислой фосфатазы (КФ), щелочной фосфатазы (ЩФ), β-глюкуронидазы, глютамино-щавелевоуксусной трансаминазы (ГЩТ), альдолазы, трансамидиназы и др. Активность ферментов в сыворотке крови и в моче определяют с помощью биохимических, спектрофотометрических, хроматографических, флуориметрических и хемилюминесцентных методов.
Энзимурия при заболеваниях почек более выражена и закономерна, чем энзимемия. Она особенно сильно выражена в острой стадии заболевания (острый пиелонефрит, травма, распад опухоли, инфаркт почки и т.д.). При этих заболеваниях обнаруживается высокая активность трансамидиназы, ЛДГ, ЩФ и КФ, гиалуронидазы, ЛАП, а также таких неспецифических энзимов, как ГЩТ, каталаза [Полянцева Л.Р., 1972].
Селективная локализация ферментов в нефроне при обнаружении ЛАП и ЩФ в моче позволяет с уверенностью говорить об острых и хронических заболеваниях почек (острая почечная недостаточность, некроз почечных канальцев, хронический гломерулонефрит) [Шеметов В.Д., 1968]. По данным А.А.Карелина и Л.Р.Полянцевой (1965), трансамидиназа содержится лишь в двух органах — почке и поджелудочной железе. Она является митохондриальным ферментом почек и в норме в крови и моче отсутствует. При различных заболеваниях почек трансамидиназа появляется в крови и в моче, а при поражении поджелудочной железы — только в крови.
Дифференциальным тестом в диагностике гломерулонефрита и пиелонефрита Krotkiewski (1963) считает активность ЩФ в моче, повышение которой более характерно для пиелонефрита и диабетического гломерулосклероза, чем для острого и хронического нефрита. Нарастающая в динамике амилаземия при одновременном снижении амилазурии может указывать на нефросклероз и сморщивание почки, ЛАП имеет наибольшее значение при патологических изменениях в клубочках и извитых канальцах почки, поскольку содержание ее в этих отделах нефрона более высокое [Шепотиновский В.П. и др., 1980]. Для диагностики волчаночного нефрита рекомендуется определение β-глюкуронидазы и КФ [Приваленко М.Н. и др., 1974].
При оценке роли энзимурии в диагностике заболеваний почек следует учитывать следующие положения. Энзимы, будучи по своей природе белками, при малой молекулярной массе могут проходить через неповрежденные клубочки, определяя так называемую физиологическую энзимурию. Среди этих энзимов постоянно определяются в моче α-амилаза (относительная молекулярная масса 45 ООО) и уропепсин (относительная молекулярная масса 38000).
Наряду с низкомолекулярными энзимами в моче здоровых лиц могут быть обнаружены в небольшой концентрации и другие энзимы: ЛДГ, аспартат- и аланинаминотрансферазы, ЩФ и КФ, мальтаза, альдолаза, липаза, различные протеазы и пептидазы, сульфатаза, каталаза, рибонуклеаза, пероксидаза [King, Воусе, 1963].
Высокомолекулярные энзимы с относительной молекулярной массой больше 70000-100000, по мнению Richterich (1958) и Hess (1962), могут проникать в мочу лишь при нарушении проницаемости клубочкового фильтра. Нормальное содержание ферментов в моче не позволяет исключить патологический процесс в почке при окклюзии мочеточника. При эпзимурии возможен выход энзимов не только из самих почек, но и из других паренхиматозных органов, клеток слизистых оболочек мочевых путей, предстательной железы, а также форменных элементов мочи при гематурии или лейкоцитурии.
Большинство энзимов неспецифично по отношению к почке, поэтому откуда происходят энзимы, обнаруженные в моче здоровых и больных, установить трудно. Однако степень энзимурии даже дли неспецифичных энзимов при поражении почек бывает выше нормы или той, которая наблюдается при заболеваниях других органов. Более ценную информацию может дать комплексное исследование в динамике ряда ферментов, особенно органоспецифичных, таких как трансаминаза.
В решении вопроса о почечном происхождении энзима в моче помогает исследование изоэнзимов с выявлением фракций, типичных для изучаемого органа. Изоэнзимы — это энзимы, изогенные по действию (катализируют одну и ту же реакцию), но гетерогенные по химической структуре и другим свойствам. Каждая ткань имеет характерный для нее изоэнзимный спектр. Ценными методами разделения изоэнзимов являются электрофорез в крахмальном и полиакриламидном геле, а также ионообменная хроматография.
При миеломной болезни и макроглобулинемии Вальденстрема в моче обнаруживают белок Бенс-Джонса. Метод обнаружения названного белка в моче основан на реакции термопреципитации. Применявшиеся ранее методы, с помощью которых оценивают растворение этого белка при температуре 100 °С и повторное осаждение при последующем охлаждении, ненадежны, так как не все белковые тела Бенс-Джонса обладают соответствующими свойствами.
Более достоверно выявление этого парапротеина путем осаждения его при температуре 40 -60 °С. Однако и в этих условиях осаждения может не произойти в слишком кислой (рН 6,5) моче, при низкой ОПМ и низкой концентрации белка Бенс-Джонса. Наиболее благоприятные условия для его осаждения обеспечивает методика, предложенная Patnem: 4 мл профильтрованной мочи смешивают с 1 мл 2 М ацетатного буфера рН 4,9 и согревают 15 мин на водяной бане при температуре 56 °С. При наличии белка Бенс-Джонса в течение первых 2 мин появляется выраженный осадок.
При концентрации белка Бенс-Джонса меньше 3 г/л проба может быть отрицательной, но на практике это встречается крайне редко, поскольку его концентрация в моче, как правило, более значительна. На пробы с кипячением нельзя вполне полагаться. С полной достоверностью он может быть обнаружен в моче иммуно-электрофоретическим методом с использованием специфических сывороток против тяжелых и легких цепей иммуноглобулинов.
источник